Материал: Вр. гипотиреоз schit
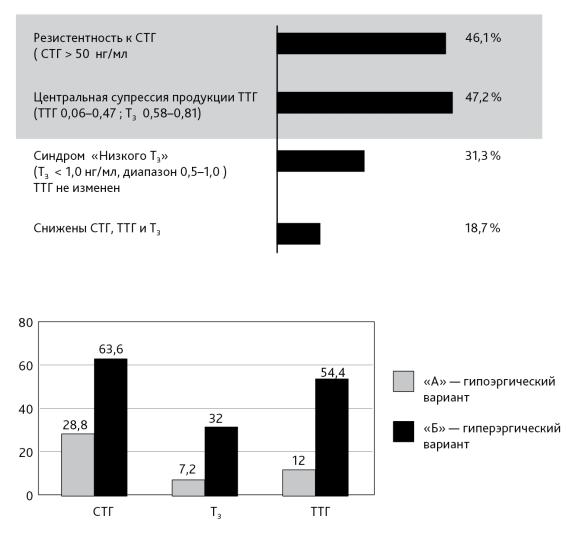
Рис. 2. Частота гормональных нарушений при гипоэргическом варианте сепсиса
Рис. 3. Содержание СТГ, Т3, ТТГ при гипоэргическом (вариант «А») и гиперэргическом (вариант «Б») неонатальном сепсисе (в сопоставимых единицах) (разгар процесса)
Обращает на себя внимание, что первое определение уровней гормонов (1–3-й дни жизни) обнаружило в группе больных с гипоэргическим вариантом сепсиса у 97,2 % новорожденных низкие значения ТТГ или Т3, то есть исходно дети данной группы имели признаки «незрелости» щитовидной железы, очевидно являющиеся результатом тяжелого антенатального страдания. В группе больных с гиперэргическим вариантом такие дети составляли лишь 7,8 %.
Гормональный профиль в разгар процесса при 2 вариантах течения неонатального сепсиса: гипоэргического («А») и гиперэргического («Б») существенно отличался (рис. 3).
Ни у одного больного с вариантом «Б» — гиперэргическим не было выявлено низкого содержания трийодтиронина (Т3). В то время как при варианте «А» зарегистрированы (рис. 3):
•синдром «низкого Т3» (Т3 < 1,0 нг/мл, диапазон 0,5–1,0; ТТГ не изменен) —
у 31,3 % детей.
•центральная супрессия продукции ТТГ (ТТГ — 0,06–0,47 мМЕ/л;
•Т3 — 0,58–0,81 нг/мл) имела место у 47,2 %;
•низкие уровни всех трех гормонов (СТГ, ТТГ, Т3) — у 18,7 % детей.
•резистентность к СТГ у 46,1 % детей данной группы (СТГ > 50 нг/мл; диапазон 51–135 нг/мл).
Таким образом, при гипоэргическом варианте сепсиса у подавляющего большинства детей имела место как дисфункция гипофизарно-тиреоидной системы уже к моменту рождения, так и гипотиреоидизм септического генеза в разгар сепсиса. По
нашему мнению, сниженная секреция ТТГ может быть в определенной мере связана с эффектом дофамина при длительной инотропной поддержке.
Дети с гиперэргическим вариантом характеризовались большей зрелостью оси гипоталамус–гипофиз–щитовидная железа. Эпизоды сниженного уровня ТТГ (< 1,7 мМЕ/л) без снижения Т3 отмечены у 34,6 % детей данной группы. При гиперэргическом варианте 15,4 % детей имели даже повышенный уровень Т3 (более 2,8 нг/мл).
Другой особенностью данного варианта была высокая частота резистентности к гормону роста (СТГ > 50 нг/мл; диапазон 51–135 нг/мл). Она отмечалась у 65,3 % детей при варианте «Б» и лишь у 25,5 % — при варианте «А». По нашим данным, повышенное содержание СТГ в начальной стадии сепсиса и прогрессивное его снижение в динамике, а также возрастание уровня Т3 являются благоприятными признаками. Неблагоприятный исход коррелировал с низкими уровнями всех названных гормонов.
Выделенные нами, гиперэргический («А») и гипоэргический («В»), варианты сепсиса отличаются по концентрации всех изученных гормонов. Полученные нами данные об исходно низких концентрациях ТТГ и Т3, низком уровне общего белка, низком IgG при гипореактивном варианте «А» указывают на незрелость системы гипоталамус–гипофиз–щитовидная железа уже при рождении и предполагают несостоятельность механизмов иммунологической защиты и их гормонального обеспечения, что отличает эту группу от гиперэргического варианта «Б».
Гипотиреоидизм септического генеза, отмеченный нами только при гипоэргическом варианте, согласуется с представлением о повреждающем эффекте эндотоксина, в частности рецепторов для ТТГ на фолликулярных клетках щитовидной железы. В целом такой вариант сепсиса можно охарактеризовать как «дефицитный». Необходимо иметь ввиду не только дефицит гормонов и других белков, энергодефицит, но и дефицит лимфокинов вследствие лимфопении, а также возможный дефицит цитокинов моноцитарного происхождения.
У детей с гиперэргическим вариантом не отмечено признаков угнетения функции щитовидной железы как исходно, так и в ходе септического процесса.
Повышенную продукцию Т3 (15,4 % детей) мы наблюдали только при гиперэргическом варианте «Б». В этой же группе характерной чертой гормонального профиля был высокий базальный уровень СТГ.
Возможно, в формирование особенностей эндокринного статуса у новорожденных детей с гипоэргическим вариантом сепсиса вносят вклад генетические факторы. Весомым аргументом за эту взаимосвязь является высокая частота эндокринных расстройств и аллергических заболеваний у матерей детей данной группы, хронических очагов инфекции упервобеременных женщин.
Патология щитовидной железы у новорожденных
Транзиторный гипотиреоз
Транзиторный гипотиреоз обнаруживается по результатам неонатального скрининга у 1–2 % новорожденных. У недоношенных детей частота его возрастает до 15 %, а у новорожденных гестационного возраста 28–32 нед., перенесших тяжелую гипоксию или гнойно-септическое заболевание, — до 75 % [30, 31].
Установлено, что транзиторный гипотиреоз более распространен в Европе (1 : 10 000), чем в США (1 : 50 000) [28]. По мнению некоторых авторов, это объясняется широким распространением йодного дефицита в Европейских странах [24, 71].
Гипотироксинемия недоношенных
Этот термин относится к патологии, возникающей у недоношенных новорожденных (особенно родившихся до 30 недель), у которых постнатальный подъем тироксина наименее выражен, а в первую неделю жизни происходит его падение ниже уровня концентрации в пуповинной крови. В последующие 3–6 недель происходит
постепенное (в течение нескольких месяцев) повышение тироксина до концентраций, характерных для доношенных детей.
Транзиторная гипотироксинемия развивается у 85 % недоношенных детей. В типичных случаях Т4 низкий, но сТ4, Т3 и ТТГ в пределах нормы (в отличие от транзиторного гипотиреоза, когда уровень ТТГ повышен). Причиной гипотироксинемии недоношенных считают функциональную незрелость гипоталамуса и недостаточный выброс ТРГ, а также снижение уровня ТСГ (вызванное голоданием, респираторным дистресс-синдромом и другими формами тяжелой перинатальной патологии) [26, 72].
Гипотироксинемия у недоношенных ассоциируется (даже с учетом поправки на другие перинатальные факторы риска) с увеличением смертности и заболеваемости в постнеонатальном периоде: увеличением длительности ИВЛ и кислородотерапии, увеличением частоты возникновения ВЖК, повреждений белого вещества мозга, ДЦП, задержек умственного развития. Однако не известно, является ли связь между низким уровнем Т3 или Т4 и краткосрочной заболеваемостью, смертностью и долгосрочной инвалидностью причинной или отражает тяжесть заболевания (состояния) самих недоношенных детей [73].
В респираторной системе тиреоидные гормоны необходимы для нормального синтеза сурфактанта [74] и механизмов абсорбции внутриальвеолярной жидкости [75, 76]. У недоношенных детей, с развившейся «болезнью гиалиновых мембран» определяется более низкий уровень Т3 и Т4, чем в контрольной группе [77]. На деятельность миокарда тиреоидные гормоны оказывают положительный инотропный и хронотропный эффекты [78], пренатальный уровень Т3 и Т4 и их постнатальное повышение имеют важное значение для сократимости и метаболизма сердечной мышцы [79]. У новорожденных, имеющих пороки сердца, требующих применения ИВЛ и других экстракорпоральных средств поддержания жизнедеятельности, уровень циркулирующих тиреоидных гормонов снижается [79]. Наконец, транзиторный гипотиреоз новорожденных (ТГН) ассоциирован с более поздним закрытием артериального протока [80].
По данным ряда обсервационных исследований больших когорт новорожденных, было показано, что низкий уровень тиреоидных гормонов в первые недели жизни сочетался с худшим неврологическим развитием [72]. В раннем детстве (18–24 месяца) дети, имевшие ТГН, отличались большей частотой когнитивных расстройств, чем дети, не имевшие подобных нарушений. Среднее снижение в группе по шкале психического развития Bayley составило 6,8–8,3 пункта, что примерно соответствует половине стандартного отклонения [81], а у более старших детей отмечено снижение IQ на 8,3 пункта [82]. Эта закономерность сохранялась и после перерасчета с учетом различных антенатальных и неонатальных факторов риска, которые могли влиять на психическое развитие. Было показано, что эти когнитивные нарушения сохранялись с возрастом [42], и проблемы со школьным обучением у детей, перенесших ТГН, возникали чаще, чем в контрольной группе [83].
Риск моторных и неврологических нарушений при ТГН также оказался повышен [84]. Помимо нарушений психического развития, ТГН ассоциирована с риском возникновения детского церебрального паралича, частота которого для детей, перенесших тяжелую ТГН, увеличивается в 2–6 раз [85].
При обследовании когорты недоношенных детей, рожденных между 24-й и 35- й неделями беременности и развивших ТГН, было показано, что в 14 месяцев жизни у них по сравнению с контрольной группой были значимо снижены многочисленные показатели (например, общая и мелкая моторика, зрительно-пространственные способности, языковые навыки). Интересно, что, по данным указанных авторов, уровень свободного T4 на 2-й неделе жизни имел прогностическое значение в отношении развития многих из этих навыков, особенно языковых. То есть ТГН ассоциирована не только с общим снижением неврологического развития, но и с нарушением развития визуальных и лингвистических способностей. Тем не менее в настоящее время остается не вполне понятным вопрос, обусловлены ли эти нарушения непосредственно ТГН или ТГН является результатом других факторов, которые сами по себе приводят к указанным нарушениям развития [72].
Необходима ли дотация гормонов ЩЖ недоношенным детям с гипотироксинемией?
При низком уровне тироксина и стойком повышении уровня ТТГ, характерном как для преходящего, так и для необратимого гипотиреоза, лечение тироксином проводят до тех пор, пока не станет ясна природа гипотироксинемии. Однако надо ли назначать лечение при низком уровне тироксина в сочетании с нормальным уровнем ТТГ — вопрос спорный.
Начиная с 1980-х годов, ряд исследователей изучали влияние заместительной терапии Т4 и/или Т3 на психомоторное развитие недоношенных младенцев. Исходным посылом для этих исследований было изучение того, как заместительная терапия при ТГН отразится на заболеваемости (смертности) и неврологическом развитии детей. Необходимо заметить, что исследования, предпринятые в 1980-х годах, были выполнены в эру до использования сурфактанта и антенатального назначения глюкокортикоидов в рутинной клинической практике. Кроме того, исследования в первую очередь фокусировались не на неврологическом развитии детей, а на неонатальной смертности и заболеваемости [72].
Впервом исследовании заместительной терапии при развившемся ТГН Schonberger et al. (1981) назначали каждому второму ребенку, родившемуся до срока 37 недель или
весом менее 2200 г 25 мкг L Т4 и 5 мкг L Т 3. В результате смертность среди детей, получавших лечение статистически значимо уменьшилась (6,6 % против 29 %) [72].
Ряд исследований проанализировали последствия назначений левотироксина недоношенным детям независимо от концентрации в сыворотке у них тиреоидных гормонов [57]. Проведено двойное слепое плацебо-контролируемое исследование (лечения тироксином 20 мкг/кг/день внутривенно, потом внутрь; с 1-го дня в течение двух недель) младенцев, родившихся на 25–30-й неделе беременности. Не доказано влияние на смертность, частоту возникновения респираторных осложнений, в том числе хронических заболеваний легких, ВЖК, ретинопатий недоношенных, показателей роста и нервнопсихического развития (индекс Бейли) в 7 месяцев скорректированного возраста [40, 57].
Вдругом исследовании сравнивали лечение тироксином с лечением плацебо у недоношенных с 25–28 недель гестационного возраста и доказанной гипотироксинемией
(Т4 менее 4 мкг/дл (51,5 нмоль/л) и ТТГ менее 20 МЕ/л) [58]. Младенцы получали плацебо или левотироксин 10 мкг/кг в день внутримышечно или перорально с 15-го дня до 7-й недели жизни. Не было никаких существенных различий в динамике набора веса, роста, росте окружности головы, частоте БЛД, ОАП, НЭК или ретинопатии недоношенных [40,
58].
Вкрупном исследовании van Wassenaer et al. (1997) 200 детей с 25–30 недель гестационного возраста получали левотироксин перорально 8 мкг/кг в день или плацебо с первых суток до 6 недель жизни. Не выявлено никакой связи между начальной
концентрацией свободного Т4 и конечным эффектом лечения. В 24 месяца жизни не было никакой разницы в показателях психомоторного развития. Когда исследователи проанализировали данные недоношенных, рожденных после 27 недель, то показатели нервно-психического развития детей, леченных левотироксином, были более низкими, чем в группе плацебо. Авторы предположили, что худшие результаты пролеченных детей
сгестационным возрастом более 27 недель показывают потенциальное пагубное воздействие возможного состояния гипертиреоза у них [37, 40, 86].
Вработе C. F. Crowther et al. (1997) было показано, что дородовое введение 200 мкг тиреотропин-рилизинг-гормона в дополнение к кортикостероидам женщинам с риском преждевременных родов, было связано с риском задержки двигательного и социального развития, сенсорными нарушениями у детей в возрасте 12 месяцев [87].
В2003 году Biswas et al. провели рандомизированное исследование влияния
терапии ТГ на исходы респираторных расстройств у 253 детей, рожденных раньше 30 недель гестации. Дети на протяжении первых 7 дней жизни получали либо плацебо, либо комбинацию L-T3 в дозе 6 мкг/кг в день и гидрокортизон в виде постоянной внутривенной инфузии. В результате выяснилось, что в обеих группах прогноз частоты развития и тяжести респираторных расстройств не отличался [72]. B работе Wassenaer et
al. было показано, что дети, рожденные ранее 28-й недели беременности, если они получали L-T4, имели стабильную среднесуточную ЧСС на протяжении первых 4 недель жизни, в отличие от младенцев, получавших плацебо, у которых происходило снижение ЧСС между 7-м и 14-м днями [72, 86, 88].
Результаты ранних исследований, изучавших неврологическое развитие, неоднозначны. Crowdhry et al. выявили статистически незначимое снижение психического развития (на 11,4 пункта) у детей, которые получали лечение, на 12-м месяце жизни, при этом в 24 месяца каких-либо отличий уже не было [72, 89]. Vanhole et al. показали, что у детей, получавших L-T4, происходило снижение на 5 пунктов по шкалам, оценивающим как двигательные, так и психические навыки, но эти изменения не были статистически значимыми [72, 57].
Висследование van Wassenaer et al. были включены 200 недоношенных младенцев,
рожденных ранее 30-й недели беременности; половина из них получала 8 мкг/кг L-T4 на протяжении 6 недель, другая половина — плацебо. Свободные и общие T4, T3, rT3, ТТГ и тироксинсвязывающий глобулин определялись на 0, 3, 7, 14, 21, 28, 35, 42 и 56-е сутки после рождения, а неврологическое развитие оценивалось через 0,5; 1; 2; 5, 7 и 10 лет. Хотя статистически значимых отличий между двумя группами детей выявлено не было,
при анализе выяснилось, что эффект терапии L-T4 зависел от гестационного возраста недоношенных. В возрасте 2 лет у детей, рожденных до 27-й недели и получавших L-T4, индекс психического развития (MDI) был на 18 пунктов выше, чем в аналогичной группе недоношенных, получавших плацебо. В противоположность этому у детей, рожденных между 27-й и 30-й неделями, индекс MDI оказался на 10 пунктов ниже, чем у получавших плацебо. В возрасте 5 лет, у детей, рожденных до 27-й недели беременности, получавших
L-T4, поведенческие и психические баллы были выше, чем у получавших плацебо, но эти отличия не были статистически значимы [72, 86, 88]
Вгруппе детей, получавших L-T4 и рожденных между 27-й и 29-й неделями, определялись лучшие показатели по двигательной шкале по сравнению с получавшими плацебо (2 % против 14 %, включая случаи ДЦП) [72, 97], но худшие по показателям когнитивного развития. В возрасте 10 лет оказалось, что получавшим плацебо и рожденным ранее 27 недель беременности в 5 раз чаще потребовалось специальное
школьное обучение, по сравнению с получавшими L-T4, и этот феномен был инвертирован для детей, рожденных между 27-й и 29-й неделями беременности [72, 86, 88].
Результаты продолжающихся исследований, которые были организованы после широкого внедрения в клиническую практику искусственного сурфактанта, пока еще находятся в стадии анализа. В исследовании TIPIT при помощи различных неврологических визуализирующих методов будет оценено развитие головного мозга, а также развитие детей, рожденных раньше 28 недель беременности. В этом исследовании могут быть получены очень важные данные о влиянии ТГ на развитие головного мозга у недоношенных детей [90, 91].
Хотя ряд исследований, посвященных лечению ТНГ, свидетельствует о преимуществах назначения L-тироксина, ни одно из них не приводит конкретных доказательств необходимости терапии L-тироксином у всех глубоко недоношенных новорожденных. Тем не менее интересно заметить, что, по данным опроса неонатологов,
примерно треть из них склонны назначать терапию L-T4 при ТНГ, а 20 % делают это регулярно [92].
Выпущенные на сегодняшний день клинические рекомендации не поддерживают назначение препаратов тиреоидных гормонов детям со сниженным уровнем T4, за исключением тех случаев, когда имеется и повышенный уровень ТТГ. Неблагоприятные эффекты назначения L-тироксина могут быть обусловлены передозировкой, необоснованным назначением терапии и/или слишком длительным сроком лечения. Кроме того, необходимо учитывать и уровень потребления йода в популяции [58, 49, 93,
94].
Имеющиеся данные «не поддерживают профилактическое использование гормонов щитовидной железы у недоношенных детей для снижения уровня неонатальной