Материал: Вр. гипотиреоз schit
Фактор |
Влияние |
|
|
|
|
|
гипотиреоза вследствие йодной недостаточности |
|
|
|
|
Тиоцианаты |
Тиоцианаты, при курении или употреблении тиоцианат-содержащих продуктов, могут |
|
ухудшить течение эндемического гипотиреоза |
||
|
||
|
|
|
|
Антитиреоидные препараты подавляют гормонопоэз ЩЖ, вмешиваясь в действие ключевого |
|
|
фермента щитовидной железы — пероксидазы. Для детей, имеющих индуцированный |
|
Материнские |
антитиреоидными препаратами гипотиреоз, характерно наличие увеличенной щитовидной |
|
антитиреоидные |
железы, что может в тяжелых случаях привести к дыхательным расстройствам. Гипотиреоз и |
|
препараты |
зоб спонтанно разрешаются по мере выведения препарата из организма (через 1–2 недели |
|
(пропилтиоурацил, |
после рождения). |
|
метимазол) |
Антитиреоидные препараты выделяются в грудное молоко (пропилтиоурацил в меньшей |
|
|
степени). Однако экскреция невелика, и грудное вскармливание считается безопасным, если |
|
|
у матери доза пропилтиоурацила составляет менее 150 мг в день |
|
|
|
|
|
Стероиды и дофамин, которые обычно используются в лечении больных недоношенных |
|
Дофамин, стероиды, |
детей, тормозят секрецию ТТГ. |
|
аминофиллин, |
Аминофиллин, кофеин также могут быть факторами риска развития гипотироксинемии |
|
кофеин, литий |
недоношенных. Прием матерью лития — причина зоба, врожденного гипотиреоза у |
|
|
новорожденных |
|
|
|
|
Стимулирующие |
Эти антитела могут конкурировать с ТТГ за связывание с рецепторами, оказывая |
|
(тиреоид- |
стимулирующее или блокирующее влияние. |
|
стимулирующие |
Материнские стимулирующие и блокирующие антитела к рецепторам ТТГ |
|
иммуноглобулины) и |
(иммуноглобулины класса G) легко проникают через плаценту. Если они представлены в |
|
блокирующие |
достаточно высоком титре, то могут иметь существенное влияние на функцию щитовидной |
|
(тиротропин- |
железы плода (другие антитела, такие как антитела к тиреоглобулину и тиреоидной |
|
связывающий |
пероксидазе, тоже могут проникать через плаценту, но они не приводят к повреждающим |
|
ингибиторный |
эффектам у новорожденных). |
|
иммуноглобулин) |
Стимулирующие и блокирующие антитела к рецепторам ТТГ могут выделяться в грудное |
|
антитела к |
молоко, однако современные рекомендации поддерживают продолжение грудного |
|
рецепторам ТТГ |
вскармливания |
|
|
|
|
Критические |
При тяжелой перинатальной патологии (сепсис, НЭК, ОАП, зависимость от кислорода в |
|
28-дневном возрасте) секреция Т4 ЩЖ снижается, активность D3 увеличивается, что |
||
заболевания, не |
||
приводит к увеличению конверсии Т4 в рТ3. Стероиды, цитокины, увеличение концентрации |
||
связанные с |
||
свободных жирных кислот, снижение потребления калорий, вероятно, способствуют |
||
патологией ЩЖ |
||
снижению активности D1 |
||
|
||
|
|
Ниже мы рассмотрим особенности функционирования ЩЖ и содержания гормонов у различных групп новорожденных.
Доношенные новорожденные:
•Рост уровня ТТГ (из-за перерезки пуповины, снижения температуры окружающей среды) отмечается через 15–30 минут после родов. Максимальная концентрация 60– 80 мЕД/л (50–100 мЕД/л) с последующим снижением на протяжении примерно 24– 48 часов. Хотя конкретные значения, полученные в различных клинических лабораториях, несколько отличаются, уровни сывороточного ТТГ более 20 мЕД/л через 24 часа после рождения и более 10 мЕД/л после первой недели жизни свидетельствуют о первичном гипотиреозе. Обычно дети с транзиторным гипотиреозом имеют концентрации ТТГ 20–40 мкЕД/мл [47, 48].
•Стимуляция ЩЖ и увеличение концентрации Т4 и Т3 в сыворотке. Рост ТТГ инициирует увеличение в 24–36 часа жизни уровней Т4 и свободного Т4 до 17 мкг/дл (218,8 нмоль/л) и 3,5 нг/дл (45,0 пмоль/л) соответственно [48].
•В результате уровень Т4 увеличивается в 2 раза, а уровень Т3 — в 8 раз [47, 49, 50].
•В раннем неонатальном периоде Т4 увеличивается до концентрации, более высокой, чем в любое другое время жизни, а затем постепенно снижается в последующие 4–5 недель жизни до верхней границы нормы взрослого (рис. 1) [35–37, 51].
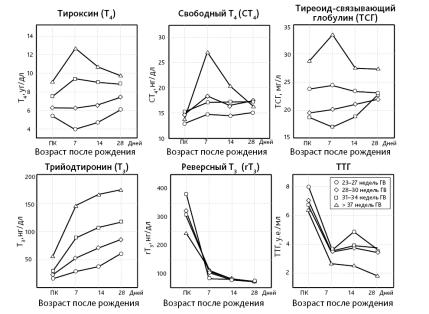
• Концентрация Т3 повышается к 7-му дню жизни и продолжает расти в первые 28 суток, что связано не только с непосредственным действием ТТГ, но и с повышенной постнатальной экспрессией активирующей D1-дейодиназы в сочетании с потерей плацентарной D3 [26, 27, 52, 53].
•Как и Т4, сывороточные концентрации свободного Т4 и ТСГ остаются повышенными в течение 7 дней постнатальной жизни, уменьшаясь в дальнейшем [26, 27, 52, 53].
•Снижается уровень rТ3 [26, 27, 52, 53].
Рис. 1. Постнатальные изменения содержания гормонов щитовидной железы в зависимости от срока гестации [48]
ПК — пуповинная кровь; ГВ — гестационный возраст
Новорожденные со ЗВУР:
•Дети со ЗВУР имеют значительно более выраженное повышение уровня ТТГ и
снижение уровней общего и свободного Т4, чем дети с нормальным весом. Причиной может быть нарушение плацентарного кровоснабжения плода, гипоксемия и ацидемия.
•Подобная реакция уменьшения Т4 и повышения ТТГ отличается от реакции на голодание у здоровых взрослых, у которых уровень ТТГ снижается. На сегодняшний день научных исследований, объясняющих этот факт, — нет [51]. В настоящее время в нашем институте проводятся исследования, посвященные изучению метаболического статуса у детей, родившихся с ЗВУР. Уже первые полученные результаты позволяют сделать вывод, что они имеют особенности, отличающие их от группы здоровых сверстников. Причем особенности метаболического статуса в данной группе сохраняются долго. Вероятно, в течение всей последующей жизни.
Недоношенные новорожденные:
•У плодов и в пуповинной крови уровень Т3 и Т4 прогрессивно увеличивается с 15-й по 42-ю неделю беременности, а ТТГ и сТ4 возрастают с 13-й недели, достигая пика на 31–34-й неделе [54].
•У недоношенных уровень ТРГ, ТТГ, Т4, сТ4, Т3 ниже, чем у доношенных. Постнатальный пик уровней ТТГ и Т4 хотя и значительный, но более плоский. Выраженность этих различий зависит от гестационного возраста (рис. 1) [35–37, 40, 46, 48, 50, 55–59].
•У недоношенных младенцев, «холодовая волна» ТТГ ниже (около 40 мЕд/л) и, соответственно, повышение Т4 менее выражено [36, 40, 46, 48, 50, 56, 59].
•Через час после родов повышение уровня ТТГ было существенно меньше у детей, рожденных до 28 недель беременности [60].
•У детей с 25–30 недель гестационного возраста свободный Т4 составляет 0,5–3,3 нг/дл (6,4–42,5 пмоль/л); в 31–36 недель свободный Т4 — 1,3–4,7 нг/дл (16,7–60,5 пмоль/л)
[36, 40, 46, 48, 50, 56, 59].
•Постнатальное повышение уровня Т4 на 7–14-й день жизни в сыворотке было недостаточно выражено у детей, рожденных на 31–34-й неделе, отсутствовало у рожденных на 28–30-й неделе. У младенцев, родившихся до 31-й недели
беременности, концентрация циркулирующего Т4 даже может снизиться в первые 1– 2 недели жизни. У детей с 25–28 недель гестационного возраста имеется снижение
концентрации Т4 в течение первой послеродовой недели до 4 мкг/дл (51,5 нмоль/л)
[36, 40, 46, 48, 50, 56, 59].
•Уровни тиреоглобулина (формы хранения T4) высоки, что отражает увеличение производства щитовидной железой плохо йодированных предшественников гормонов
[35–37, 40, 46, 48, 50, 55–59].
•Факторы, влияющие на становление тиреоидного статуса у недоношенных детей с ОНМТ: незрелость гипоталамо-гипофизарно-тиреоидной оси; сниженная способность ЩЖ концентрировать йод, синтезировать и йодировать тиреоглобулин; незрелость метаболизма тиреоидных гормонов и системы дейодирования в периферических
тканях (низкий уровень D1 в печени приводит к низкой концентрации Т3, высокой рТ3, а также высоким уровням сульфатированных производных); внезапное увеличение потребности в гормонах ЩЖ для термогенеза, функции сердца, действия скелетных мышц, а также потребностей обмена веществ; внезапное прекращение
передачи Т4 от матери плоду; воздействие неонатальных заболеваний; недостаточное поступление и отрицательный баланс йода; избыток йода (йодсодержащие антисептики и рентгеноконтрастные агенты) [35–37, 40, 46, 48, 50, 55–59].
•Обычно у недоношенных новорожденных уровень Т4 в крови остается ниже чем, у доношенных детей примерно до 4 недель жизни [50]. У новорожденных, рожденных
до 28-й недели беременности, низкие концентрации гормонов могут отмечаться до 8 недель жизни [49]. На протяжении первых пяти недель жизни уровень ТТГ повышается в ответ на низкий уровень тиреоидных гормонов, после чего на 4–14-
й неделях прогрессивно снижается [50].
•При выраженной недоношенности отрицательная обратная связь начинает адекватно функционировать только примерно на 5-й неделе жизни, что достаточно грубо эквивалентно 30-недельному сроку беременности.
•Еще одним фактором, оказывающим влияние на функционирование гипоталамо- гипофизарно-тиреоидной оси, является ограниченный функциональный резерв ЩЖ недоношенных детей, рожденных до 28 недель беременности. Так, запас йода и тиреоглобулина у таких детей составляет всего 20–30 % от такового у доношенных [50]. Прекращение поступления йода от матери в сочетании с его ограниченным потреблением после рождения способствует развитию относительной недостаточности ЩЖ.
Необходимо отметить, что ряд сопутствующих недоношенности процессов в целом
может приводить к состоянию, которое описывается у взрослых термином «синдром эутиреоидной патологии» [50]. У детей его чаще всего называют «синдром низкого Т3». Как мы указывали выше, этот синдром чаще всего встречается у детей, рожденных раньше 30 недель беременности, и примерно в два раза чаще у детей, рожденных на 23– 27-й неделе, по сравнению с рожденными на 28–30-й неделях [50].
«Синдром низкого Т3» у недоношенных характеризуется: а) снижением уровня ТТГ; б) нормальным, сниженным или высоким уровнем общего Т4; в) нормальным или повышенным свободным T4; г) низким общим и свободным Т3.
К возникновению синдрома могут приводить многочисленные заболевания или состояния, в том числе голодание, сепсис, почечная недостаточность, хирургические вмешательства, функционирующий артериальный проток, некротизирующий
энтероколит, мозговые изменения и необходимость в кислороде [61]. Выраженность синдрома эутиреоидной патологии напрямую зависит от тяжести этих заболеваний [50]. Кроме того, развитию подобных нарушений может способствовать ряд лекарственных препаратов, применяемых для лечения заболеваний: дофамин, аминофиллин, кофеин, дексаметазон и диаморфин [59, 61]. Отдельного обсуждения, по нашему мнению, требуют новорожденные, заболевшие сепсисом.
Интегративный ответ организма на инфекционный агент реализуется через единый нейроиммуноэндокринный механизм. Стимуляция патогеном (чаще эндотоксином грамотрицательных микроорганизмов) и цитокинами (ФНО, ИЛ-1, ИЛ-6 и др.) вызывает активацию каскада центрально опосредованных нейро-эндокринных ответов. В частности, происходит активация симпатико-адреналовой системы и «осей»: гипоталамус-гипофиз- надпочечники и гипоталамус-гипофиз-щитовидная железа. Лептин (пептид, секретируемый адипоцитами — важнейший регулятор энергетического обмена) также существенно повышен при септическом шоке, однако он, в отличие от названных цитокинов, ингибирует «ось»: гипоталамус-гипофиз-надпочечники. Указанные процессы повышают уровень катехоламинов и усиливают катаболическую направленность обмена веществ [62]. С другой стороны, глюкокортикоиды лимитируют распространение воспаления, то есть генерализацию процесса.
D. Annane (1998) выявлен факт сниженной чувствительности рецепторов к норадреналину при тяжелом сепсисе (при сохранении резерва адреналовой системы), ведущей к вазодилатации и снижению системного давления при септическом шоке [63]. Это послужило основанием для попытки применения в клинической практике вазопрессина с целью нормализации АД [64]. Другие исследователи отмечают случаи развития адреналовой недостаточности как причине гипотензии при сепсисе. При течении септического процесса выявлена диссоциация концентрации АКТГ, β-эндорфинов и кортизола (последние 2 гормона повышены без адекватного увеличения АКТГ). Имеются сообщения о развитии надпочечниковой недостаточности при септическом шоке у детей. Указывают также на частое сочетание низкой продукции ТТГ и СТГ.
Японские исследователи еще в 1999 году выявили супрессию ТТГ-ответа на рилизинг-гормон гипоталамуса у септических больных с полиорганной недостаточностью
ипоказали прогностическое значение этого факта. На повреждение гипоталамогипофизарно тиреоидной оси у погибших больных указывают и результаты других работ [65]. У выживших пациентов имел место высокий уровень ТТГ и высокая продукция тиреоидных гормонов, в то время как у погибших впоследствии — низкая продукция ТТГ
итиреоидных гормонов. По нашим наблюдениям, летальный исход при неонатальном сепсисе сочетается с исключительно низкими концентрациями ТТГ и Т3. Аналогичные
данные получены H. Monig et al. [66]. При этом низкая продукция данных гормонов сочеталась с повышенным содержанием ИЛ-1β, ФНОα, ИЛ-6, «растворимого ИЛ-2
рецептора (sIL2-R)». Предполагается центральная супрессия продукции ТТГ и,
соответственно, низкая продукция тиреоидных гормонов у больных, переносящих сепсис. Установлено [67], что «синдром низкого Т3» (без повышенной продукции тропного гормона) сочетается с тяжелым течением неонатального сепсиса. Нередко у больных отмечается также низкий уровень Т4, то есть имеет место «гипотиреоидизм
септического генеза».
Установлен факт резистентности организма септического больного к экзогенным и эндогенным факторам роста. Ее связывают с двумя обстоятельствами:
1)Снижением под влиянием цитокинов экспрессии рецепторов для СТГ на клетках печени и снижением вследствие этого продукции инсулиноподобного фактора роста — ИФР1, что, в свою очередь, не позволяет реализовать анаболический эффект и вносит свой вклад в истощение и развитие метаболических расстройств при сепсисе.
2)Имеются сообщения о наличии общего сигнального пути у СТГ и ИЛ-1β на клетках печени, что препятствует реализации анаболических эффектов СТГ. Концентрация СТГ часто очень высока [68]. Однако, по нашим данным, повышенное содержание СТГ в начальной стадии сепсиса и быстрое прогрессивное его снижение в динамике является благоприятным признаком.
A. D. Sam et al. (1999) сообщили о депрессии продукции тестостерона и повышении концентрации эстрадиола у больных, заболевших сепсисом [69]. Возможно, защитный эффект андростендиона и дегидроэпиандростерона (в экспериментальной летальной бактериальной инфекции и эндотоксиновом шоке) связан с восполнением их дефицита при сепсисе.
Таким образом, анализ работ свидетельствует о том, что на разных стадиях септического процесса имеется различный гормональный статус. При этом, если в начале процесса имеет место адаптивная стимуляция желез внутренней секреции, то в дальнейшем развитие их дисфунции, что требует учета при проведении терапии.
Последние 15–20 лет внимание исследователей было привлечено к новому маркеру системного воспалительного ответа, предшественнику кальцитонина — прокальцитонину. Было показано, что он синтезируется мононуклеарами крови, а также клетками АПУДсистемы и его синтез модулируется липополисахаридами клеточной стенки грамотрицательных бактерий. Прокальцитонин является вторичным медиатором, лишь усиливающим системный воспалительный ответ синдром (SIRS). Большинство специалистов расценивают его не только как ранний диагностический признак SIRS при сепсисе (более значимый, чем С-реактивный белок), но и как показатель тяжести септического процесса и прогностический признак. Некоторые исследователи указывают на возможность с помощью определения концентрации прокальцитонина дифференцировать SIRS инфекционной и неинфекционной этиологии (например, посттравматический). В связи с многочисленными результатами, касающимися прокальцитонина, интерес в свете тематики монографии представляют данные L. Lind et al., полученные в 2000 году [70]. Они выявили гипокальцемию у септических больных, сочетающуюся с повышенной концентрацией паратиреоидного гормона. При этом она не была связана с повышенной экскрецией или низкой резорбцией кальция! Авторы заключили, что низкая концентрация кальция в крови при сепсисе отражает тяжесть системного воспалительного ответа.
Современный этап трактовки патогенеза гнойно-септического процесса требует учета достижений иммунологии, механизмов реализации системного ответа организма на инфекционный агент, включающего весь спектр медиаторов, как нейро-эндокринного уровня регуляции целого, так и медиаторов межклеточного взаимодействия (цитокинов, селектинов, интегринов). Цитокины, обладая полифункциональностью обеспечивают все этапы воспалительного, гемостатического и иммунологического процессов вплоть до выздоровления.
Однако патогенез системного воспалительного ответа не сводится к гиперцитокинемии. Как мы отмечали выше, интегративный ответ организма реализуется через единый нейроиммуноэндокринный механизм. Особенностям гормонального профиля у септических больных посвящено достаточно большое количество исследований. Однако в просмотренной нами литературе мы не встретили результатов исследований, посвященных выделению лабораторных вариантов сепсиса, в том числе и вариантов гормонального статуса, поэтому мы и сочли необходимым остановиться на этом вопросе несколько более подробно, приведя собственные данные. Спектр изучаемых нами гормонов определялся не только их физиологическим значением, но исследованиями других авторов.
У всех септических больных выявлены гормональные дисфункции (рис. 2), однако характер их был различен (рис. 3).