Материал: Сыровая А.О. и др Аминокислоты глазами химиков, фармацевтов, биологов. Т. 2
|
CH3 |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
C |
|
|
H |
CH |
|
COOH |
||||||
|
|
|
|
|
N |
|
(CH2)4 |
|
|
||||||
|
|
|
|
|
|
|
|
||||||||
N |
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
O |
|
|
|
|
|
NH2 |
|
|||||
|
|
|
|
|
|
|
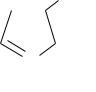
Пирролизин |
|
|
|
|
||||
Селеноцистеин представляет собой аналог цистеина, в котором тиоловая группа замещена на селеноловую. Селеноцистеин включается в состав селенобелков практически всех живых организмов. Он обнаружен в составе многих ферментов, например, глутатионпероксидаз, тиоредоксинредуктаз [9]. В
организме человека встречается 25 белков, содержащих селеноцистеин [10].
Формилметионин – это производное метионина, в котором водород аминогруппы замещен на формильную группу. Формилметионин играет важную роль в синтезе белков бактерий, а также митохондрий и хлоропластов и не встречается в составе цитозольных белков эукариот. В организме человека формилметионин распознается иммунной системой, как чужеродный материал и инициирует реакцию борьбы организма с потенциальной инфекцией [8].
Пирролизин сходен по структуре с лизином, однако имеет карбоксилированное пирролиновое кольцо, присоединенное к ε-аминогруппе боковой цепи лизина. Пирролизин – природная, генетически кодируемая специфическим кодоном (UAG, обычно стоп-кодон) аминокислота, которая непосредственно в процессе трансляции, как стандартная аминокислота,
включается в состав белков некоторых метан-продуцирующих одноклеточных организмов (археи) [11].
D-аминокислоты
В природе встречаются главным образом α-аминокислоты [12]. Основная структурная особенность этих соединений (α-аминокислот) – это наличие
226
асимметрического центра – атома углерода, при котором находятся аминная и карбоксильная функциональные группы. Это означает, что все
α-аминокислоты, за исключением глицина, могут существовать в виде пары конфигурационных (оптических) изомеров – L- и D-. Экспериментально найдено,
что из пар антиподов молекул α-аминокислот в жизнедеятельности организмов практически всегда и везде фигурируют только L-изомеры. Это значит, что организмы синтезируют только L-α-аминокислоты и потребляют тоже только L-α-
аминокислоты, т.е. реакции биосинтеза α-аминокислот и последующего их метаболизма in vivo строго стереоспецифические процессы [13]. Соответственно,
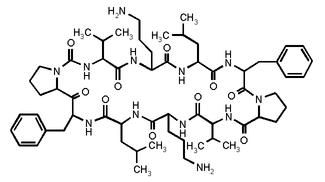
аминокислоты, входящие в состав белка, относятся к L-ряду; D-аминокислоты встречаются в природе сравнительно редко, в частности, в составе пептидных антибиотиков бактериального происхождения. Так, например, D-фенилаланин входит в состав грамицидина С – антибиотика, выделяемого бактерией Bacillus brevis, живущей в почве. Молекула грамицидина С представляет собой циклический декапептид, содержащий два остатка D-фенилаланина [14].
Грамицидин С имеет следующую структуру:
Грамицидин С
Грамицидин А содержит D-валин, D-лейцин, D-триптофан; актиномицин D
содержит D-изолейцин; полимиксин – D-серин; D-пролин встречается в эргоалкалоидах [15]. Например, D-пролин является составной частью алкалоидов спорыньи (из рожков спорыньи выделено 12 алкалоидов, представляющих собой
227
различные сочетания лизергиновой или изолизергиновой кислот с аминокислотами, пировиноградной кислотой или аминоспиртами). Алкалоиды спорыньи обладают высокой фармакологической активностью.
D-глютаминовая и D-аспарагиновая кислоты, D-аланин и D-фенилаланин обнаружены в бациллах сибирской язвы, картофельной палочке (Bacillus mesentericus) и в других микроорганизмах [5]. D-аланин входит в состав тейхоевых кислот – биополимеров, содержащихся в грамположительных бактериях (Lactobacillus), D-глютаминовая кислота входит в состав пептидогликанов клеточной стенки грамположительных и грамотрицательных бактерий [16].
D-серин в большом количестве содержится в головном мозге млекопитающих и может действовать в качестве нейротрансмиттера, а также служить в качестве медиатора важных физиологических и патологических процессов [17].
D-аминокислоты в достаточно большом количестве встречаются в пептидогликанах клеточных стенок бактерий [18].
L-аминокислоты включаются в состав белков обычным путем, согласно генетической информации, во время трансляции на рибосомах, тогда как,
D-аминокислоты, найденные в белках, образуются в процессе ферментативной посттрансляционной модификации после трансляции и транслокации в эндоплазматический ретикулум. Например, D-валин и D-γ-гидроксивалин обнаружены в составе пептидов яда некоторых видов морского организма – конусной улитки (род Conus) [19].
В 1980 г. из кожи южноамериканской лягушки рода Phyllomedusa был выделен и затем охарактеризован пептид с сильной и продолжительной морфиноподобной активностью – дерморфин. Он представляет собой гептапептид. Отличительной особенностью молекулы дерморфина является наличие в положении 2 остатка D-аланина, с которым связывают высокую
228
биологическую активность пептида. Экспериментальная замена остатка
D-аланина на остаток другой аминокислоты приводит практически к полной потере опиоидной активности [20].
D-аминокислоты используются в рацемической кристаллографии для создания центросимметричных кристаллов, которые (в зависимости от белка),
могут обеспечить более простое и надежное определение структуры белка [21].
α-Аминокислоты, не входящие в состав белков Как уже было упомянуто, в природе встречаются главным образом
α-аминокислоты, в то же время, β- и γ-аминокислоты представлены в природе единичными случаями [12,13]. Здесь можно отметить нейромедиатор ЦНС млекопитающих γ-аминомасляную кислоту (ГАМК) и β-аланин, являющийся фрагментом пантотеновой кислоты – составной части кофермента А. Интересным представителем природных γ-аминокислот является карнитин (бетаин 3-гидрокси- 4-триметиламиномасляной кислоты), определяемый еще иногда как витамин ВBt.
Карнитин в значительных количествах присутствует в мышцах животных, в
бактериях и растениях, является фактором роста некоторых насекомых [13].
В растениях и микроорганизмах часто встречаются α-аминокислоты, не принимающие участия в образовании белков. Они образуются во время повышенной потребности в азоте, например при образовании почек или прорастании семян, или же запасаются в виде растворимых веществ. Многие аминокислоты, образовавшиеся при обмене веществ низших организмов, имеют свойства антибиотиков. Они действуют как аминокислоты антагонисты, т. е.,
являются конкурентными ингибиторами при обмене веществ, задерживая определенные ступени биосинтеза аминокислот или способствуя образованию ложных последовательностей при биосинтезе белков [12].
Непротеиногенные аминокислоты чрезвычайно разнообразны по строению и, следовательно, имеют различные химические и биологические свойства. Среди
229
непротеиногенных аминокислот встречаются соединения, имеющие в радикале малые циклы, причем, весьма напряженные, гетероциклы, необычные гетероатомы (например, йод) [13].
Производные аланина Между непротеиногенными и протеиногенными аминокислотами иногда
существует близкое структурное родство. Так, аланину соответствуют свыше 30
производных, различающихся заместителями водородного атома метильной группы. Заместителем может быть аминогруппа, как, например, у α,β-диаминопропионовой кислоты.
CH2 CH COOH
NH2 NH2
α,β-Диаминопропионовая кислота
Эта аминокислота встречается в растениях семейства мимозовых [12]. В
качестве заместителя может присутствовать циклопропановое кольцо, как у найденной в различных фруктах аминокислоты гипоглицина А
(β-(метиленциклопропил)аланин) и 1-аминоциклопропанкарбоновой кислоты:
H2C |
|
|
CH2 |
|
|
CH |
|
COOH |
|
|
|
|
|
||||
|
|
|||||||
|
|
|
|
|
|
|
||
|
|
CH2 |
|
NH2 |
||||
Гипоглицин А
CH2  CH2
CH2
C COOH
NH2
1-Аминоциклопропанкарбоновая кислота
230