Материал: Сыровая А.О. и др Аминокислоты глазами химиков, фармацевтов, биологов. Т. 2
электромиграция нейтральных аминокислот через ионообменные мембраны //
Журн. прикл. химии. – 1974. – Т. 47. – № 6. – С. 1258–1261.
20.Кулинцов П. И., Бобрешова О. В., Аристов И. В. и др. Механизмы электротранспорта в системах ионообменная мембрана-раствор аминокислоты // Электрохимия. – 2000. – Т. 36, № 3.– С. 365–368.
21.Шапошник В. А., Селеменев В. Ф., Терентьева Н. П.. Барьерный эффект при электромиграции пролина и валина через ионообменные мембраны при электродиализе // Журн. прикл. химии. – 1988. – Т. 61, № 5. – С. 1185–1187.
22.Bobreshova O., Novikova L., Kulintsov P., Balavadze E. Amino acids and water electrotransport through cation-exchange membranes // Desalination. – 2002. – V. 149. – P. 363–
368.
23. Martinez D., Saundeax R., Saundeax J., Gavach C. Electrotransport of alanine
through ion-exchange memebranes // J. Membr. Sci. – 1992. – V.69. – P. 273–281.
24.Пащенко Л. П., Любарь А. В., Булгакова Н. Н., Бобрешова О. В., Аристов Ю. В., Кулинцов П. И. Повышение биологической ценности изделий из муки тритикале // Известия вузов. Пищевая технология. – 2002. – № 2-3. С. 26–28.
25.Pashenko L. P, Zharkova I. M., Korenman Ya. L, Koshelev L. A. Application of an Ecologically Clean Preparation of Lysine in Baking Technology // Ecological Congress International Journal. – 2002. – № 2, V.5. – P. 35–37.
26.Пат. 2200410 Россия, С1 7А 21 D 8/02, 13/04. Способ приготовления хлеба / Пащенко Л. П., Любарь А. В., Родионова Н. С., Булгакова Н. Н., Бобрешова О. В., Аристов И. В. Заявл. 03. 08. 2001, № 20011216913. Опубл. 20.
03.2003. Бюл. № 8.
27.Lindenmeier M., Fast V. And Hofmann T. Structural and Functional Characterization of Pronil-lysine, a Novel Protein Modification in Bread Crust Melanoidms Showing in Vitro Antioxidative and Phase I/II Enzyme Modulating Activity // J. Agric. Food Chem. – 2002. – V.50. – P.6997–7006.
186

ГЛАВА 15
ГИСТИДИН
СЫРОВАЯ АННА ОЛЕГОВНА Заведующая кафедры медицинской и биоорганической химии ХНМУ,
д.фарм.н., профессор
187
СПИСОК СОКРАЩЕНИЙ
АТФ – аденозинтрифосфат
СТГ – соматотропный гормон
Ig – иммуноглобулин
188
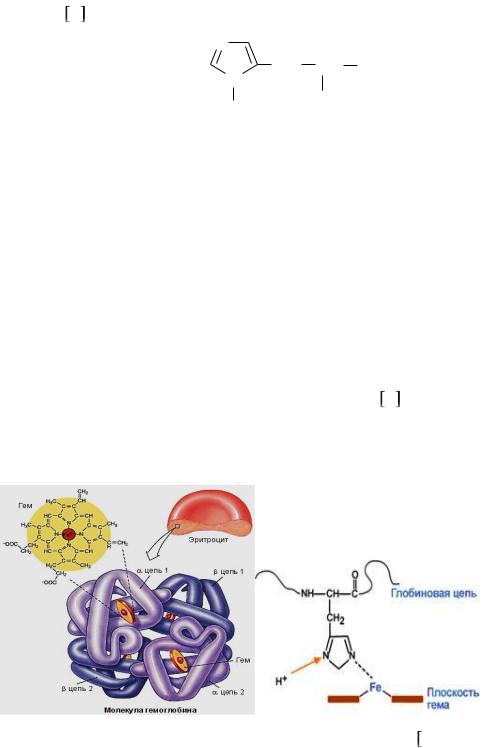
Незаменимая гетероциклическая аминокислота гистидин –
(L-β-имидазолилаланин или L-α-амино-β-(4-амидазол)-пропионовая кислота) (рис. 1), которая была в 1896 году выделена одновременно двумя учѐными: Kossel
из сернокислых гидролизатов протамина спермы осетра и Hedin – из белковых гидролизатов 1 .
N
CH2 CH COOH
N
H NH2
Рис 1 Строение гистидина Гистидин представляет собой прозрачные, бесцветные или белые
кристаллы, растворимые в воде, малорастворимые в спирте, нерастворимы в эфире. L-гистидин – аминокислота, которая по мнению Snyderman и соавторов
(1961 г.) является незаменимой аминокислотой для детей, а по мнению Kopple, Swendseid (1974 г.) – и для взрослых. Дневная потребность в гистидине составляет 1,5 – 2,0 гр. Отсутствие гистидина замедляет синтез гемоглобина и приводит к развитию анемий в связи с тем, что белковая часть гемоглобина требует достаточно большого количества гистидина 1 . Это объясняется тем, что гем связан с глобиновым компонентом через гистидиновые остатки в полипептидных цепях молекулы гемоглобина (рис. 2).
Рис. 2 Строение гемоглобина 2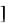
189

Гистидин может образовываться при распаде гемоглобина. В организме вызывает значительное увеличение секреции соматотропного гормона (СТГ).
Гистидин входит в состав многих белков в виде L-конфигураций. Он принимает активное участие в синтезе карнозина (азотистого экстрактивного вещества мышц), улучшает азотистый баланс, функцию печени, повышает желудочную секрецию и моторику кишечника, иммунитет, нормализует сердечный ритм.
Хлороводородная соль гистидина в медицинской практике применяется при язвенной болезни желудка и двенадцатиперстной кишки, гастритах, гепатитах,
атеросклерозе, сниженном иммунитете 3 . Имеются данные о благоприятном влиянии гистидина на липопротеиновый обмен у больных атеросклерозом 4 .
Гистидин в комбинации с аденозинтрифосфатом (АТФ), калием и магнием входит в комплексный препарат АТФ-ЛОНГ, который применяют как антиаритмическое и антиишемическое средство. Установлена в эксперименте его способность повышать работоспособность животных 3 .
В процессе катоболизма гистидин дезамининируется под действием гистидазы (гистидин-амиаклиазы) образуется уроканиновая кислота, которая через ряд реакций превращается в глутамат. Также образуется одноуглеродный фрагмент, соединѐнный с тетрагидрофолиевой кислотой, который может быть использован в реакциях синтеза. Известно наследственное заболевание гистидинемия, которая возникает в результате отсутствия гистидазы. Для этого заболевания характерно повышенное содержание гистидина в крови и в моче,
нарушение умственного развития 1 .
Гистидин – протеиногенная кислота, которая при некоторых патологических состояниях путѐм декарбоксилирования L-гистидина превращается в значительное количество гистамина (рис. 3). Это декарбоксилирование катализируется в тканях млекопитающих ферментом гистидиндекарбоксилазой. В качестве кофактора выступает пиридоксальфосфат.
190