Материал: спектр и фотометр
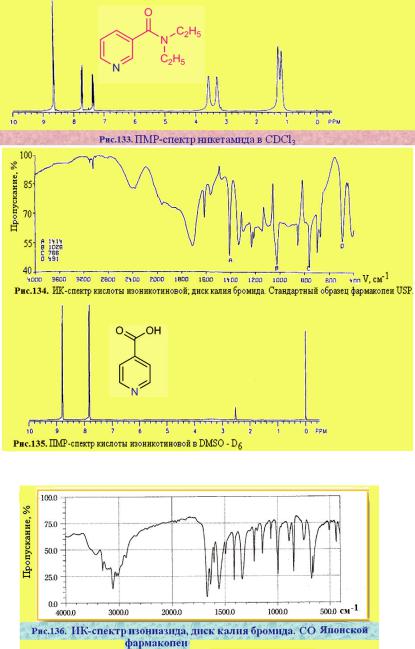
Изониазид
146
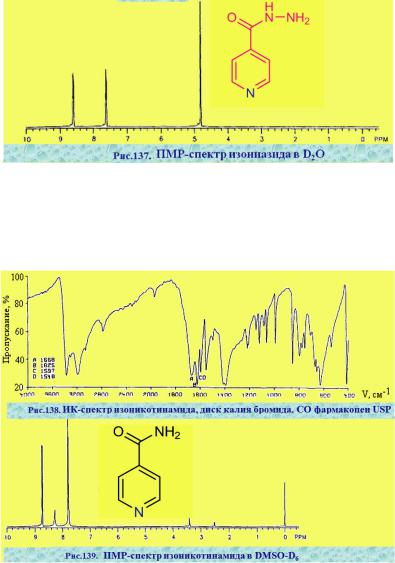
УФ-спектр: в 0,1 М растворе HCl: λмакс = 266 нм, λмин = 234 нм в области 220-350 нм.
Применение. Противотуберкулезное средство.
Изоникотинамид
УФ-спектр изоникотинамида: в 0,1 М растворе HCl: λмакс = 266 нм, λмин = 234 нм в области 220-350 нм. Получение фтивазида с т. пл. 227оС
Посторонние примеси в изоникотинамде: Свободный гидразин
(не более 0,02%). ТСХ: («Силуфол УФ-254», ацетон-вода (80:2), сравнение с индивидуальным гидратом гидразина).
147
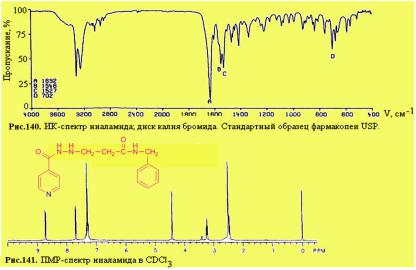
Применение. Противотуберкулезное средство. Внутрь по 0,3 г 3 раза в день.
Ниаламид
УФ-спектр ниаламида: в 0,1 М растворе HCl в области 220-350 нм: λмакс = 267 нм, λмин = 236 нм.
Применение. Антидепрессант. В психиатрической практике при депрессивных состояниях различных форм. Таблетки (драже) по 0,025г.
Этионамид и протионамид
Подлинность Т.пл.: этионамид – 158-164оС, протионамид – 140-143оС.
ИК-спектры:сравнение со спектроми сравнения или со спектрами СО.
УФ-спектры: растворы в этаноле (10 мкг/мл) в области 230-360 нм: λмакс = 290 нм (этионамид), λмакс = 291 нм (протионамид).
Аоколо0,42(этионамид,290нм),около0,78(протионамид,290нм). раствор в 0,1 М HCl: λмакс1 = 230 нм, λмакс2 = 278 нм (этионамид).
Количественное определение этионамида. УФ-спектрофотометрия (Фармакопея США):
λ = 290 нм, растворитель – метанол, сравнение со стандартным образцом.
Применение. Противотуберкулезные средства. Менее активны, чем изониазид и стрептомицин, но действуют на устойчивые к ним микобактерии. Лечение различных форм туберкулеза внутрь в виде таблеток и драже по 0,25
г.
148
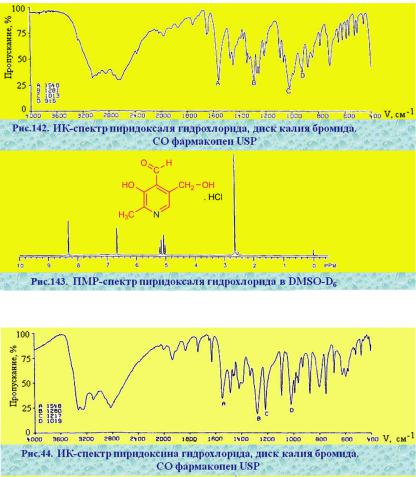
Производные пиридинметанола и оксипиридина Пиридоксаль гидрохлорид. Испытания подлинности подтверждают
данными ИК- и ПМР-спектров (см. рис. 142 и 143).
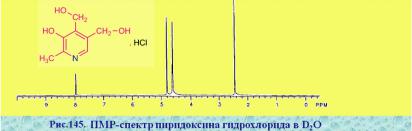
Пиридоксина гидрохлорида (см. рис. 144 и 145).
УФ-спектры: максимумы поглощения в фосфатном буферном растворе (рН =7) в области 280-450 нм:
пиридоксина гидрохлорид – 254 и 324 нм, пиридоксальфосфат – 330 и 388 нм.
0,002%-ный раствор пармидина в HCl: λмакс = 268 нм.
раствор эмоксипина в боратном буфере (рН= 8) в области 220-350 нм: λмакс1 = 250 нм, λмакс2 = 325 нм, λмин1 = 230 нм, λмин2 = 270 нм.
149
Посторонние примеси. ТСХ: «Силуфол УФ-254 нм»,
хлороформ-метанол (15:5) (пармидин), бензол-этанол-раствор аммиака (45:13:1) (эмоксипин), детекция в УФ-свете (254 нм).
Применение. Пиридоксина гидрохлорид – витамин В6. Применяют при токсикозах у беременных, паркинсонизме, хореи, пеллагре, острых и хронических гепатитах, кожных и других заболеваниях.Внутрь, подкожно, внутримышечно и внутривенно по 0,02-0,05-0,1 г в сутки. Пиридоксальфосфат – кофермент витамина В6. Таблетки 0,01 и 0,02 г.
Эмоксипин: внутриглазные и посттравматические кровоизлияния, диабетическая ретинопатия, тромбозы сосудов сетчатки. 1% раствор внутривенно и внутримышечно, субконъюнктивально, ретробульбарно и парабульбарно. Пармидин: комплексная терапия атеросклероза. Мексидол: Последствия острых нарушений мозгового кровообращения, в том числе после транзиторных ишемических атак, в фазе субкомпенсации в качестве профилактических курсов.
Производные 1,4-дигидропиридина
В таблице 3 представлены некоторые производные 1,4-дигидропири- дина, широко применяемые в медицинской практике в качестве антиангинального средства.
Подавляющее большинство 1,4-дигидропиридинов получают с использованием классической реакции Ганча, разработанной для синтеза пиридина и его различных вариантов. Первый 1,4-дигидропиридин был синтезирован в 1882 году в качестве стабильного промежуточного соединения. В своей простейшей форме, синтез включает нагревание ароматического альдегида, например, ортонитробензальдегида (1) с этилацетоацетатом
(2) и аммиаком. Данная реакция определенно включает в себя, в качестве первого этапа, альдольной конденсации с образованием бензилиденового производного (3). Далее к конъюгату добавляют второго моля эфира ацетоуксусной кислоты, которая приводит к образованию 1,5-дикетона (4), а взаимодействие карбонильной группы с аммиаком обеспечивает образова-
150