Материал: Шкарин В.В., Шафеев М.Ш. Дезинфектология.Руководство для студентов медицинских вузов и врачей
Licheniformis, B-6. Бактериальный тест представляет собой инсулиновый флакон с определенным количеством спор, вложенный в пакетик из упако вочной бумаги. Тест может храниться в холодильнике при температуре +4°С в течение 2 лет без значительного снижения числа спор и их термоустойчи вости.
Для контроля стерилизатора пакеты с бактериальными тестами нуме руют и размещают в тех же контрольных точках, что и химические тесты и максимальные термометры (см. табл. 24, 25). Споры в паровом стерилиза торе погибают через 15 мин при 120°С, в воздушном стерилизаторе через 30 мин при 160°С. Эти показатели гибели спор соответствуют требованиям международных стандартов. По окончании стерилизации пакеты с тестами вынимают из стерилизатора и в тот же день доставляют в бактериологичес кую лабораторию с сопроводительными документами.
Влаборатории, в асептических условиях, в каждый флакон вносят 2,0 мл питательной среды и закрывают стерильными резиновыми пробка ми. Далее тесты из паровых стерилизаторов инкубируют при температуре 55°С, из воздушных стерилизаторов — при температуре 37°С в течение 7 сут с ежедневным просмотром результатов. В качестве контроля обяза тельно используют тест, который не подвергается действию стерилизующе го агента. Как правило, рост тест-культуры отмечается уже на 1—2-е сутки.
Основанием для оценки эффективности работы стерилизатора служит гибель спор в тесте после стерилизации, т.е. отсутствие помутнения пита тельной среды. В случае помутнения готовят мазок с окрашиванием по Граму и производят высев на питательный агар для сопоставления выделен ной культуры с контрольной. Рост на агаре любой другой культуры и нали чие в мазке кокков, серраций и т.д. относят на загрязнение при посеве. При наличии роста тест-культуры и обнаружении ее в мазке ищут причины не удовлетворительной работы стерилизатора и осуществляют повторный его контроль.
Впроцессе контроля возможны варианты, когда результаты химичес кого и бактериологического тестов не совпадают.
1.Химические тесты расплавились, максимальная температура на тер мометрах соответствует режиму, а бактериальный тест положительный. Это говорит о том, что температура стерилизации была достигнута, но на ко роткое время, недостаточное для гибели тест-культуры, то есть материалы
иинструменты остались нестерильными.
2.Бактериальный тест отрицательный (тест-культура погибла), а хи мический тест не изменил своего агрегатного состояния. Это свидетельству ет о том, что температура в стерилизаторе чуть ниже температуры плавле ния химического теста, т.е. ниже допустимой для данного режима, но дос таточно высока и продолжительна для гибели тест-культуры. Инструмен ты и материалы в данном случае тоже считаются нестерильными.
Оперативные (физические и химические) и бактериологический мето ды контроля взаимно дополняют друг друга, и поэтому показателями каче ственной работы стерилизующей аппаратуры являются:
<^ 93
•отсутствие роста микроорганизмов при посеве всех биотестов на пи тательной среде;
•изменение исходного состояния (цвет, агрегатное состояние) хими ческих индикаторов;
•отклонение температуры в различных точках камеры стерилизатора от номинального значения.
Технический контроль и ремонт стерилизационной аппаратуры прово дит объединение «Медтехника» по договору с лечебным учреждением или специалист с техническим образованием, который назначается приказом руководителя учреждения.
Контроль стерильности изделий медицинского назначения
В целях профилактики внутрибольничных инфекций в ЛПУ осуще ствляется постоянный контроль за стерилизацией медицинских изделий и соблюдением асептических условий их использования (табл. 28). Бактери ологические лаборатории санитарно-эпидемиологических станций и ЛПУ проводят контроль стерильности только тех ИМН, которые стерилизуют ся в самом ЛПУ. Бактериологический контроль осуществляется санитар но-эпидемиологической станцией не реже 2 раз в год, лабораторий ЛПУ — не реже 1 раза в месяц. Забор проб на стерильность производит специально выделенный лаборант санитарно-эпидемиологической станции или меди цинская сестра под руководством сотрудника бактериологической лабора тории со строжайшим соблюдением правил асептики.
Объектами бактериологического контроля являются хирургические инструменты, шприцы, иглы, системы переливания крови многоразового использования, зонды, катетеры, резиновые перчатки и другие изделия из резины и пластикатов, хирургический шовный материал, различная аппа ратура (аппараты экстракорпорального кровообращения и другие), пере вязочные материалы, операционное белье.
В ЛПУ, имеющих ЦСО, контролю на стерильность подлежит не менее 1% от числа одновременно простерилизованных изделий одного вида. В учреждениях, не имеющих ЦСО и осуществляющих стерилизацию в отде лениях и кабинетах, контролю подлежат не менее 2 предметов одного вида медицинского инструментария и не менее 2 предметов одного наименова ния изделий из текстиля, одновременно простерилизованных. При центра лизации процессов стерилизации все изделия, подлежащие контролю, на правляют в бактериологическую лабораторию в упаковке, в которой осу ществлялась их стерилизация (пакеты, биксы, мягкие упаковки). Перед доставкой в лабораторию упаковки дополнительно завертывают в стериль ную простыню или мешок. При децентрализованной стерилизации забор проб проводят в стерильные емкости с соблюдением строжайших правил асептики непосредственно перед началом работы.
|
|
|
Т а б л и ц а 2 8 |
Контроль за стерилизацией ИМН и соблюдением асептических условий |
|||
|
|
Виды контроля |
|
|
Самоконтроль, |
Метрологический |
Госнадзор, |
Направление |
осуществляемый |
и технический |
осуществляемый |
контроля |
персоналом |
контроль, |
санэпидстанциями |
|
учреждения |
осуществляемый |
и дезстанциями |
|
|
ПО «Медтехника» |
|
Контроль за подготов кой объекта к стерили зации
Предстерилизационная Ежедневно очистка
Комплексность наборов Постоянно с учетом асептических условий применения
Нормы и правила за грузки стерилизационПостоянно ных коробок и стерили заторов
При каждом об следовании не ре же 1 раза в квар тал с использова нием регламенти рованных проб
Работа аппаратов и обо рудования для предстерилизационной очистки и дезинфекции
Контроль условий сте рилизации, обеспечи ваемый персоналом объекта надзора (рабо та, режим, упаковка, загрузка и т.д.)
Стерильность медицин ских изделий
Воздушная среда в цен трализованной стерилизационной
|
За техсостоянием |
При плановых об |
Постоянно |
в соответствии с |
следованиях и по |
|
договорами, после |
показанию |
|
монтажа и ремон |
|
|
та |
|
|
|
Бактериологиче |
|
|
ский, не реже |
|
|
2 раз в год |
Ежедневно - за |
За техсостоянием |
Отбор проб воз |
проветриванием, |
вентиляционных |
духа 4 раза в год с |
работой вентиля |
систем, бактери |
использованием |
ционных систем, |
цидных ламп и |
аппарата Кротова |
кондиционеров, |
т.д. |
|
бактерицидных |
|
|
ламп; отбор проб |
|
|
воздуха i раз в |
|
|
месяц |
|
|
Правильность использо |
Ежедневно визу |
При каждом об |
вания стерильного мате |
ально |
следовании с при |
риала |
|
менением визу |
|
|
ального контроля |
f^** 95 <"^»'
Посев исследуемых изделий желательно проводить в настольных бок сах с ламинарным потоком стерильного воздуха; при отсутствии таких бок сов — в боксированных помещениях (бокс с предбоксником). Для обеспе чения асептических условий производят соответствующую подготовку: поверхности помещения обеззараживают 3—6% растворами перекиси во дорода, облучают ультрафиолетовыми лучами с использованием бактери цидных ламп; в работе используют стерильный инструмент, посуду и спец одежду. Перед предбоксником снимают наружную мягкую упаковку с ис следуемых предметов, в предбокснике пакеты и стерилизационные короб ки протирают 6% раствором перекиси водорода и оставляют на 30 мин на стерильном лотке, после чего вносят в бокс; при поступлении изделий в мягкой двухслойной упаковке наружную снимают в предбокснике, во внут ренней — сразу переносят в бокс.
Контроль стерильности изделий проводят путем погружения в пита тельные среды целого изделия или его части; в исключительных случаях, когда контролю подвергают изделия больших размеров, пробы забирают путем смыва стерильной салфеткой, предварительно увлажненной стериль ным физиологическим раствором, стерильной водопроводной водой или раствором соответствующего нейтрализатора. Посев с предметов одного наименования, их частей или смывов с одного предмета проводят одновре менно на две питательные среды: тиогликолевую и бульон Сабуро. Первую используют для выявления бактерий — как аэробных, так и анаэробных, вторую — для выявления грибов.
Посевы в тиогликолевую среду культивируют в термостате при темпе ратуре 32±ГС, в бульоне Сабуро при 22±ГС. После стерилизации паро вым или воздушным способом посевы термостатируют в течение 7 сут, пос ле стерилизации радиационным, газовым способами и растворами — 14 сут. При отсутствии роста микроорганизмов во всех посевах с изделий из одной загрузки паровых, воздушных или газовых стерилизаторов, одной партии изделий, стерилизованных радиационным способом, или из одной группы изделий, подвергавшихся одномоментно стерилизации растворами в одной емкости, изделия считают стерильными. В случае прорастания посевов (по мутнение питательной среды, образование осадка) готовят мазки для мик роскопического подтверждения роста микробов. Следует иметь в виду, что рост вегетативной микрофлоры в единичных пробирках может иметь мес то в результате загрязнения их в процессе посева, исключение составляют стрептококки в посевах с изделий, простерилизованных радиационным спо собом. Однако данные разных исследований свидетельствуют, что вторич ное инфицирование стерильных изделий происходит после стерилизации на различных этапах: сушки, выгрузки из стерилизаторов, транспортиров ки и хранения. Поэтому материал подлежит повторному исследованию. Зак лючение о стерильности образцов, простерилизованных газовым способом, делают через 14 сут, простерилизованных паровым и воздушным способа ми — после 8 сут.
96
Централизованное стерилизационное отделение
Задачи и функции ЦСО
Основными задачами ЦСО являются обеспечение ЛПУ полноценно обработанными медицинскими стерильными инструментами, материала ми, внедрение в практику современных методов предстерилизационной очистки и стерилизации медицинских инструментов и материалов.
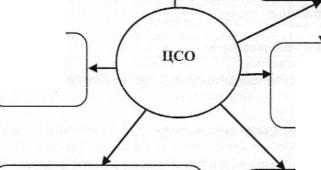
Стерилизационное отделение осуществляет (рис. 7 ) : а) прием использованных инструментов;
б) разборку, сортировку, очистку инструментов и ИМН; в) упаковку и стерилизацию инструментов, материала, ИМН;
г) выдачу стерильного инструментария, материала, а также изделий одноразового применения;
д) самоконтроль за качеством предстерилизационной очистки и эффек тивностью работы стерилизационной аппаратуры;
е) ведение документации.
Прием
использованных
ИМН
J
Разборка, сортировка, очистка ИМН
Ведение |
|
докумен |
Упаковка, |
тации |
стерилизация |
|
ИМН |
Самоконтроль за качеством |
Выдача |
|
предстерилизационной очистки и |
||
стерильных ИМН |
||
эффективностью работы |
||
подразделениям ЛПУ |
||
стерилизационной аппаратуры |
||
|
Рис. 7. Функции централизованного стерилизационного отделения Л П У
7 Заказ № 1558