Материал: сера и селен дом
Глютатион также является ингибитором свободнорадикальных процессов, защищая, например, организм от ионизирующего излучения. Он поддерживает в активном состоянии такие поступающие с пищей антиоксиданты, как аскорбиновая кислота и витамин Е (токоферол). Нуклеофильный характер атома серы в сульфгидрильной группе глютатиона используется живой природой для нейтрализации ксенобиотиков с алкилирующей способностью, например:
![]()
Из образующегося при этом сульфида глютатион не регенерируется. С С-конца от него гидролазами отщепляется глютаминовая кислота и с N‑конца глицин, а замещенный по атому серы цистеин выводится из организма в виде растворимой в воде соли соответствующего производного меркаптуровой кислоты после ацетилирования аминогруппы, например, для S-бензильного производного:
![]()
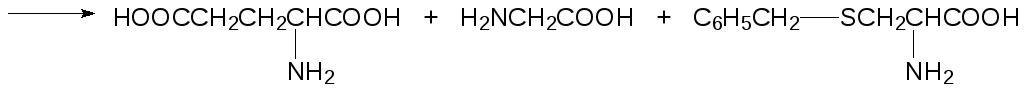
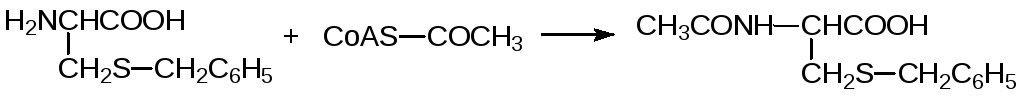
Уникальные функциональные и регуляторные свойства глютатиона позволяют использовать его для лечения онкологических, сердечнососудистых и нейродегенеративных заболеваний. Так, например, развитие злокачественных опухолей может быть заторможено комплексным препаратом Реканкостат, в состав которого входят цистеин, глютатион и антоциановые красители из таких ягод, как черника, черноплодная рябина и смородина.
Важную роль в реализации сигнальных функций монооксида азота играют S-нитрозотиольные соединения, главным из которых является S‑нитрозоглютатион (GSNO). Эти эндогенные соединения, образующиеся из легко окисляющегося и слишком лабильного NO и тиолов, служат достаточно стабильным и быстро мобилизуемым источником монооксида азота, кроме того, они участвуют в детоксикации пероксидных соединений, а S‑нитрозоглютатион ингибирует агрегацию тромбоцитов.
Тиоэфирные группы в составе белков и аминокислот могут окисляться с образованием сульфоксидных групп предназначенными для биотрансформации ксенобиотиков неизбирательными монооксигеназами. Восстановление окисленных тиоэфиров соответствующими S- и R‑сульфоксидредуктазами (восстановление S- и R‑изомеров) возможно в том случае, когда сульфоксидная функциональная группа достаточно свободна для включения её в активный центр фермента. В белках метионин участвует в образовании внутренней гидрофобной сферы и поэтому восстановление его окисленной формы становится невозможным. Это отражается в том, что старение организма человека сопровождается увеличением содержания окисленного метионина в составе его белков.
Активное участие в образовании холина — соли триметил-2- гидроксиэтиламмония — принимает образующийся из метионина S‑метилметионин:
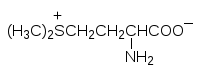
Холин является структурным элементом таких биомолекул, как нейромедиатор ацетилхолин и мембранные липиды.
Кроме этого, S‑метилметионин нормализует обмен жиров и защищает от эрозии стенки желудка. Это его свойство использовалось для лечения язвы желудка, из-за чего его даже называли витамином U (от лат. ulcer — язва). Известно также антигистаминное и антидепрессантное действие S‑метилметионина. Это вещество содержится в сырых овощах, в частности, для лечения язвы желудка использовали свежеприготовленный сок из капустных листьев. Недостаток в этом эндогенном биоактивном веществе, проявляющем к тому же антитоксикантные свойства, испытывают курильщики и те, кто злоупотребляет алкоголем. С этим, очевидно, связан повышенный риск появления у них гастрита и язвы желудка.
В водорослях и в фитопланктоне S-метилметионин подвергается декарбоксилированию и окислительному дезаминированию. Конечным продуктом этих метаболических превращений становится диметилсульфониопропионат (диметил-2-карбоксиэтилсульфоний):
![]()
Предполагается, что это вещество участвует в осмотических эффектах в клетках водных организмов. Диметилсульфониопропионат не имеет ни вкуса, ни запаха. Он накапливается в морских организмах, питающихся фитопланктоном (моллюски, коралловые полипы). Его влияние на человеческий организм пока не стало объектом детального изучения, но именно с ним, очевидно, связано хорошее самочувствие тех, кто употребляет в пищу сырые морепродукты. При нагревании диметилсульфониопропионат разлагается с выделением диметилсульфида, неприятный запах которого сопровождает процесс термической обработки морепродуктов.
Превращения диметилсульфониопропионата в природе приводят к образованию диметилсульфоксида, который восстанавливается до диметилсульфида ДМСО-редуктазой — ферментом с атомом молибдена в активном центре. Летучий диметилсульфид поступает в атмосферу и здесь окисляется до гигроскопичной метансульфокислоты. Образовавшиеся в результате сорбции воды метансульфокислотой микрокапли служат центрами конденсации влаги воздуха над океанами. Образующиеся при этом облака играют важную роль в поддержания теплового режима Земли, т. к. над океанами нет пыли, способствующей образованию облаков над континентами. Увеличенная облаками отражающая способность Земли (альбедо) является определяющим погоду климатическим фактором.
Сернистые соединения определяют бактерицидные, фунгицидные и противовирусные свойства лука и чеснока. Лечебные свойства чеснока упоминаются во всех дошедших до наших времён древних медицинских трактатах. В цитоплазме интактных клеток этих растений содержится производное цистеина аллиин (от лат. allium - чеснок). Он представляет собой замещенный по атому серы аллильной группой цистеин, образующийся из γ-глютамилцистеина:
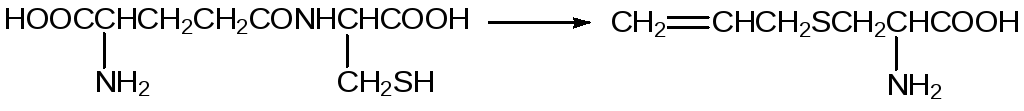
При разрушении клеток аллиин входит в контакт с находившимся в вакуолях ферментом аллииназой, которая разлагает две молекулы аллиина на аллицин и пируват аммония

Аллицин представляет собой тиоэфир, образованный пропентиолом и пропенсульфиновой кислотой. Именно это вещество, образующееся при разрушении клеток чеснока, определяет резкий запах и жгучий вкус, которые ощущаются во рту во время еды пищи с добавлением чеснока.
Кроме аллицина из аллиина в меньших количествах образуются и другие сераорганические соединения, определяющие вместе с ним лечебные свойства чеснока. При измельчении головок чеснока число серосодержащих соединений в образующейся массе возрастает в несколько раз. Кроме того, в чесноке содержатся повышенные количества селенорганических соединений, образующихся по аналогии с сероорганическими. Во всём этом комплексе активных веществ, очевидно, проявляется эффект синергизма, поскольку получить такой же лекарственный эффект с отдельными выделенными из прошедшего естественную ферментацию сока чеснока веществами не удается.
В растениях семейства крестоцветных содержится широкий спектр S‑глюкозидов, которые гидролизуются тиогликозидазой (мирозиназой) с образованием сульфатов оксиминотиокислот:
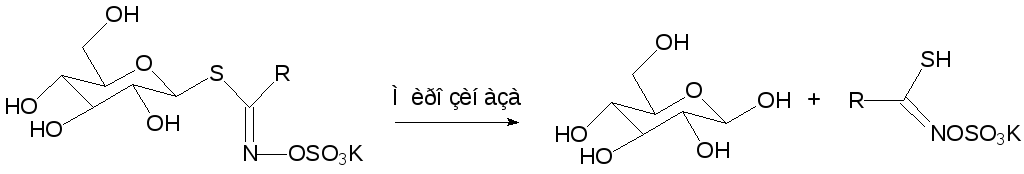
Эти неустойчивые соединения разлагаются различными путями. В частности, в кислых средах они превращаются в нитрилы RCN, тогда как в нейтральных из них образуются изотиоцианаты RNCS.
Самым известным тиогликозидом является тиогликозид синигрин (R = CH2CH=CH2).
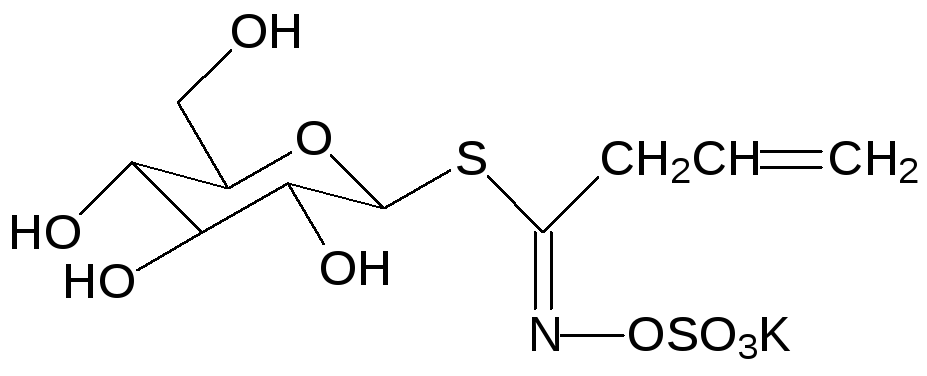
Он содержится в растениях горчицы, хрена, рапса. Особенно много его в семенах горчицы и в корне хрена. Мирозиназа разлагает синигрин с образованием аллилизотиоцианата (CH2=CHCH2NCS), известного как аллилгорчичное масло. Это вещество с резким запахом и жгучим вкусом защищает растения от поедания травоядными животными.
Съеденная в сыром виде капуста брокколи защищает от заболеваний некоторыми видами злокачественных опухолей. Считается, что это связано с образованием в разрушающихся растительных клетках сульфорафана (4‑метилтиоксобутилизотиоцианата). Сульфорафан, как и аллилизотиоцианат, представляет собой продукт ферментативного превращения содержащегося в растениях семейства капустных S‑глюкозида:
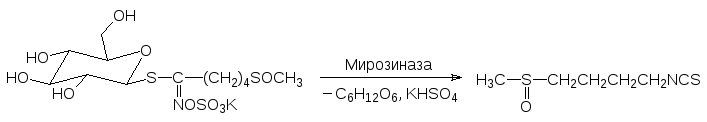
В прошедшей термическую обработку капусте это вещество содержится в ничтожном количестве, поскольку нагревание денатурирует фермент мирозиназу и ускоряет гидролиз изотиоцианатных групп. Интересно, что полученный синтетическим путём сульфорафан не проявляет активности, выявленной у сырой брокколи.
Противораковая активность обнаружена у ещё одного S-гликозида глюкобрассицина:
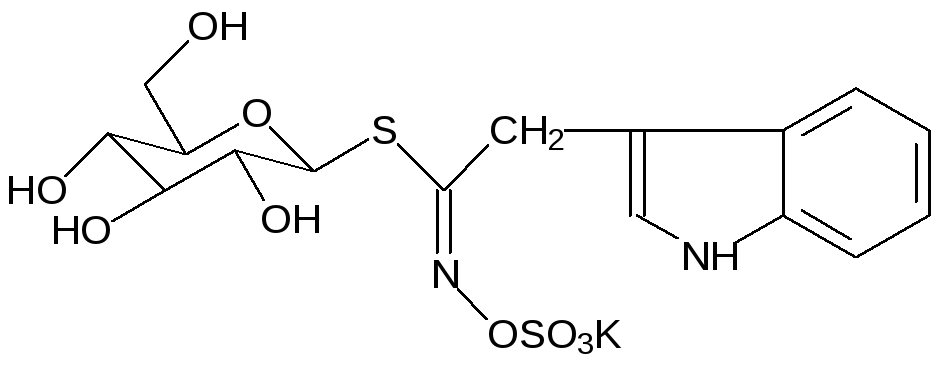
В разных концентрациях это вещество содержится практически во всех растениях семейства капустных, но максимальным содержанием глюкобрассицина отличается вайда красильная. Ферментация листьев вайды использовалась древними кельтами для получения синего красителя, известного сейчас как индиго. Глюкобрассицин снижает риск заболевания раком молочной железы, раком лёгкого и других видов злокачественных опухолей. Действие мирозиназы на глюкобрассицин должно приводить к образованию индол-3-илметилизотиоцианата, но это вещество неустойчиво и в продуктах ферментативного разложения глюкобрассицина обнаруживается в основном индол-3-илкарбинол. Он уже поступает в продажу в качестве биоактивной пищевой добавки, но опыты по использованию его в качестве противоракового средства, антиоксиданта и противосклеротического средства продолжаются.
Понятно, что образующиеся при разрушении растительных клеток сернистые соединения с резким запахом и жгучим вкусом, предназначены прежде всего для пассивной защиты растений от поедания их травоядными животными, а положительный эффект, оказываемый ими в отдельных случаях на здоровье человека, вовсе не означает, что природа специально приготовила их для использования нами в качестве лечебных средств. Так, например, все плесневые грибы выделяют в субстрат, на котором они развиваются, микотоксины, предназначенные для защиты этой среды обитания от других плесневых грибов и бактерий. Многие из микотоксинов токсичны и для человека. Так, например, построенные из аминокислот с участием цистеина токсины бледной поганки вызывают отравления с летальным исходом. Но всё же широкие исследования биологической активности микотоксинов привели к обнаружению бактерицидных веществ с невысокой токсичностью для теплокровных. Нам такие соединения известны как антибиотики. В качестве примера серосодержащих антибиотиков можно привести формулы пенициллинов и цефалоспоринов, например:
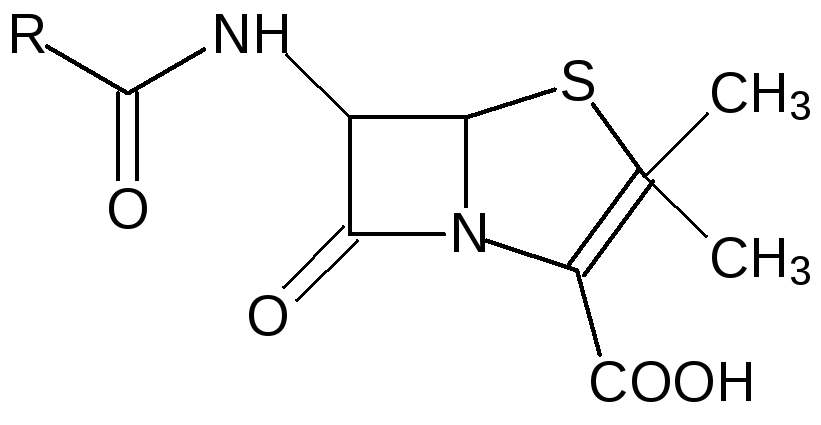
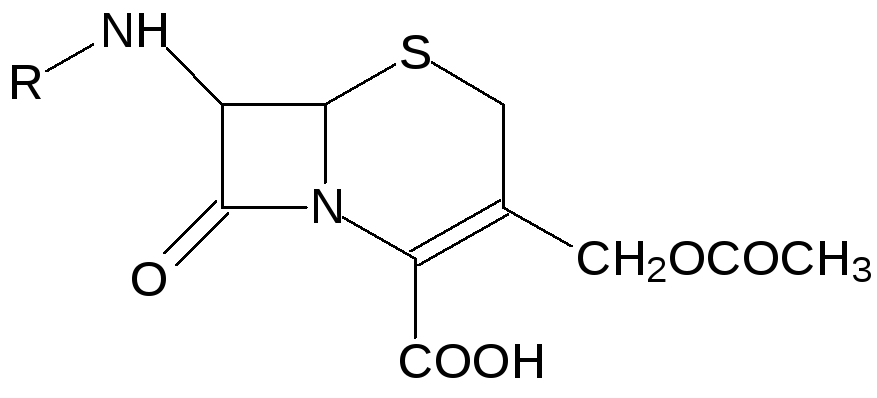
Из морских многощетинковых червей нереид выделен токсин с дитиолановым структурным элементом нереистоксин:
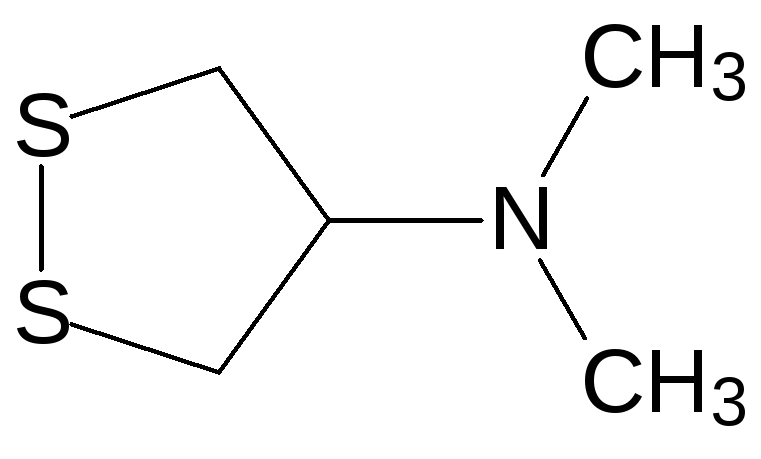
Он показал хорошие инсектицидные свойства при достаточно низкой токсичности для теплокровных. По механизму действия нереистоксин представляет собой антагонист ацетилхолина, блокирующий передачу нервных импульсов в холинорецепторах. Его структура была использована для дизайна более эффективных и безопасных инсектицидов, в числе которых, например, тиоциклам (эвисект, 5-диметиламино-1,2,3-тритиан) и бенсултап (банкол, 1,3-бис(бензолсульфонилтио)-2-диметиламинопропан):
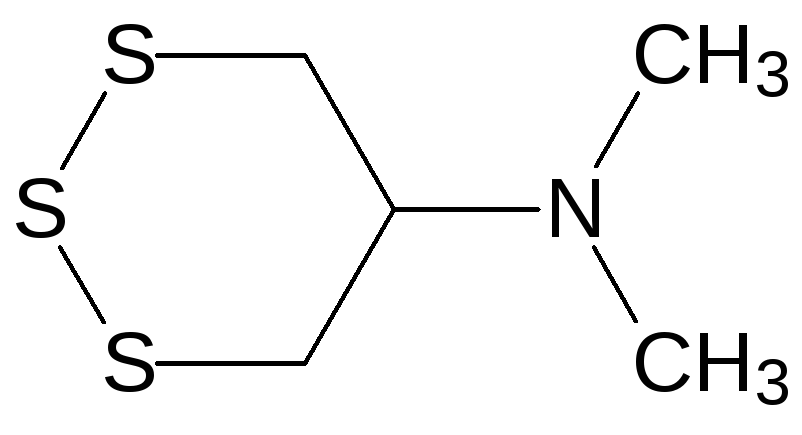 и
и
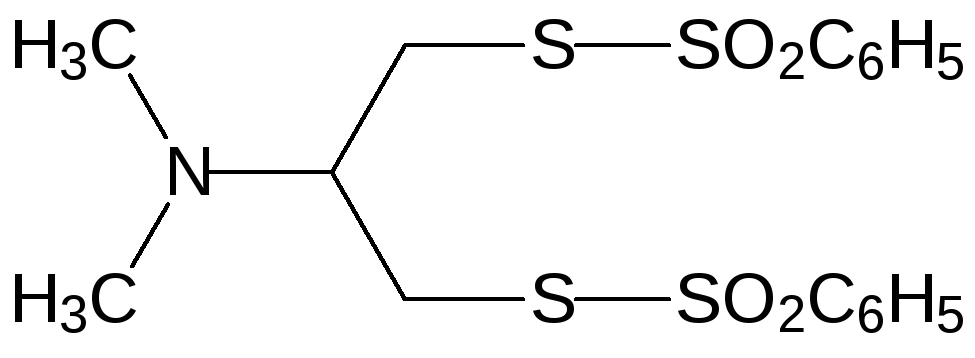
Важное преимущество этих соединений в сравнении с фосфорорганическими и карбаматными инсектицидами состоит в том, что они не взаимодействуют с холинэстеразой и поэтому не вызывают необратимых изменений в работе холинэргических синапсов.
Представленными примерами биологически активных соединений с атомами серы, выделенных из животных, растений и микроорганизмов, конечно, не исчерпывается всё многообразие использования особенностей этого элемента живой природой для биосинтеза защитных веществ.
Органические производные селена
Первые селенорганические соединения (алкилселенолы, селениды и диселениды) были получены ещё в XIX веке, но неприятный запах, токсичность и нестабильность долгое время препятствовали проведению исследований по их практическому применению в органическом синтезе.
В химических свойствах селена и серы есть много общего. У селена, как и у серы, пять степеней окисления: −2, 0, +2, +4 и +6. Селенолы подобно тиолам получают по реакции элементного селена с металлорганическими соединениями, селенолы, как и тиолы, легко окисляются с образованием диселенидов; сульфоксидам соответствуют селеноксиды, а сульфеновым и сульфиновым кислотам соответствуют селениновые и селеноновые кислоты и т.д. Поэтому описание таких превращений на селенорганических соединениях не представляет особого интереса.
Однако у селенорганических соединений есть своя специфика. В общем случае соединения селена более нуклеофильны и имеют более высокую кислотность (для С6Н5SеН pKa = 5.9), чем соответствующие соединения серы. Ещё одна особенность обусловлена невысокой прочностью связи селена с углеродом — селен образует более длинную и более слабую связь с атомом углерода (234 кДж/моль для связи Se-C и 272 кДж/моль для связи S-С).
Селениды (R-Se-R) и диселениды (R-Se-Se-R) представляют собой самые стабильные органические производные селена. Связь между атомами селена в диселенидах может разрываться действием восстановителей и окислителей с образованием при этом электрофильных или нуклеофильных интермедиатов, а радиационное воздействие приводит к гомолитическому разрыву связей между атомами селена с образованием селенцентрированных радикалов.
Образующиеся из диселенидов и галогенов арильные и алкильные селенилгалогениды, например RSeCl, представляют собой электрофильные реагенты, используемые в органическом синтезе. Определённый синтетический интерес представляют и селенорганические соединения с окисленными атомами селена — аналогичные сульфоксидам селеноксиды (R2SeO) и аналоги сульфонов селеноны (R2SeO2).
Лабильность связи углерода с селеном демонстрируется реакцией окисления аллильной СН-связи диоксидом селена. Она протекает с промежуточным образованием CSe-связи и с последующей перегруппировкой с её разрывом:
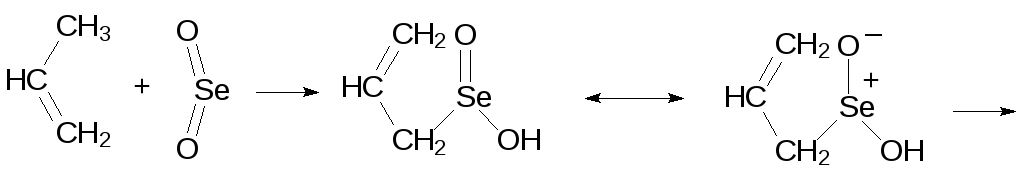
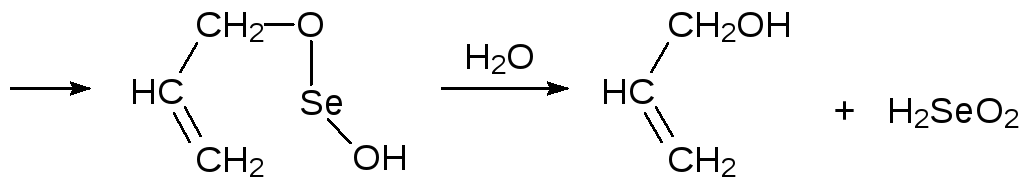
Так же можно переводить в аллильные спирты соединения с эпоксидными группами. Для этого используют уже реагенты с нуклеофильными атомами селена. Для этого, например, восстанавливают дифенилдиселенид боргидридом натрия в спирте:
![]()
Полученное соединение представляет собой комплекс фенилселенида натрия с триэтилборатом. Фенилселенид натрия реагирует с эпоксидной группой с раскрытием цикла. После этого атом селена окисляют пероксидом водорода, а образующийся селеноксид в мягких условиях разлагается с образованием двойной связи:
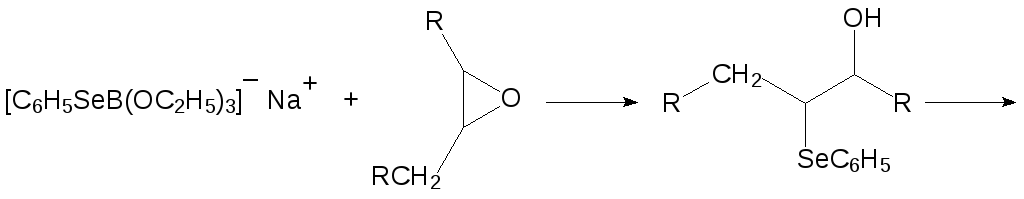
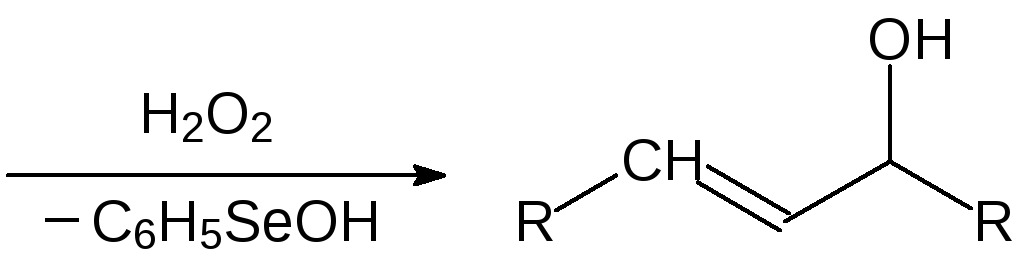
В ещё одном способе образования двойной связи в качестве исходного селенорганического соединения используют образующийся при хлорировании дифенилдиселенида бензолселенилхлорид. Действием бензолселенилхлорида на кетон замещают один из активированных карбонильной группой атомов водорода. Полученный дизамещенный селенид окисляют пероксидом водорода, а образовавшийся селеноксид аналогично предыдущему отщепляет элементоорганический структурный элемент региоспецифично по схеме цис-элиминирования: