Материал: сера и селен дом
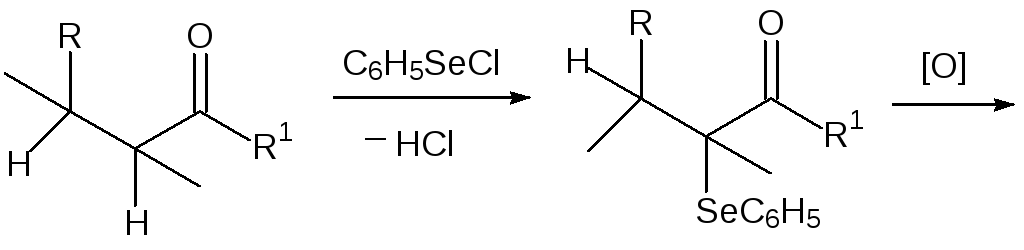
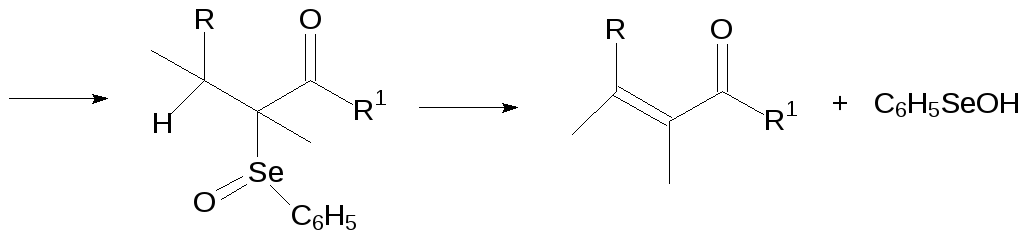
С участием селенорганических соединений с высоким выходом регио- и стереоспецифично протекают многие реакции, сопровождающиеся образованием новых СС-связей. Эти и другие особенности химии селенорганических соединений послужили основанием для интенсивного изучения синтетических возможностей, которые представляют соединения с SeС-связями (см., например, Organoselenium Chemistry: Modern Developments in Organic Chemistry, Ed. Thomas Wirth, Springer Vrl., 2000).
Селен в течение многих лет рассматривался только как элемент, все соединения которого имеют неприятный запах и токсичны. Избыточное поступление селена в организм человека действительно приводит к нарушению обменных процессов, при этом более всего нарушается биосинтез белков. Соединения селена могут вызывать анемию, поражение центральной нервной системы, тканей печени. В местностях, где почва содержит аномально большое количество селена, у животных наблюдается «щелочная болезнь» — выпадение шерсти, деформации и размягчение рогов и копыт, симптомы анемии. Повышенное содержание селена в продуктах питания приводит к разрушению эмали зубов, хроническим артритам и желудочно-кишечным расстройствам.
Однако уже в 50‑е годы прошлого века было показано, что селен является обязательным микроэлементом. Его поступление в организм в определенных достаточно узких пределах концентраций защищает экспериментальных животных от некротического перерождения печени, а недостаточное поступление селена в организм человека лежит в основе нейродегенеративных заболеваний, болезни Кешана (кардиомиопатия) и Кашина-Бека (остеохондропатия). Дефицит по селену проявляется в утомляемости, ослаблении иммунитета, мышечной дистрофии. Показано, что селенсодержащие ферменты участвуют в реакциях иодирования при образовании гормонов щитовидной железы. Важно также, что дефицит по селену связан с повышенным риском появления злокачественных новообразований. При этом надо принимать во внимание, что оптимальное количество селена, поступающего в организм человека, составляет около 100 мкг/день, при этом в мультивитаминные составы его включают в количестве до 70 мкг в дневной дозе. Показано, что избыточное поступление селена в количествах более 400 мкг/день приводит к потере волос и нарушению структуры ногтей, а в количествах более 2400 мкг/день проявляется эффект хронической токсичности. Известно также, что неорганические соединения селена значительно превосходят по токсичности его органические производные, так, например, для селенистого ангидрида ПДК составляет 0,1 мг/м3.
Растения синтезируют селенсодержащие аминокислоты из селенсодержащих минеральных компонент почвы, включающихся в метаболизм вместе с сульфитами и сульфатами. Основным источником поступающего в организм человека и животных селена являются продукты растительного происхождения (чеснок, бразильский орех), но его много и в таких субпродуктах, как почки и печень.
В организме человека селен присутствует в основном в виде трёх аминокислот: селеноцистеина (её считают 21-й белковой аминокислотой), селенометионина и S-метилцистеина. В 1973 г. был выделен первый фермент с атомом селена в активном центре — глютатионпероксидаза, участвующая в нейтрализации активных форм кислорода. Селеноцистеин входит также в состав, дегидрогеназ, глицинредуктазы, тиоредоксинредуктазы. Связанный с селеном антиоксидантный эффект существенно усиливается витамином Е, что предполагает синергизм их действия. Благоприятствует активности глутатионпероксидазы и витамин С за счет повышения кишечной адсорбции микроэлемента.
Исключительное значение имеет открытие селенсодержащего белка, находящегося в мембранах клеток печени, почек, щитовидной железы. Этот фермент иодтиронин-5-деиодиназа катализирует отщепление иода от тироксина с образованием основного гормона щитовидной железы — трииодтиронина. Описанный эффект его действия свидетельствует о тесных взаимоотношениях между двумя микроэлементами: иодом и селеном, а также о возможности развития патологических состояний щитовидной железы при дефиците не только иода, но и селена. Учитывая фундаментальную роль щитовидной железы в регуляции обмена веществ, значение этого открытия трудно переоценить.
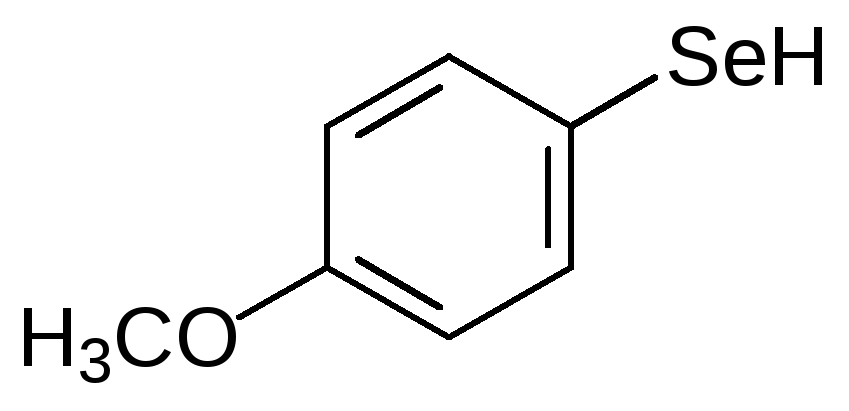
Полученные в ходе синтетических исследований селенорганических соединений вещества проявляют интересные виды биологической активности. В частности, они могут быть гербицидами, фунгицидами и бактерицидами. Противораковая активность была обнаружена у 4‑метоксибензолселенола:
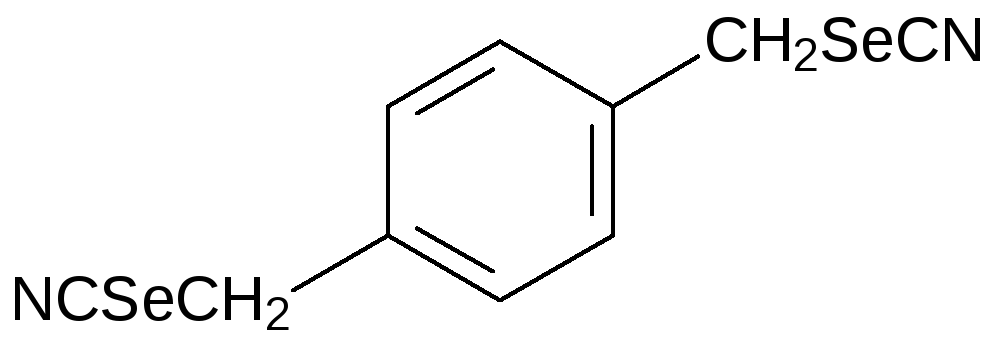
Ещё более эффективным противораковым средством оказался 1,4‑бис(селеноцианатометил)бензол:
Получены и другие селенорганические соединения с противораковыми свойствами и с другими видами фармакологической активности.
Хорошие профилактические свойства по отношению к онкологическим заболеваниям показывает октагидро-9- фенилселеноксантен (селексен, БАД Селен Актив):
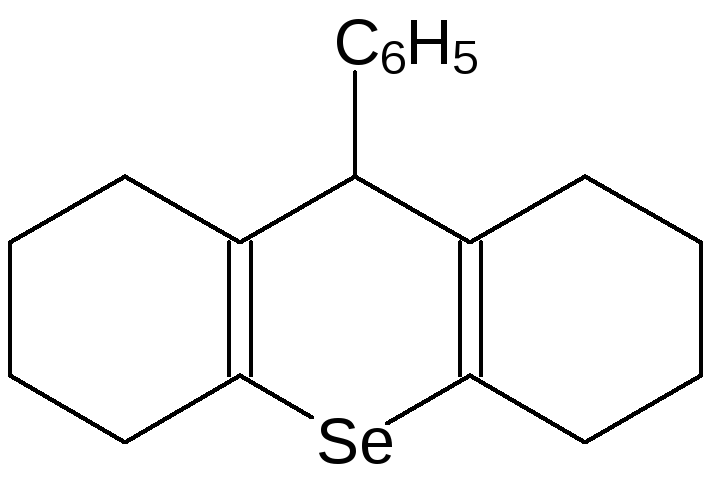
Одним из самых интересных селенорганических соединений оказался эбселен (2-фенил-1,2-бензизоселеназол-3(2H)-он):
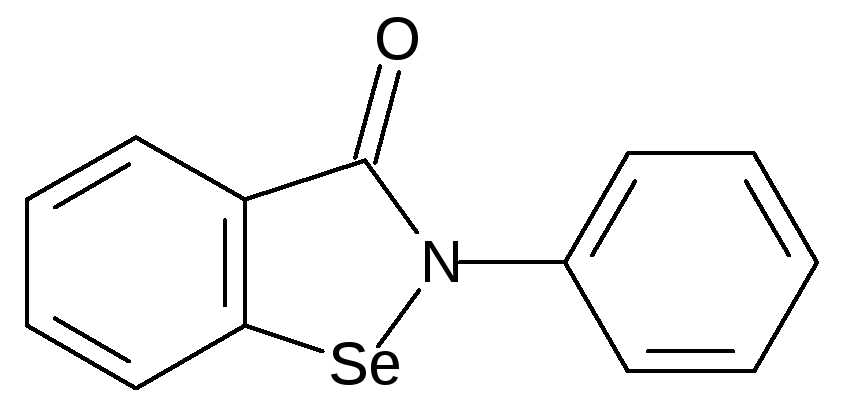
Известно несколько способов получения эбселена. Впервые он был получен из бензанилида. На первой стадии действием диизопропиламида лития (LDA) бензанилид переводят в N-литиевое производное:
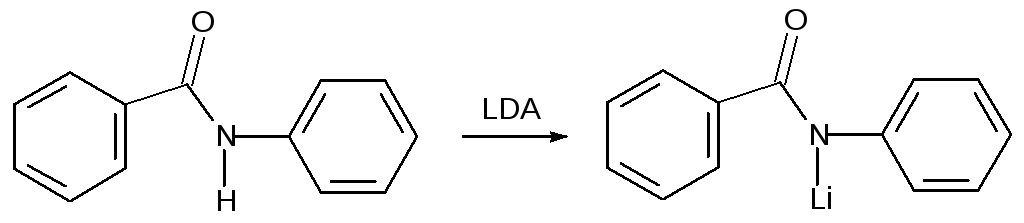
Затем прибавляют бутиллитий, который избирательно замещает в этом соединении атом водорода в орто-положении к карбонильной группе, и обрабатывают полученное литийорганическое соединение элементным селеном:
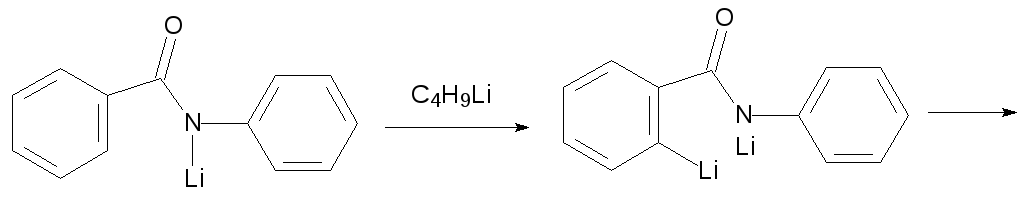
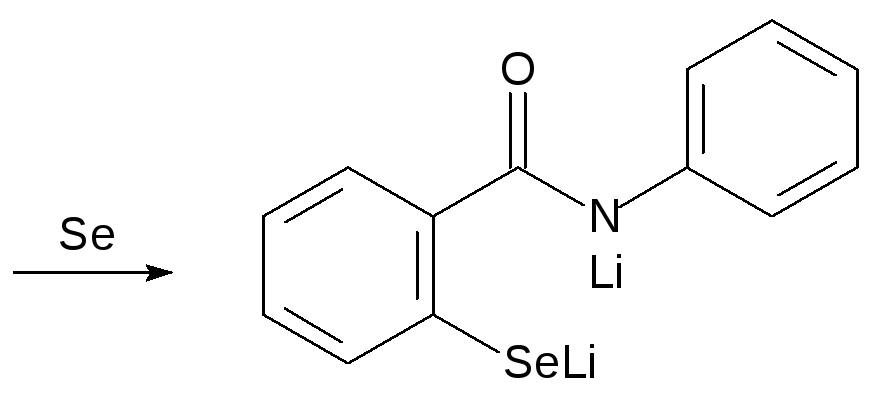
Действие дибромида меди на полученный селенид приводит к циклизации с образованием эбселена:
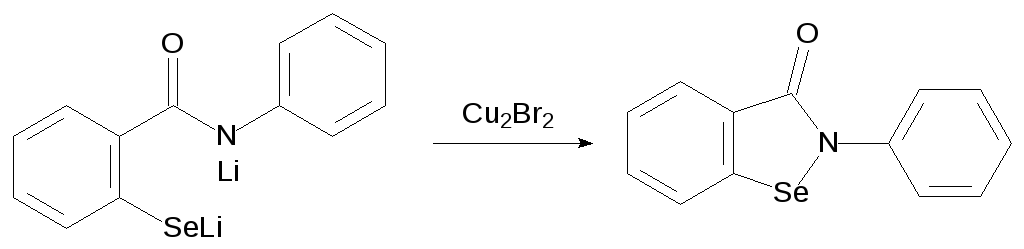
Ещё один способ получения эбселена представлен катализируемой иодидом меди реакцией 2‑бром(иод)бензоиланилина с элементным селеном в присутствии карбоната калия при температуре около 110 °С в диметилформамиде:
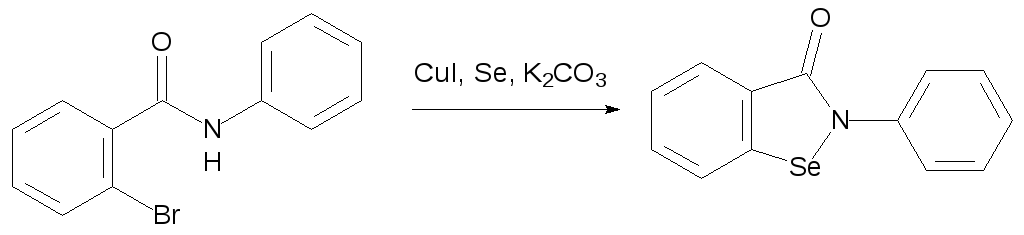
Интересно, что выход в этой реакции в зависимости от природы заместителей в ароматических остатках может составлять 96 %.
Биохимические процессы в организме человека протекают с использованием дегидрогеназ, супероксиддисмутазы, глютатионпероксидазы и других ферментов в качестве антиоксидантных систем для предотвращения оксидативного стресса. Любые функциональные изменения в этих ферментах могут приводить к воспалениям и к онкологическим заболеваниям. В метаболизме с участием кислорода образуются его активные формы - супероксидный анионрадикал и пероксидный анион, окисляющие биомолекулы. Супероксиддисмутаза катализирует диспропорционирование супероксида на кислород и пероксид, а пероксид дисропорционирует в присутствии каталазы с образованием кислорода и воды или же восстанавливается глютатионпероксидазой в митохондриях или в цитозоле.
Глютатионпероксидаза включает четыре идентичных белковых субъединицы, каждая из которых содержит в активном центре один атом селена. Известны по крайней мере четыре типа близких по строению глютатионпероксидаз: а) цитозольная, б) желудочнокишечная, в) плазматическая и г) фосфолипидная глютатионпероксидазы. Представленный на схеме механизм действия глютатионпероксидаз включает взаимодействие селенольной формы фермента ЕSeH с органическим гидропероксидом или пероксидом водорода ROOH с образованием окисленной формы фермента ЕSеОH, её взаимодействие с глютатионом (GSH) с образованием воды и глютатионилглютатионпероксидазы (ЕSeSG) и восстановление активной формы фермента ЕSeH в реакции ЕSeSG с глютатионом с его превращением в дегидроглютатион (GSSG):
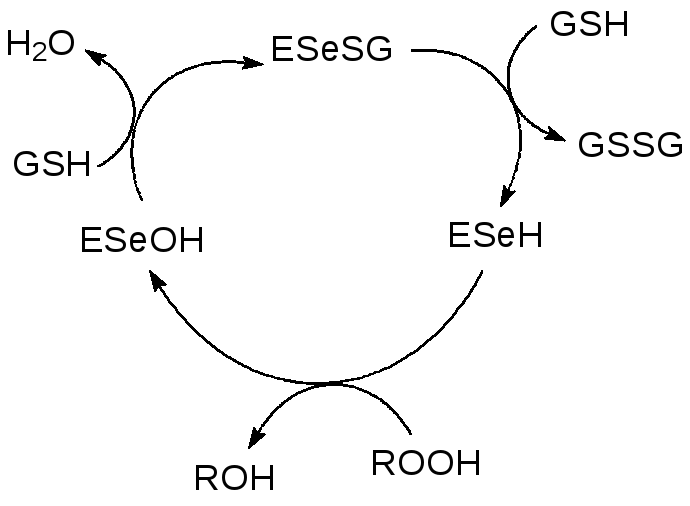
В соответствии с этим при посредничестве глютатинопероксидазы гидропероксид превращается в воду или гидрокисидное соединение, пероксидный атом кислорода восстанавливается до воды, а две молекулы глютатиона превращаются в дегидроглютатион. Фермент защищает от повреждающего действия перекиси водорода, гидропероксидов ненасыщенных и полиненасыщенных жирных кислот, холестерина и других продуктов перекисного окисления липидов, обладающих сильным повреждающим действием на биомембраны и биологически активные молекулы. Таким образом, селен защищает организм от накопления продуктов пероксидов, нормализует состояние ядер, предупреждает повреждение их хромосом, стимулирует функции рибосом, а, следовательно, и синтез белка.
Соединения селена участвуют в регуляции синтеза нуклеиновых кислот и белков, снижают концентрацию липидов и глюкозы в крови, нейтральных жиров в печени при одновременном накоплении макроэргических участников метаболизма. Антисклеротический эффект эндогенных селенорганических соединений связан с его влиянием на обменные процессы с участием метионина. Отмечено их влияние и на активность других ферментативных систем.
Синтетическое соединение эбселен уже используется в качестве лекарственного средства. В организме человека он выполняет функции глютатионпероксидазы, нейтрализуя вместе с глютатионом пероксидные соединения в соответствии со схемой:
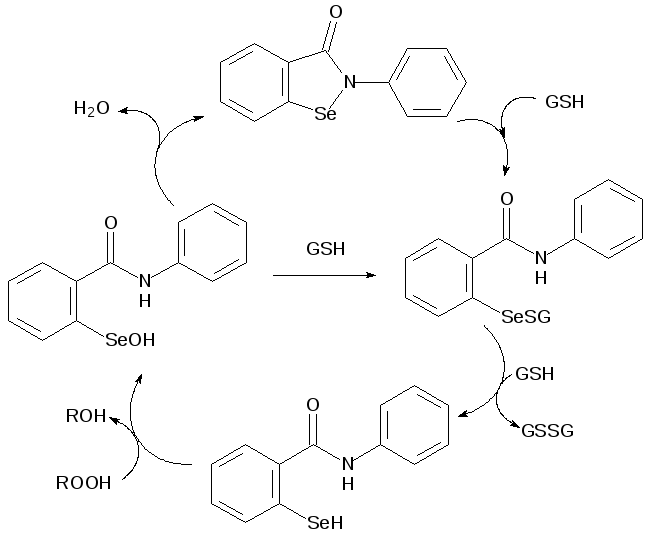
Пока в качестве антиоксидантов и средств для профилактики онкологических заболеваний используются только селексен и эбселен, но синтез новых селенорганических соединений может привести к получению ещё более активных веществ с цитостатическими свойствами и с другими видами фармакологической активности.
Development of Isoselenocyanate Compounds’ Syntheses and Biological Applications
As the number of cases and cancer-related deaths are projected to rise in upcoming years, it is urgent to find ways to prevent or treat cancer. As such, food-derived products have gained attention as potential chemopreventive agents due to their availability, safety, and low cost. Isothiocyanates, the breakdown products of sulfur-containing glucosinolates in cruciferous vegetables, have shown substantial anticarcinogenic and chemopreventive activities for different human cancers. Furthermore, organoselenium compounds are known to exhibit chemopreventive and chemotherapeutic activity; moreover, these compounds are more effective anticancer agents than their sulfur isosteres. Hence, isothiocyanates have been modified to yield isoselenocyanates, which are more cytotoxic toward cancer cells when compared to their corresponding sulfur analogues. Herein, the synthesis and development of isoselenocyanates as novel treatments for cancer and other diseases are reviewed, highlighting the diverse chemistry and computational studies of this class of compounds as well as their pertinent biological applications.