Материал: сера и селен дом
Сульфоны
Еще один класс сероорганических соединений с атомом серы в максимальной степени окисления представлен сульфонами. Они образуются при окислении сульфидов (тиоэфиров) с промежуточным образованием сульфоксидов:
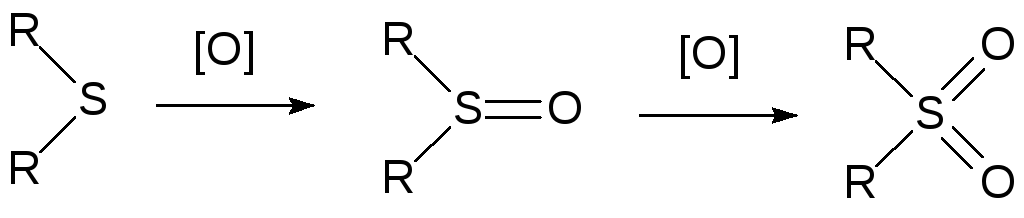
В роли окислителей могут выступать надкислоты, азотная кислота, перманганат калия в разбавленной серной кислоте или в уксусной кислоте, бихромат натрия и др. Пероксид водорода окисляет сульфиды до сульфонов в присутствии катализаторов на основе кислот молибдена, вольфрама и ванадия. Чаще всего для окисления сульфидов используют надуксусную кислоту, образующуюся из 30 %-го пероксида водорода в смеси ледяной уксусной кислоты и уксусного ангидрида (50:50). При окислении надуксусной кислотой прибавлением её к органическому сульфиду часто наблюдается индукционный период. Окисление азотной кислотой сопровождается выделением нитрозных газов, которые после доокисления кислородом воздуха можно возвращать в процесс.
Сульфоны являются побочными продуктами при сульфировании ароматических соединений серной кислотой, поскольку сульфокислоты реагируют с исходными веществами так же, как и серная кислота. Для направленного получения сульфонов из сульфокислот и ароматических соединений в качестве катализатора реакции сульфонирования используют полифосфорную кислоту (ПФК), например:
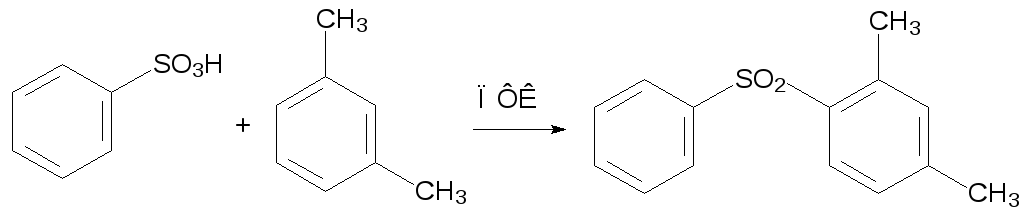
По реакции Фриделя-Крафтса сульфоны получают ацилированием ароматических соединений сульфохлоридами при катализе хлоридом алюминия:
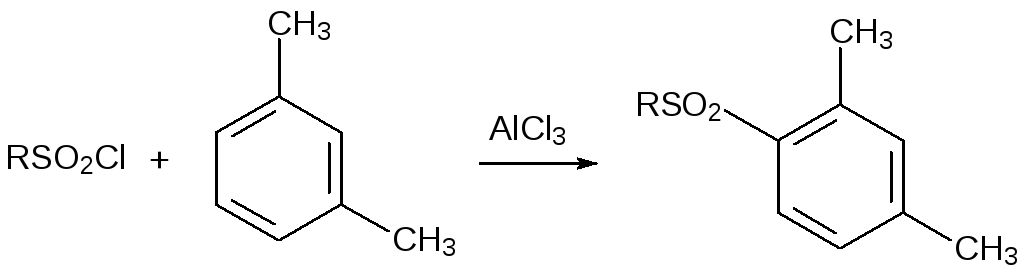
В качестве растворителей в этой реакции используют дихлорметан или дихлорэтан.
Выше были представлены превращения сульфиновых кислот, в которых образуются сульфоны. Для присоединения сульфиновых кислот к непредельным связям, протекающим с образованием сульфонов, эти связи должны быть поляризованы электроноакцепторными группами. Так, например, в реакцию с сульфиновыми кислотами могут вступать акриловые кислоты, их эфиры, винилкетоны, нитроэтиленовые соединения и винилсульфоны, например:
![]()
При облучении УФ светом или в присутствии катализаторов радикальных реакций диоксид серы реагирует с этиленом с образованием полимерных этиленсульфонов:
![]()
Специфическим полярным апротонным растворителем является 1,1‑диоксотиолан (сульфолан). Его используют в промышленности в экстракционных способах очистки углеводородов и в лабораторной практике. Сульфолан получают в двухстадийном процессе, включающем реакцию бутадиена с диоксидом серы и гидрирование образующего продукта циклизации на катализаторах на основе никеля Ренея:
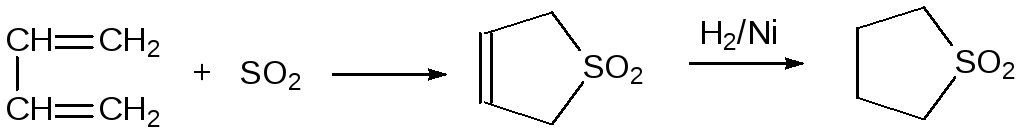
Атомы водорода в α-положении к сульфонильной группе активированы. Так, например, они могут замещаться в реакциях с бутиллитием, реактивами Гриньяра, гидридом натрия или амидом натрия. Образующиеся металлорганические соединения можно использовать для получения сульфонов более сложного строения:
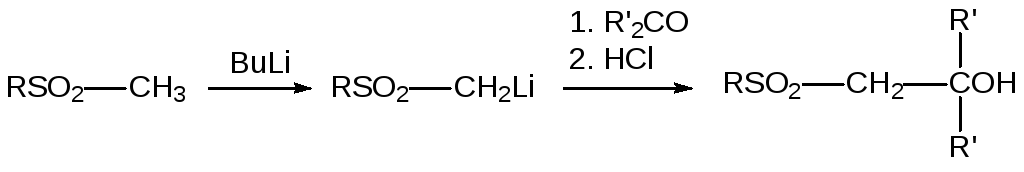
Важно, что образующиеся в реакциях металлорганических производных сульфонов продукты могут отщеплять сульфоновую группу в результате восстановления или элиминирования в присутствии оснований. Так, например, при алкилировании литийорганических соединений на основе сульфонов эфиром бромуксусной кислоты образуются сложные эфиры с сульфогруппой в β-положении, которые в присутствии оснований отщепляют сульфоновую группу и превращаются в эфиры акриловых кислот:
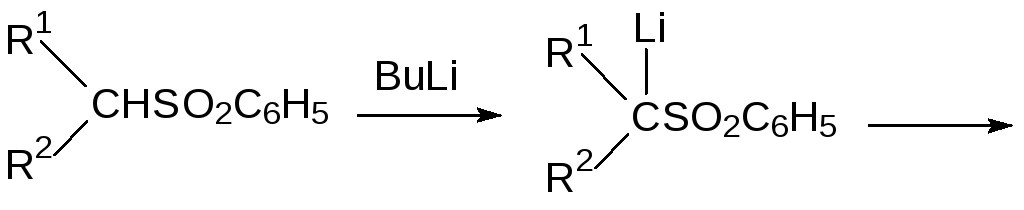
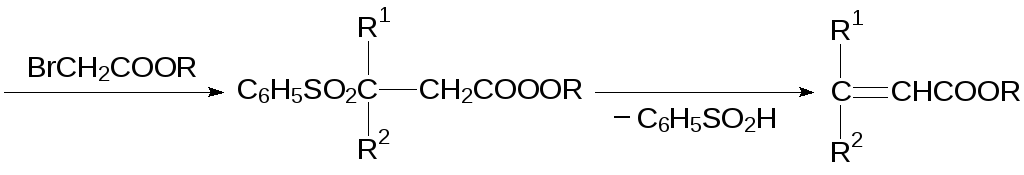
Индуктивный эффект SO2-группы, проявляющийся на связанных с ней алкильных остатках, используется, например, в синтезе хризантемовой кислоты, входящей в состав пиретринов и пиретроидов с инсектицидной активностью. По реакции натриевой соли бензолсульфиновой кислоты с диметилаллилхлоридом получают диметилаллилфенилсульфон:
![]()
Действием этилмагнийбромида его переводят в магнийорганическое соединение, которое реагирует с двойной связью эфира диметилакриловой кислоты с образованием трёхчленного цикла, элиминируя фенилсульфинат:
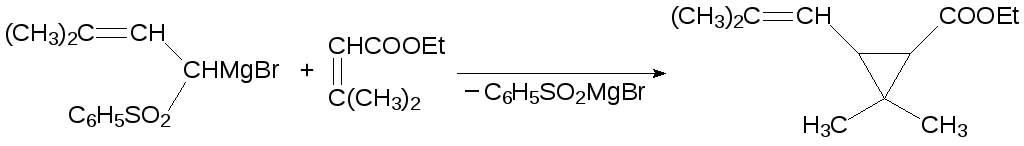
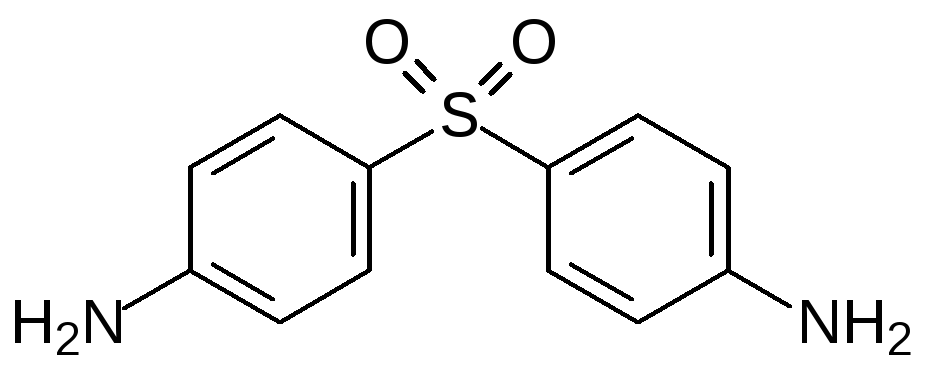
Для лечения проказы и других инфекций используется Дапсон, представляющий собой достаточно простое соединение – 4,4´-диамино-дифенилсульфон:
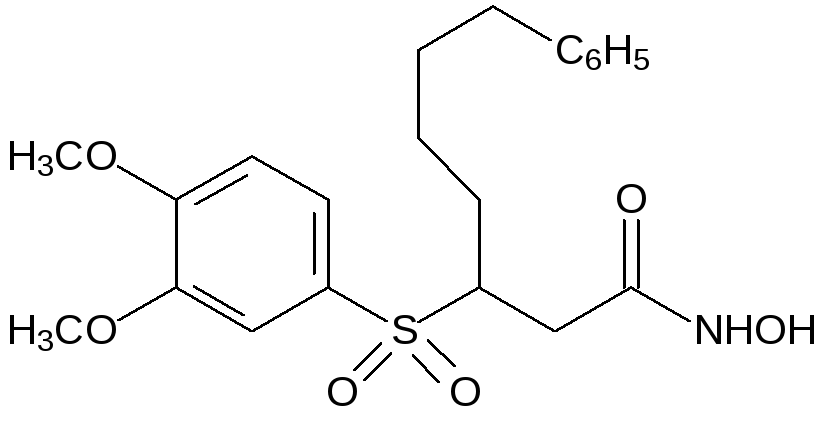
Сульфоновые функциональные группы, имитирующие пептидные группы СONH, вводят в состав фармакологически активных соединений со свойствами пептидомиметиков. Так, например, избирательным блокатором некоторых матриксных металлопротеиназ является соединение формулы:
Матриксные металлопротеиназы предназначены для разложения внеклеточных белков. Ингибиторы этих ферментов могут найти применение для лечения метастазирующего рака, язвы желудка, ревматоидного артрита, остеопороза и других заболеваний, а также для замедления старения кожи.
Производные серы в живой природе
Органические соединения серы играют важную роль в живой природе. Атомы серы в их составе легко вступают в окислительно-восстановительные превращения, а соединения с тиольными и тиоэфирными группами отличаются высокой нуклеофильностью. Можно предположить, что реакции с переносом электронов с участием атомов серы и железа лежали в основе процессов, приведших к зарождению жизни. Первичная оболочка Земли содержала значительные количества сероводорода и двухвалентного железа. Образованные ими железосерные кластеры включались в белковые молекулы для осуществления требуемых для метаболических процессов окислительно-восстановительных превращений. И на современном уровне развития живой природы железосерные белки распространены во всех царствах, включая животных, растения, грибы, бактерии и археи. Они участвуют в переносе электронов в процессе окислительного фосфорилирования в мембранах митохондрий и хлоропластов, обеспечивают работу многих ферментов, в частности, такого важного фермента, как цис-аконитаза в цикле Кребса.
Атомы серы входят в состав двух из двадцати белковых аминокислот – цистеина и метионина:
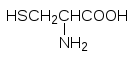
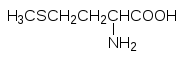
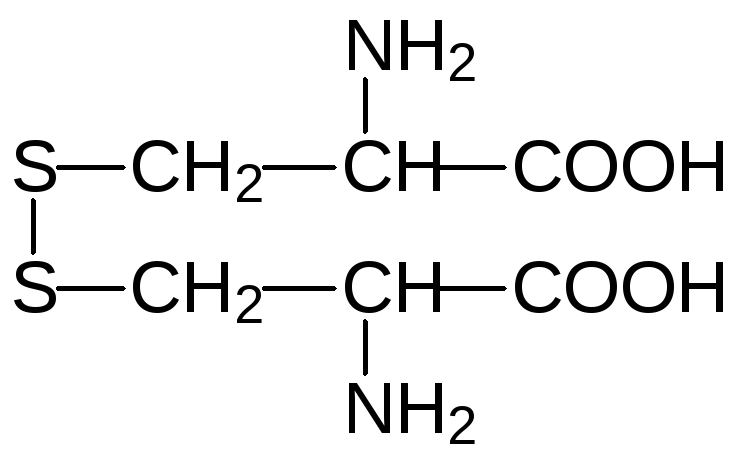
Дисульфидные мостики, образующиеся при окислении сульфгидрильных групп включенных в пептидную цепь молекул цистеина стабилизируют третичную структуру белков. При гидролизе белков две соединенные дисульфидной связью молекулы цистеина выделяются в виде ещё одной серосодержащей аминокислоты цистина:
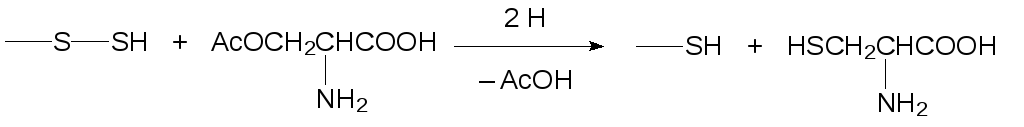
Образование всех сероорганических соединений в живой природе начинается с биосинтеза белковой аминокислоты цистеина. Поступающий в клетки растений и микроорганизмов сульфат реагирует с аденозинтрифосфатом. Образующийся в этой реакции аденилилсульфат переносит сульфатный остаток на сульфгидрильную группу в молекуле белка переносчика с образованием тиосульфатного структурного элемента -S-SO3H, который восстанавливается ферредоксином, превращаясь в ‑S‑SH. Такой механизм восстановления сульфата реализуется для того, чтобы исключить образование токсичного и подвижного сероводорода. Далее при катализе цистеинсинтазой функциональная группа -S-SH реагирует с ацетатом серина по схеме:
Из цистеина в растительных клетках образуется другая белковая аминокислота метионин. Для этого β-карбоксильная группа аспарагиновой кислоты восстанавливается с образованием гомосерина в цепочке превращений:
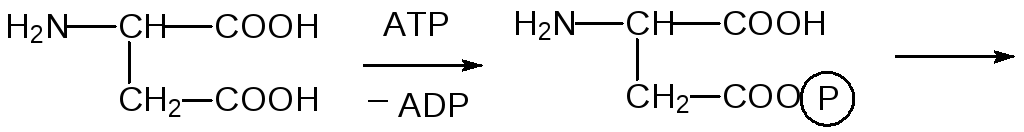
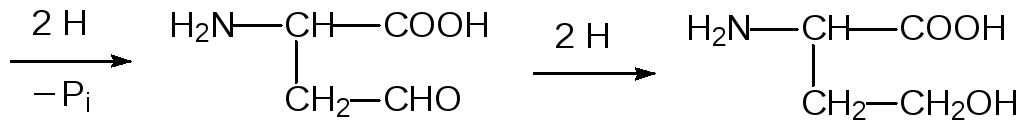
Образовавшаяся гидроксильная группа ацилируется ацилкоферментом А, и О-ацилированный гомосерин при катализе О-ацилгомосерин-(тиол)лиазой реагирует с цистеином с образованием цистатионина:
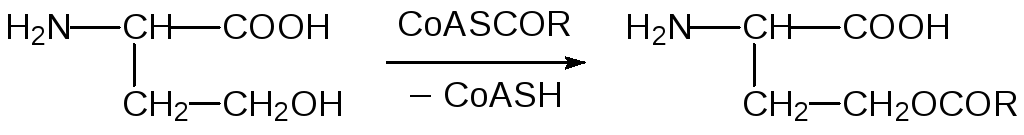
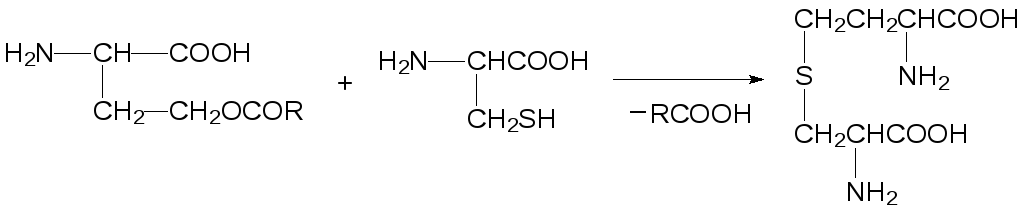
Далее цистатионин-β-лиаза разлагает цистатионин на гомоцистеин и пируват аммония:
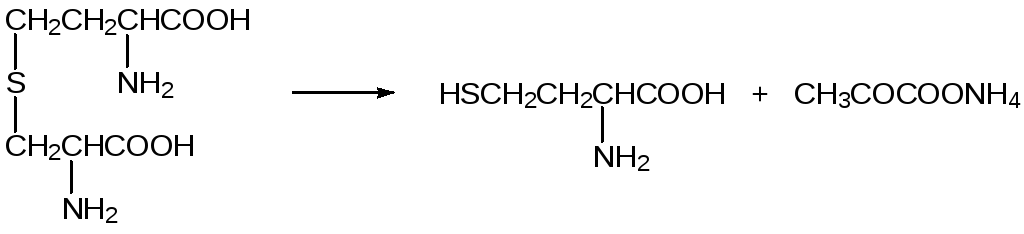
Образовавшийся гомоцистеин метилируется по атому серы N5‑метилтетрагидрофолилтриглутаматом (N5-Me-H4Fol-TriGlu):
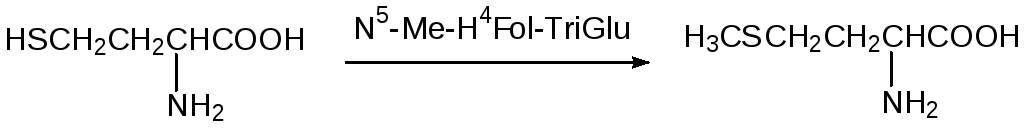
Содержания метионина в растениях, лежащих в начале пищевой цепи гетеротрофных представителей живого, чаще всего достаточно для покрытия потребности организмов животных в органических соединениях серы. Лишь при составлении комбикормов для птиц появляется потребность в добавлении метионина. В соответствии с этим протекающие в клетках животных метаболические процессы используют метионин в качестве основного исходного продукта для образования сернистых соединений, включая цистеин, а метионин является незаменимой аминокислотой.
При недостатке цистеина часть поступающего с пищей метионина превращается в эту аминокислоту. Ключевым соединением и в этом случае является цистатионин. Связанные с этим биохимические реакции включают образование из метионина и аденозинтрифосфата S‑аденозилметионина и его деметилирование с образованием гомоцистеина, который реагирует с серином с образованием цистатионина при катализе цистатионинсинтазой:
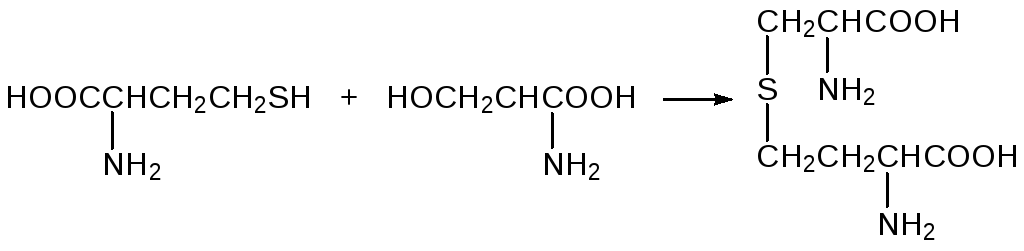
После этого по аналогии с представленной выше схемой биосинтеза цистеина в метаболизме растений цистатионин разлагается пиридоксальфосфатзависимым ферментом γ-цистатионазой, но в клетках животных цистатионин разлагается не на гомоцистеин и пируват, а на цистеин и α‑кетобутират:

Образующиеся из цистеина структурные элементы с сульфгидрильными группами участвуют в работе активных центров оксидоредуктаз (тиоредоксин), а также в работе мультиферментной системы, синтезирующей пальмитиновую кислоту, из которой образуются все другие жирные кислоты. В результате декарбоксилирования цистеина образуется цистеамин H2NCH2CH2SH, входящий в состав участвующего во всех превращениях жирных кислот и в синтезе пренильных соединений, терпенов и стероидов кофермента А (CoA-SH):
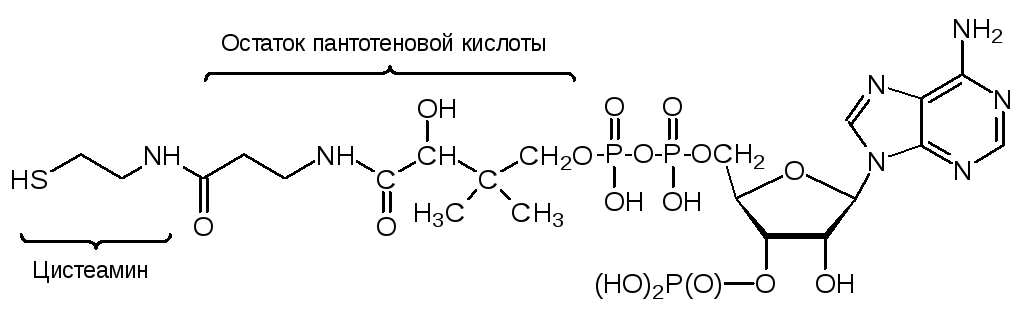
Окисление цистеамина приводит к образованию таурина H2NCH2CH2SO3H с самыми разными регуляторными функциями в биохимических процессах в живых системах.
В работе пируватдегидрогеназного мультиферментного комплекса участвует простетическая группа на основе липоевой кислоты с дитиолановым структурным элементом:
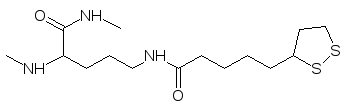
Дисульфидная связь в этом гетероцикле раскрывается в реакции с гидроксиэтильным остатком, связанным с тиаминпирофосфатным коферментом. Дитиолановый цикл при этом раскрывается по схеме восстановления дисульфидной связи, принимая образовавшуюся из гидроксиэтильного остатка ацетильную группу по одному из атомов серы. Далее ацетильная группа переносится на кофермент А и соединенный с ферментом остаток липоевой кислоты оказывается в восстановленном виде с 1,3-дитиольной группой вместо дитиолановой. Обратное превращение дитиола в дитиолан протекает по схеме дегидрирования. Однако дитиольный структурный элемент в остатке дигидролипоевой кислоты может реагировать с ионами тяжёлых металлов, связываясь с ними двумя прочными связями. Понятно, что такие соли не могут дегидрироваться с образованием дитиоланового структурного элемента и не могут участвовать в окислительно-восстановительных превращениях. Следствием отравления солями тяжёлых металлов становится блокировка работы пируватдегидрогеназного мультиферментного комплекса. Это лишает клетку важнейшего источника энергии. Тяжёлые металлы связываются и с другими сульфгидрильными группами в составе белков и ферментов, нарушая их нормальное функционирование. Липоевая кислота легко образуется в организме из других серосодержащих соединений, но в свободном виде она в организме присутствует в ничтожных количествах. Понятно, что введение в организм малотоксичных дитиольных соединений может быть использовано для профилактики и лечения отравлений солями мышьяка, ртути, свинца, таллия и других тяжёлых металлов. Одним из таких соединений является входящая во все фармакопеи дигидролипоевая кислота:
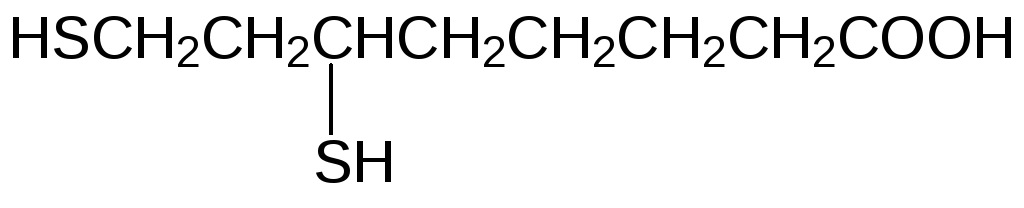
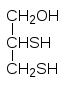
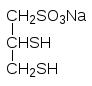
Синтетическими препаратами с аналогичным антидотным действием являются дитиоглицерин (БАЛ, Британский антилюизит) и унитиол (натриевая соль 2,3-димеркаптопропансульфокислоты):
В качестве средств, нейтрализующих токсическое действие ионов тяжёлых металлов, могут выступать и соединения с одной тиольной группой. В этой связи можно назвать N-ацетилцистеин, используемый преимущественно в составе муколитических препаратов для лечения кашля:
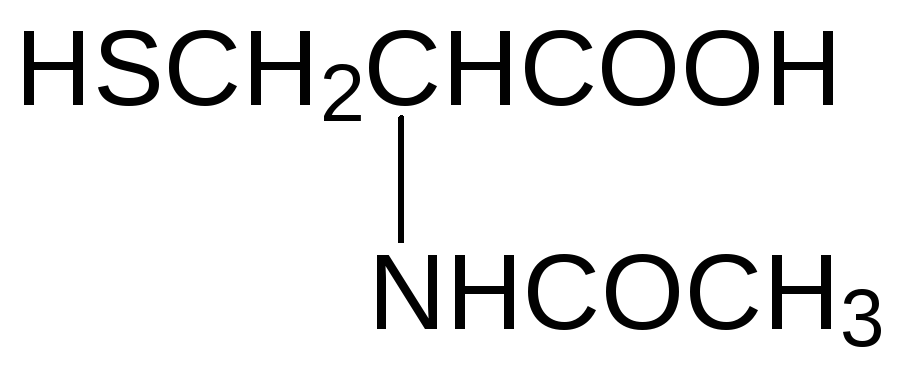
Его эффект основан на восстановлении дисульфидных связей в гликопротеинах слизистых выделений. Следствием этого становится снижение их молекулярной массы и вязкости их растворов. Связанное с приёмом ацетилцистеина повышение содержания свободных тиольных групп в организме потенцирует бактерицидный эффект антибиотиков. Отмечено также повышение уровня глютатиона на фоне приёма ацетилцистеина в дозах от 200 до 600 мг в сутки.
Простетическая группа ферментов, вводящих в молекулы метаболитов карбоксильную группу с образованием СС-связи, например, превращение пировиноградной кислоты в щавелевоуксусную или пропионилкофермента А в метилмалонилкофермент А, основана на биотине (витамин Н), в состав которого входит тиолановый гетероцикл:
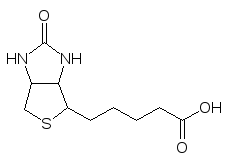
Ещё два кофермента с тиольными группами 2‑меркапто-этансульфокислота (кофермент М) и фосфат N-ω-меркаптогептаноил-треонина (кофермент В) принимают участие в образовании метана анаэробными метанобразующими бактериями:
-
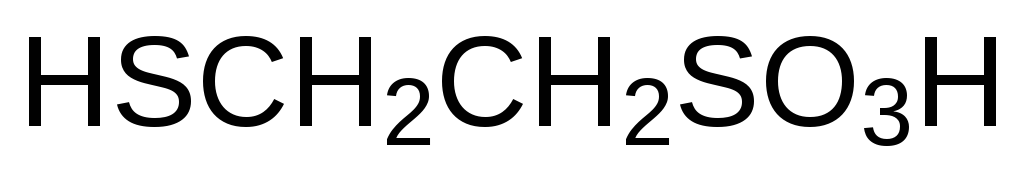
и
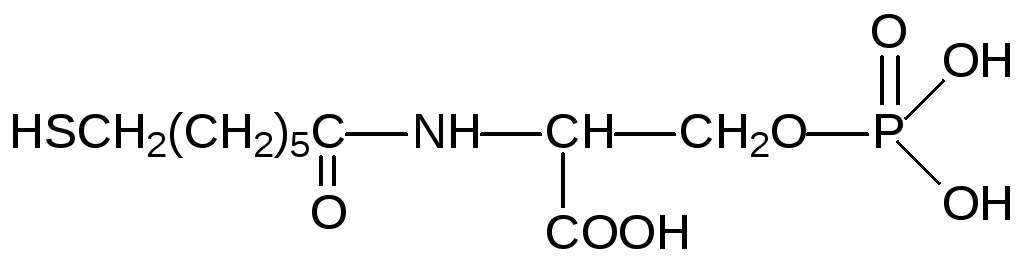
2-Меркаптоэтансульфокислота используется в качестве лекарственного средства Месна (стр. ).
Важную роль в обеспечении нормального функционирования клеток организма играет глютатион — γ-глютамил-цистеинил-глицин:
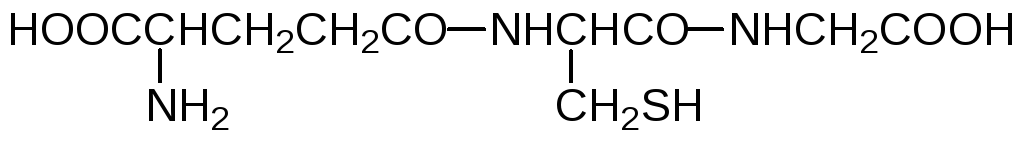
В молекуле этого необычного трипептида глютаминовая кислота участвует γ-карбоксильной группой. В биохимии его обозначают GSH, где SH – это участвующая в превращениях глютатиона сульфгидрильная группа. Многие бактерии, все грибы, растения и животные могут синтезировать глютатион из глютаминовой кислоты, цистеина и глицина в двухстадийном процессе с участием двух молекул аденозинтрифосфата (АТФ, АТР), при этом скорость его образования лимитируется содержанием в цитозоле свободного цистеина. Глютатион является главным антиоксидантом в водных средах и регулятором окислительно-восстановительных процессов. Окисление глютатиона активными формами кислорода протекает по сульфгидрильной группе с образованием дегидроглютатиона GSSG с дисульфидной связью. Фермент глютатионредуктаза с участием NADH восстанавливает дисульфидную связь в этом соединении, регенерируя GSH. Повышенное содержание в биологических средах организма дегидроглютатиона свидетельствует о наличии оксидативного стресса.