Материал: сера и селен дом
![]()
Ароматические соединения с гидроксильными и аминными группами реагируют с роданом (тиоцианогеном) с замещением атома водорода в пара- или орто-положении на роданогруппу, при этом 2-аминороданиды могут циклизоваться с образованием тиазольного цикла:
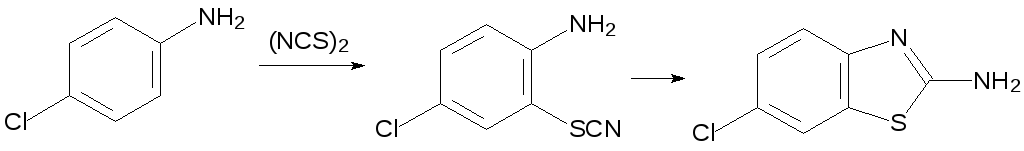
Более универсальный способ введения тиоцианатных групп в ароматические соединения представлен реакцией солей диазония с неорганическими роданидами в присутствии роданида меди или медного порошка (реакция Зандмейера).
К соединениям с двухвалентным атомом серы могут быть также отнесены тиокетоны и тиоэфиры с тиокарбонильными функциональными группами. Основной способ их получения представлен обменной реакцией соответствующих кислородных производных с декасульфидом фосфора Р4S10 или продуктом его взаимодействия с анизолом - реактивом Лоусона (S.-O. Lowesson), например:
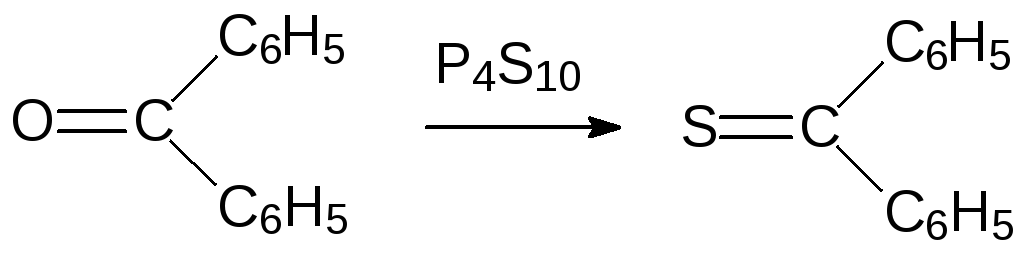
Многие тиокарбонильные соединения отличаются высокой реакционной способностью и интенсивно окрашены. Это связано со спецификой связывающей атомы серы и углерода двойной связи (π-связи), которая образована различающимися по размерам орбиталями 2р электронов атома углерода и 3р электронов атома серы. Геометрия этих орбиталей не обеспечивает достаточно плотного их перекрывания.
В соответствии с этим тиокарбонильные соединения легко вступают в различные превращения, одним из которых является перегруппировка Ньюмена-Кворта (M. S. Newman, H. Kwart, 1965-1966). При температуре около 300 °С в инертной атмосфере О‑ариловые эфиры тиокарбаминовых кислот претерпевают внутримолекулярную перегруппировку и превращаются в соответствующие S-ариловые эфиры:
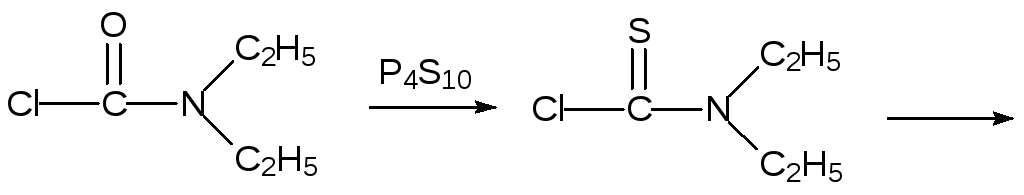
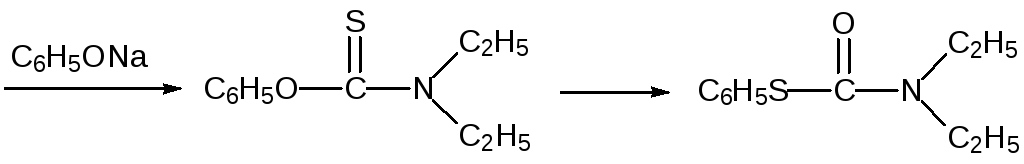
Это превращение имеет определенное значение как один из способов получения тиофенолов (после гидролиза тиокарбаматов).
В тион-тиольные перегруппировки вступают также эфиры дитиоугольной кислоты (ксантогенаты) и О-эфиры тиокарбоновых кислот (перегруппировка Шёнберга, A. Schönberg, 1930).
Сульфоксиды
Первичными продуктами окисления тиоэфиров являются сульфоксиды. В качестве окислителей тиоэфиров может использоваться пероксид водорода в кислой среде, элементный иод и другие окислители. Многотоннажное производство диметилсульфоксида основано на окислении азотной кислотой диметилсульфида – побочного продукта целлюлозно-бумажной промышленности.
Сульфоксиды ароматического ряда могут быть получены по реакции соответствующих ароматических соединений с диоксидом серы при катализе кислотами Льюиса или сильными кислотами:
![]()
Сульфоксиды имеют пирамидальное строение и поэтому сульфиды с разными заместителями у атома серы прохиральны – их окисление в сульфоксиды приводит к образованию рацемической смеси пространственных изомеров, которую можно разделить на стереомеры, так как рацемизация их при комнатной температуре идёт очень медленно. Так, например, одним из лекарственных препаратов с сульфоксидной функциональной группой является нейролептик модафинил:
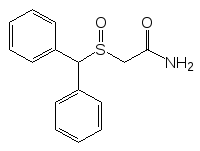
Его применяют для лечения сонливости и в качестве мягкого психостимулятора. При этом оказалось, что R-изомер модафинила (армодафинил) заметно превосходит по активности рацемическую смесь изомеров. Правда, во многих странах модафинил внесен в список потенциальных наркотических средств и запрещен ВАДА к использованию спортсменами.
Сульфоксидная функциональная группа содержится также в молекулах средств для лечения язвы желудки омепразола и лансопразола, действие которых основано на ингибировании протонного насоса (К+,Н+-АТФазы), генерирующего кислотную среду в желудке. И в этом случае более эффективным оказался один из пространственных изомеров омепразола по сульфоксидной группе (S-изомер, эзомепразол):
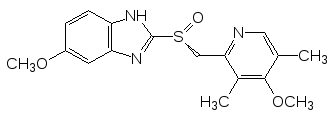
Высокая полярность сульфоксидной группы и пирамидальная структура молекулы делают сульфоксиды хорошими лигандами для комплексообразования. В соответствии с этим диметилсульфоксид является одним из самых распространенных апротонных полярных растворителей в лабораторной практике. Он менее токсичен, чем другие высокополярные растворители (диметилформамид, гексаметапол и др.).
Полярные апротонные растворители специфически сольватируют катионы, вследствие чего реакции нуклеофильного замещения металлированных производных протекают в них на несколько порядков быстрее, чем в протонных растворителях, снижающих реакционную способность нуклеофильного реагента в результате образования водородных связей.
Под названием димексид диметилсульфоксид используется в фармакологии в качестве местного противовоспалительного и обезболивающего средства. Его вводят также в состав лекарственных средств, предназначенных для трансдермального введения активных начал. В смеси с водой в концентрации от 10 до 50 % он значительно ускоряет поступление лекарств через кожу.
При использовании диметилсульфоксида в качестве растворителя надо учитывать достаточно высокую реакционную способность этого вещества. Так, например, диметилсульфоксид может выступать в роли окислителя. В реакции с первичными алкилгалогенидами или сульфонатами он образует сульфоксониевые соли, которые разлагаются действием третичных аминов на альдегид и диметилсульфид (реакция Корнблюма), а п‑толилсульфонат (тозилат) вторичного спирта в реакции с диметилсульфоксидом и триэтиламином превращается в кетон:
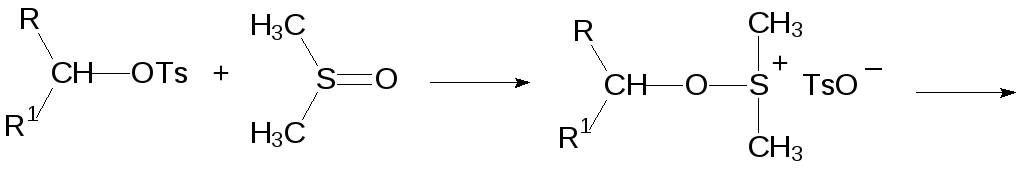
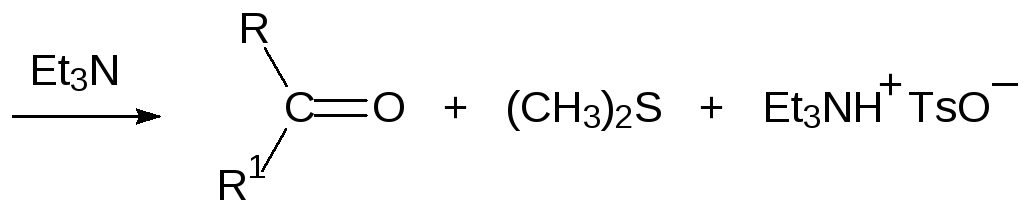
Ещё один способ превращения первичных и вторичных спиртов в альдегиды и кетоны представлен окислением по Сверну. В этом случае диметилсульфоксид реагирует с оксалилхлоридом с образованием хлорида диметилхлорсульфония, который далее в присутствии основания реагирует со спиртом по схеме:
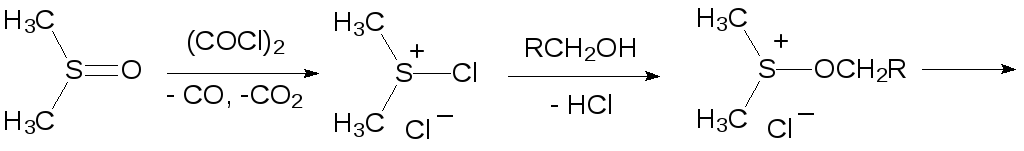
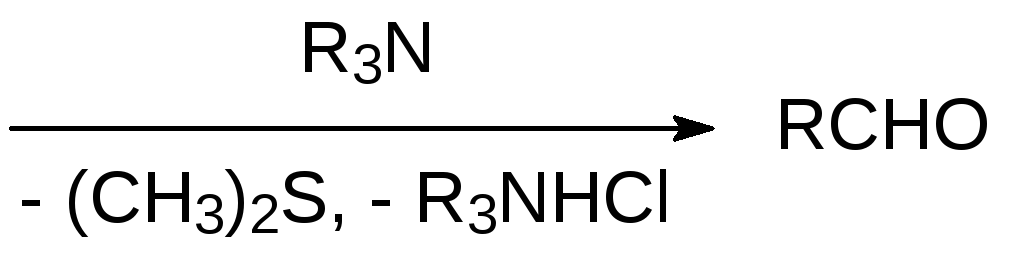
Окислительным превращением алкильного остатка в хлорформиатах сопровождается их реакция с диметилсульфоксидом в присутствии оснований:
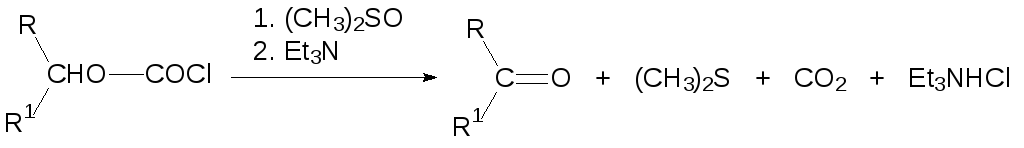
Диметилсульфоксид реагирует также с другими ацилирующими реагентами. При этом атом серы восстанавливается, а в одной из связанных с атомом серы алкильных групп повышается степень окисления. В качестве примера приводится реакция метилэтилсульфоксида с уксусным ангидридом (R. Pummerer, 1909), в результате которой происходит окислительное превращение связанной с атомом серы этильной группы, протекающее с образованием ацетильного производного S‑метилполутиоацеталя:
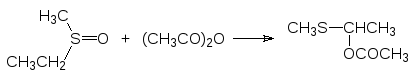
С гидридом натрия диметилсульфоксид реагирует с выделением водорода:
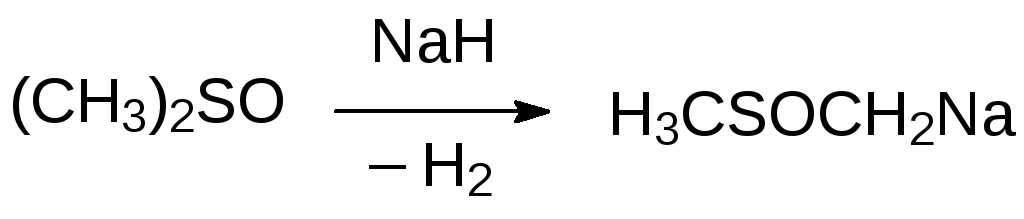
Образующийся при этом димсилнатрий можно использовать в качестве сильного основания в гомогенной среде.
Диметилсульфоксид нельзя использовать в качестве растворителя при проведении реакций с участием первичных аминов, так как он реагирует с ними с образованием сульфимидов:
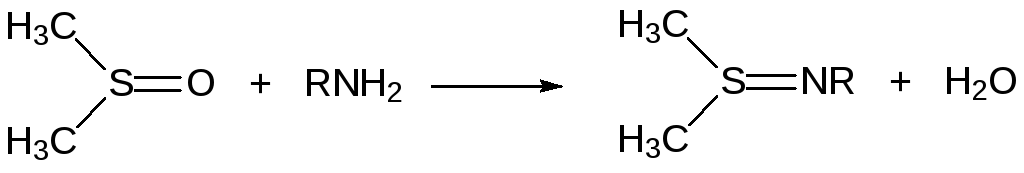
В реакции сульфоксидов с алкилаторами образуются соли сульфоксония. Так, например, метилиодид переводит диметилсульфоксид в иодид триметилсульфоксония:
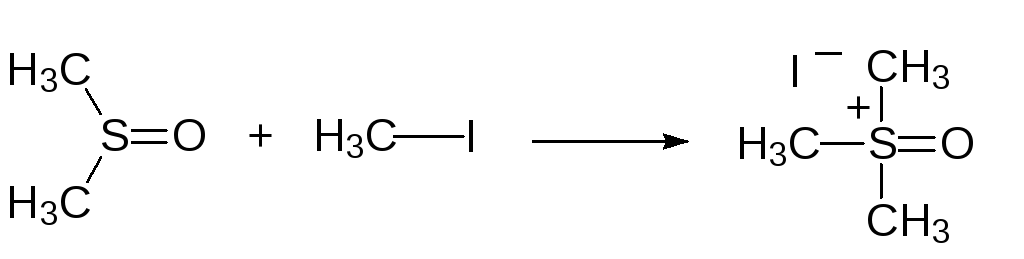
Важная область применения образующихся при алкилировании тиоэфиров и сульфоксидов сульфониевых и сульфоксониевых солей представлена реакциями, известными как реакции Джонсона-Кори-Чайковски (Johnson-Corey-Chaykovsky) или реакции Кори-Чайковски. При действии сильных оснований на соли сульфония и, соответственно, сульфоксония они превращаются в илидные соединения:
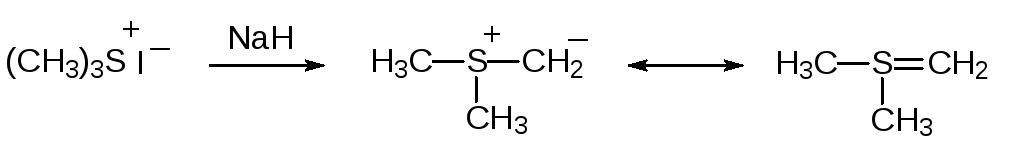
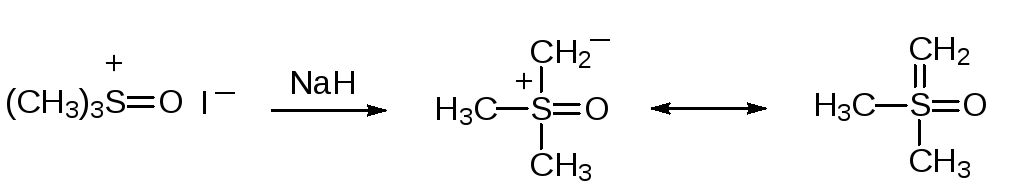
Диметилсульфид и диметилсульфоксид являются хорошими уходящими группами, и поэтому в реакциях с непредельными соединениями илиды на основе серы встраивают алкилиденовые группы по двойным связям с образованием трёхчленных циклов. При этом метилид диметилсульфония используется преимущественно для получения оксиранов (эпоксидов). Так, например, в производстве эффективного триазольного фунгицида тебуконазола на предпоследней стадии получают эпоксидное соединение действием на 2‑(4-хлорфенил)этилтретбутилкетон метилида диметилсульфония, образующегося из бромида триметилсульфония и третбутилата калия:
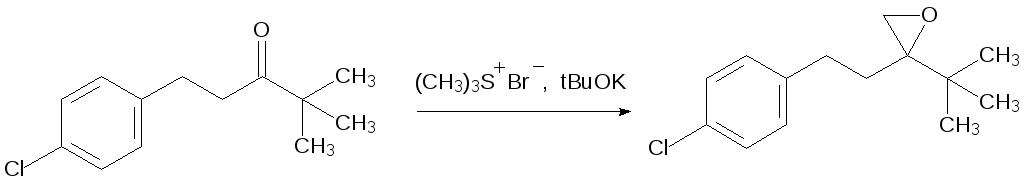
Далее полученное соединение реагирует с триазолятом натрия с раскрытием оксиранового цикла.
В смеси диметилсульфоксида с тетрагидрофураном метилид диметилсульфоксония, полученный из иодида триметилсульфоксония и гидрида натрия, реагирует преимущественно с этиленовыми двойными связями с образованием циклопропанового структурного элемента, например:
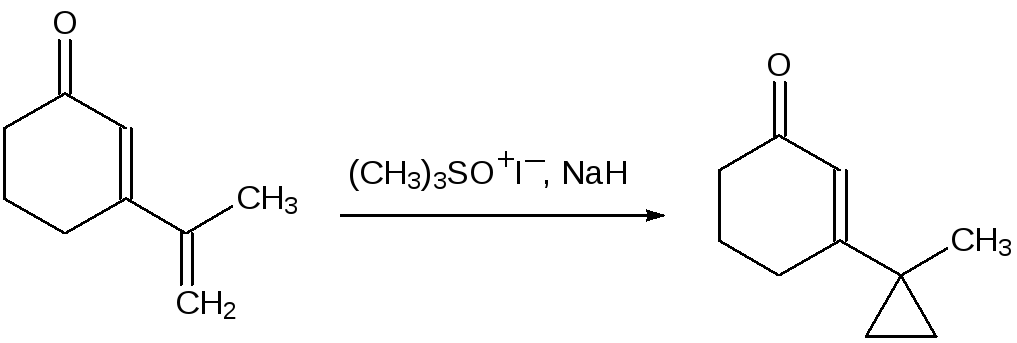
Если в реакции циклопропанирования должен участвовать алкилиденовый фрагмент, отличный от метиленовой группы, реакцию проводят с илидом, образующимся из галогенида алкилдифенилсульфоксония или алкилдифенилсульфония. Так, например, один из способов получения эфира хризантемовой кислоты, используемой для получения пиретроидных инсектицидов, включает взаимодействие изопропилида дифенилсульфоксония с эфиром 5-метилгекса-2,4-диеновой кислоты:
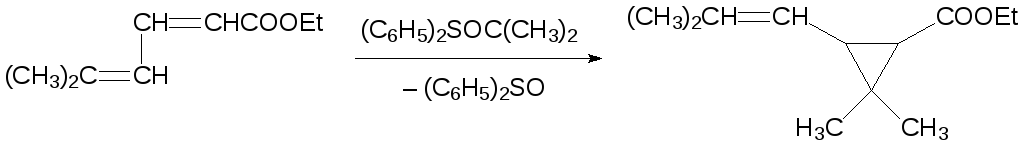
Вторым продуктом этой реакции становится дифенилсульфоксид, который можно возвращать в процесс для получения изопропилида дифенилсульфоксония.
Метилид диметилсульфоксония реагирует также с оксиранами. Так, например, глицидиловые эфиры реагируют с ним с образованием алкоксиоксетанов. В третбутаноле при температуре 50 °С эта реакция протекает в течение времени около 4 суток:
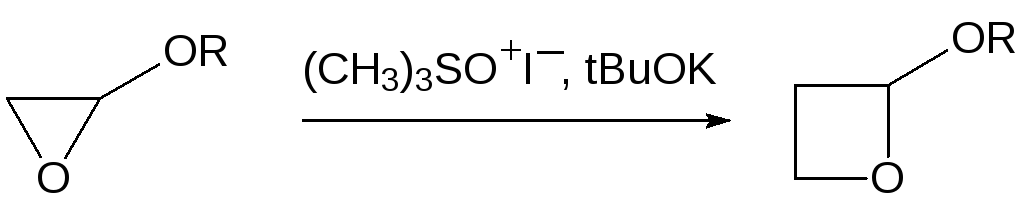
По аналогичной схеме можно переводить азиридины в азетидины.
Сульфеновые кислоты
Промежуточные продукты в реакции окисления тиолов сульфеновые кислоты общей формулы RSOH неустойчивы, они легко окисляются и восстанавливаются. В водных растворах сульфеновые кислоты диспропорционируются с образованием тиоэфиров сульфиновых кислот:
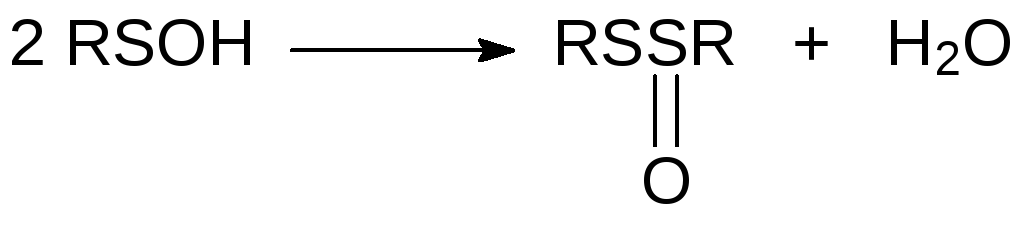
Для получения сульфеновых кислот используют реакции термического разложения сульфоксидов с третичным атомом углерода у атома серы. Так, например, алкилтретбутилсульфоксид разлагается с образованием алкансульфеновой кислоты и изобутена уже при температуре 80-100 °С в соответствии со схемой:
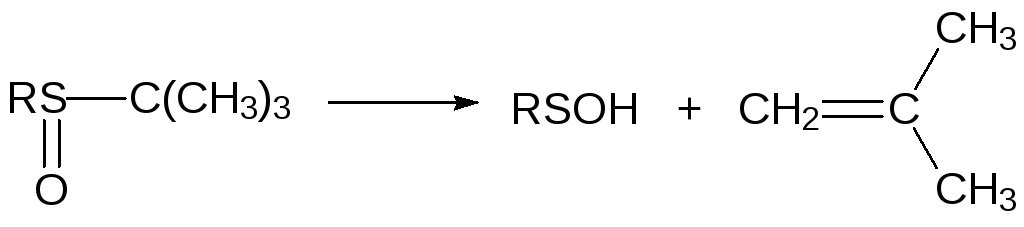
Более известны хлорангидриды сульфеновых кислот, которые могут быть получены селективным хлорированием дисульфидов:
![]()
Сульфенхлориды также можно перевести в сульфеновые кислоты через их эфиры, гидролизующиеся щелочами с образованием достаточно устойчивых солей:
![]()
Сульфенхлоридом является очень токсичный перхлорметилмеркаптан, образующийся из сероуглерода при хлорировании его в присутствии иода:
![]()
Его используют для получения фунгицидного средства для обработки плодовых растений и протравителя фолпета (фталана), образующегося в реакции фталимида с перхлометилмеркаптаном:
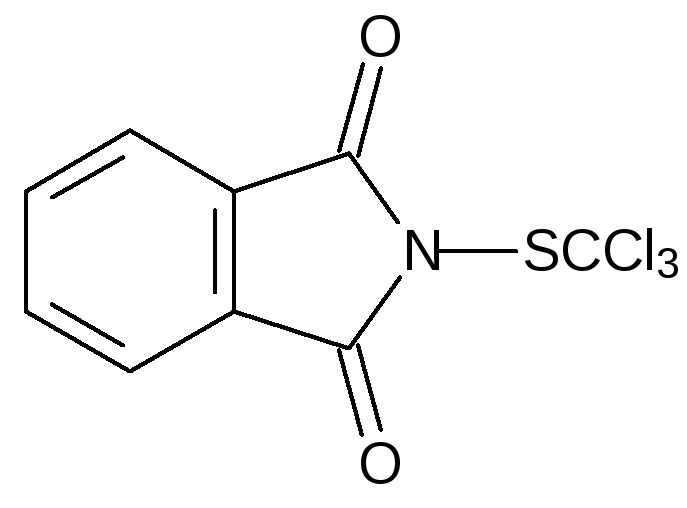
Восстановлением перхлорметилмеркаптана дихлоридом олова или металлическим цинком получают дихлорангидрид тиоугольной кислоты (тиофосген) CSCl2. Эта очень токсичная жидкость оранжевого цвета, разлагающееся на воздухе с образованием оксидов серы и хлористого водорода, может быть использована для синтеза тиокарбаматных пестицидов. При хранении тиофосген димеризуется с образованием стабильного бесцветного кристаллического соединения.
Алкилирование солей сульфеновых кислот подчиняется правилу Пирсона. При действии мягких электрофилов из них образуются сульфоксиды:
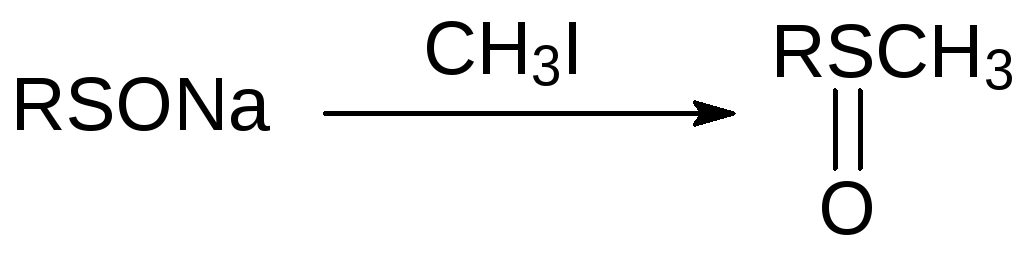
Алкилирование сульфенатов генераторами жестких карбокатионов приводит к образованию эфиров сульфеновых кислот.
Сульфеновые кислоты присоединяются к активированным двойным связям с образованием сульфоксидов, например:
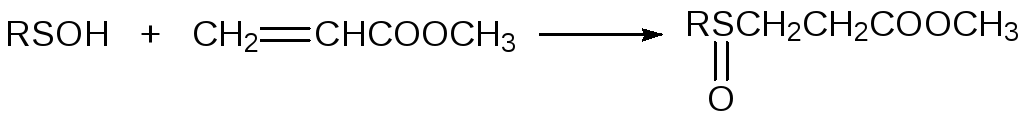
Сульфеновые кислоты находят ограниченное применение в качестве добавок к смазочным маслам и исходных продуктов в синтезе лекарственных препаратов и пестицидов.
Сульфиновые кислоты
Сульфиновые кислоты представляют собой одноосновные кислоты общей формулы
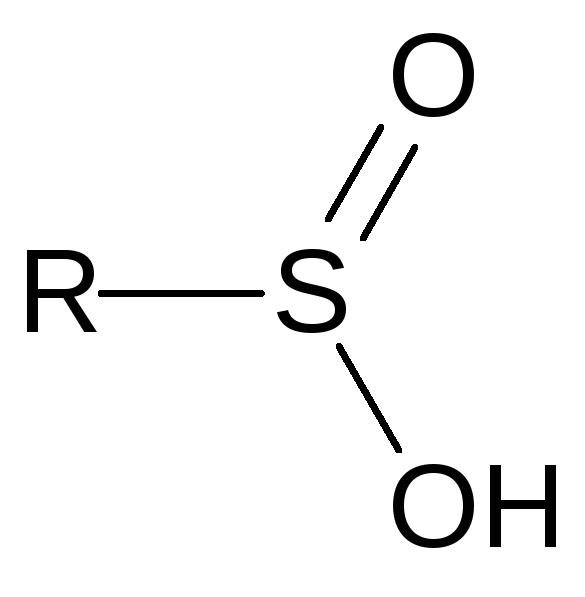
Атом серы в этом состоянии окисления, как и у сульфоксидов, имеет пирамидальное строение, но из-за лёгкости перехода протона от одного атома кислорода к другому хиральными являются только производные сульфиновых кислот с замещенными гидроксильными группами.