Материал: сера и селен дом
Органические производные элементов шестой группы
Элементоорганические соединения элементов шестой группы Периодической системы Д.И.Менделеева представлены производными серы, селена и теллура. В шестую группу входит еще и кислород, но валентные электроны его электронной оболочки находятся на втором уровне, что исключает использование атомом кислорода d-орбиталей, и поэтому кислород, принимая два электрона, образует только две связи, что отличает его от других элементов шестой группы. Есть, конечно, аналогии в соединениях двухвалентных кислорода, серы и селена. Так, например, спиртам (R−OH) соответствуют тиолы и селенолы (R−SH и R−SeH), простым эфирам (R−O−R) — сульфиды и селениды (R−S−R и R−Se−R), кетонам (О=CR2) — тиокетоны и селенокетоны (S=СR2 и Se=CR2), пероксидам (R−OO−R) — дисульфиды и диселениды (R−SS−R и R−SeSe−R), где R представляет собой радикал, связанный с гетероатомом через атом углерода.
Строение валентных оболочек атомов элементов шестой группы определяет различия в свойствах спиртов, тиолов и селенолов. Так, например, тиолы представляют собой более сильные кислоты, чем спирты, поскольку SH‑связь слабее OH‑связи, и в более объёмном атоме серы лучше распределяется образующийся в результате ухода протона отрицательный заряд. По этой же причине и селенолы являются более сильными кислотами, чем тиолы. Кроме того, гидроксильные группы образуют более прочные водородные связи, чем тиольные группы. Следствием этого становится более высокая температура кипения спиртов в сравнении с аналогичными тиолами (78,4 °С для этанола и, соответственно, 35 °С для этантиола).
И всё же главное отличие атомов серы и селена от атомов кислорода состоит в их способности к образованию соединений, в которых эти элементы находятся в окисленном состоянии с более высокими значениями валентности. В качестве примера можно привести сульфоксиды (R2SO), сульфоны (R2SO2), сульфиновые кислоты (RS(O)OH), сульфокислоты (RSO2OH) и др. Аналогичные соединения образует и селен. Эти соединения с более высокой валентностью атомов серы и селена стабилизированы связыванием с участием 3d (или 4d) орбиталей и увеличенным по сравнению с атомом кислорода размером атомов серы и селена. Селен образует более длинные и более слабые легко поляризуемые связи, что определяет различие в реакционной способности и в свойствах органических производных серы и селенорганических соединений.
Сера и селен играют важную роль в биохимических превращениях, выступая в качестве функциональных групп в активных центрах ферментов и коферментов. Они входят также в состав белковых аминокислот. Синтетические селенорганические соединения демонстрируют интересные виды биологической активности. Опыты по синтезу их структурных аналогов с атомами теллура с целью получения ещё более активных соединений не увенчались успехом. У теллурорганических соединений шире индекс безопасности, но попадающие в организм соединения теллура включаются в обменные процессы вместе с соединениями серы и селена и в течение длительного времени остаются в составе белков и других биополимеров. Из организма теллур выводится в основном через потовые железы и легкие в виде летучего диметилтеллурида с отвратительным запахом, напоминающим чесночный. Известно, например, что люди, в организм которых поступало однократно всего лишь около 15 мг теллура, источали зловоние в течение более полугода. Соединения теллура легко проникают через кожу, поэтому работать даже с элементным теллуром можно только в изолирующих боксах в специальных перчатках. Всё это делает бесперспективным изучение синтетических возможностей и биологической активности теллурорганических соединений.
Органические производные серы
В учебной литературе по органической химии достаточно много внимания уделяется химии органических производных серы, представленных в основном сульфокислотами и тиолами (меркаптанами). Есть также многочисленные монографии, в которых детально рассматриваются способы получения и свойства других органических соединений с атомами серы. В качестве примера можно привести работы Оаэ Сигеру, «Химия органических соединений серы», 1975 г., 512 с., и «Химия органических соединений серы» под ред. Л. И. Беленького, 1988 г., 320 с., включающей даже такие разделы, как исследование органических реакций с помощью соединений радиоактивной серы, квантово-химические расчеты молекул с атомами серы и др., однако те, кто специализируется в области химии биологически активных соединений, вряд ли обратятся к этим всеобъемлющим и малодоступным монографиям.
Большое практическое и теоретическое значение имеют производные тиофена, тиазола, тиадиазола, фенотиазина и других серосодержащих гетероароматических соединений. В молекулах этих гетероциклов электроны атома серы включены в ароматические системы и в связи с этим изучение таких веществ относится, конечно же, к специальным разделам химии ароматических соединений.
В серосодержащих органических соединениях, как и в неорганических, степень окисления серы составляет от –2 до +6. Это подразумевает большое разнообразие элементорганических соединений с атомом серы, однако в практическом отношении наибольший интерес представляют
тиолы R-SH
сульфиды R-S-R
дисульфиды R-S-S-R
сульфоксиды R-SO-R
сульфеновые кислоты R-SOН
сульфиновые кислоты R-SO2Н
сульфоновые кислоты R-SO2OH
сульфоны R-SO2-R
Особенность
номенклатуры сероорганических соединений
состоит в том, что в основе названия
соединения с одной SС-связью
лежит углеводород или его производное,
например, СН3SН
– метантиол, СН3С6Н4SО3Н
– толуолсульфокислота, а в названия
соединений с двумя SС-связями
органические остатки входят как радикалы:
СН3SСН3
– диметилсульфид. Часто названия
сероорганических соединений образуются
из названий соответствующих кислородных
производных с префиксом тио,
например, это тиокислоты, тиоэфиры,
тиофенол, тиоанизол и т.д. Префикс тио
используется также для названий аналогов
кислородсодержащих соединений с атомами
серы, для которых другие варианты были
бы слишком сложными. Например, это
окрашенные в цвета от жёлтого до синего
тиокетоны R2C=S,
тиокислоты RCSOH и тиоэфиры RC(S)OR' и RC(O)SR'
(О- и S-эфиры тиокарбоновых кислот).
Для циклических соединений с атомом серы используются названия:
![]()
![]()
![]()
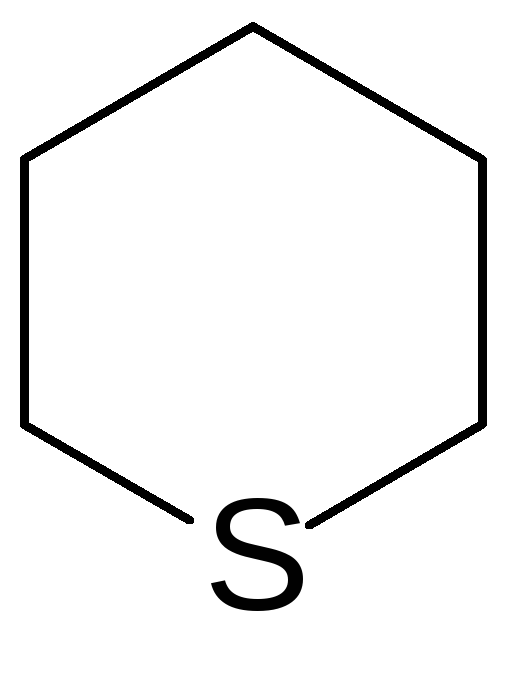
Тииран Тиетан Тиолан Тиан
Соединения двухвалентной серы
Тиолы, называющиеся также меркаптанами (от лат. mercurium captans — связывающие ртуть), представляют собой тиоаналоги спиртов. В природе встречается достаточно много тиольных соединений. Одна из белковых аминокислот цистеин представляет собой меркаптоаланин НSСН2СН(NН2)СООН, цистеин входит также в состав трипептида глютатиона (γ-Glu-Cys-Gly). Кофермент А представляет собой ацилированный по атому азота тиоэтаноламин (цистеамин), а бутантиол является одной из дурно пахнущих компонент секрета, выделяющегося при опасности из специальных желез скунса. Неприятный запах меркаптанов распознается в очень низких концентрациях (10-7-10-8 моль/л). Поэтому этилмеркаптан и третбутилмеркаптан используют для одорирования подаваемого в жилые помещения природного газа для того, чтобы можно было обнаружить его утечку. Однако в низкой концентрации некоторые тиолы могут иметь и приятный запах, в частности, в состав ароматических веществ жареного кофе входит фурфурилтиол, а следовые концентрации 4‑меркапто-4-метилпентан-2-она придают характерный аромат винам сорта Совиньон.
Способы получения тиольных соединений включают прямое алкилирование гидросульфидов щелочных металлов алкилгалогенидами, диалкилсульфатами или алкилсульфонатами. Так, например, из диметилсульфата и гидросульфида натрия можно получать метантиол:
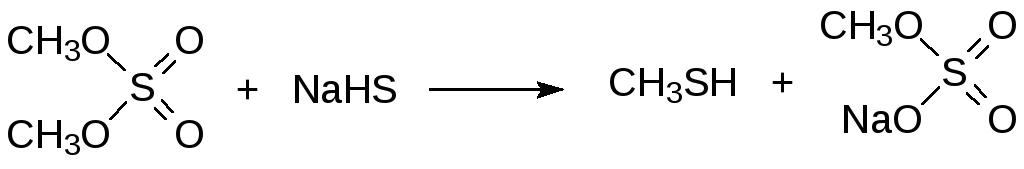
Эта реакция сопровождается образованием значительного количества диметилсульфида в результате алкилирования диметилсульфатом соли образовавшегося метилмеркаптана:
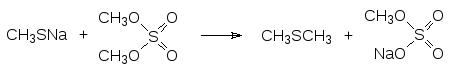
Более избирательно протекает образование меркаптанов в двухстадийном процессе, когда на первой стадии проводят алкилирование тиосульфата:
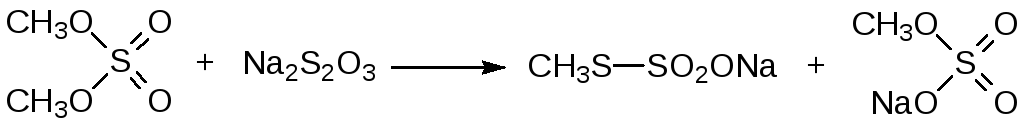
Полученные соли моноэфиров тиосерной кислоты (их иногда называют солями Бунте) гидролизуются в присутствии кислот с образованием алкантиолов:
![]()
Аналогичный способ получения тиолов представлен алкилированием и последующим гидролизом моноэфиров дитиоугольной кислоты (ксантогенатов), образующихся по реакции алкоголятов с сероуглеродом:
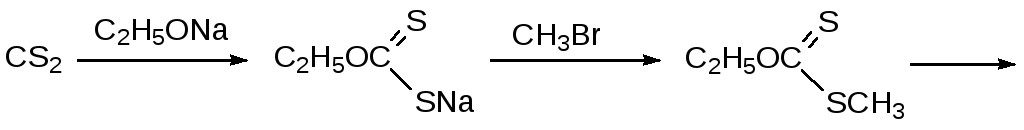
![]()
Побочным продуктом этой реакции становится серооксид углерода, представляющий собой очень токсичный и легко воспламеняющийся газ.
Тиолы образуются также при щелочном гидролизе тиурониевых солей, которые получаются при алкилировании тиомочевины алкилгалогенидами:
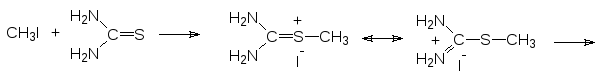
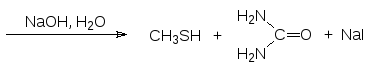
Однако промышленное производство метантиола, используемого, в частности, в производстве аминокислоты метионина, основано на алкилировании сероводорода метанолом в газовой фазе при катализе оксидом алюминия при температуре 300-350 °С:
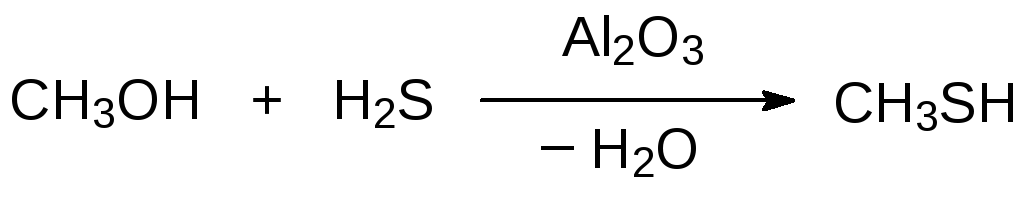
Тиольные соединения образуются также в результате присоединения сероводорода к двойным связям олефинов. В присутствии генераторов свободных радикалов или при облучении УФ светом присоединение протекает против правила Марковникова. Так, например, в кварцевом реакторе гидрохлорид аллиламина реагирует с избытком сероводорода в спиртовой среде в свете ртутной лампы с образованием гидрохлорида 3‑меркаптопропиламина:
![]()
Олефины, легко образующие карбокатионы, присоединяют сероводород в присутствии кислот:
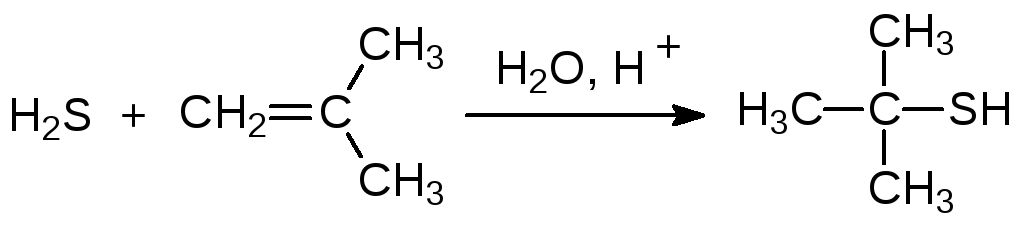
Побочными продуктами в реакциях присоединения сероводорода к олефиновым соединениям являются соответствующие тиоэфиры, а при недостатке сероводорода это направление реакции становится основным.
Против правила Марковникова в присутствии оснований сероводород и тиолы присоединяются к активированным электроноакцепторными группами двойным связям. В частности, так из метилмеркаптана и акролеина при катализе третичным амином в промышленном масштабе получают 3‑метилтиопропионовый альдегид (метиональ) – промежуточный продукт в производстве D,L‑метионина:
![]()
Интересно, что при катализе ацетатом меди выход целевого продукта в этой реакции может достигать 97 %.
На этой реакции основано, очевидно, и уменьшение побочного токсического действия циклофосфамида и ифосфамида лекарственным средством на основе 2-меркаптоэтансульфокислоты (Месна):
![]()
Этот препарат принимают при химиотерапии онкологических заболеваний циклофосфамидом и ифосфамидом. Биотрансформация этих цитостатиков приводит к образованию акролеина, оказывающего токсический эффект на ткани мочевого пузыря и почек. Сопровождение лечения этими препаратами приёмом Месны значительно снижает риск геморрагического цистита и гематурии. Присоединяясь по активированной двойной связи акролеина сульфгидрильной группой по аналогии с представленным выше уравнением реакции с метантиолом Месна значительно снижает токсичность акролеина. Известно также применение Месны в качестве муколитического средства по аналогии с ацетилцистеином (АЦЦ, АСС).
Присоединение сероводорода по тройным связям протекает неселективно. Продуктами реакции становятся цис- и транс-изомеры соответствующих дивинилсульфидов.
1,3-Диацетиленовые соединения реагируют с сероводородом в слабощелочной среде с образованием тиофенов, например:
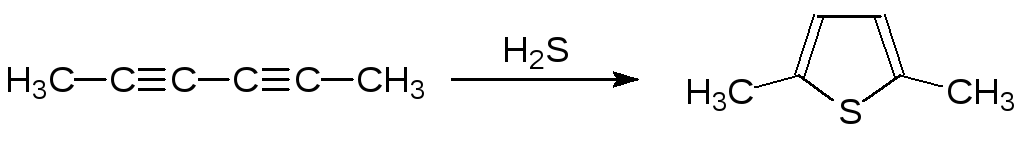
К олефиновым двойным связям присоединяются и хлориды серы. Так, например, один из способов получения 2,2´-дихлордиэтилсульфида, использовавшегося в качестве боевого отравляющего вещества под названием иприт, горчичный газ и др., представлен реакцией дихлорида серы с этиленом:
![]()
Хлорангидриды ароматических сульфокислот достаточно устойчивы в кислых водных средах при комнатной температуре. В соответствии с этим их можно использовать для синтеза тиолов ароматического ряда (тиофенолов) восстановлением цинком в соляной кислоте:
![]()
Еще один способ получения тиофенолов основан на реакции солей арилдиазония с гидросульфидом натрия, например:
![]()
Побочным продуктом в этой реакции становится дифенилсульфид, образующийся в результате взаимодействия соли диазония с первичным продуктом реакции тиофенолом. Более избирательный способ получения тиофенолов основан на реакции солей диазония с ксантогенатами. Продуктами этой реакции становятся S‑ариловые эфиры О-алкил-дитиоугольных кислот, которые, как это было представлено выше в схеме получения алкантиолов, гидролизуются с образованием тиофенолов:
![]()
Тиольные соединения образуются также в реакциях магнийорганических соединений с элементной серой. В частности, этим способом удобно получать тиофенолы:
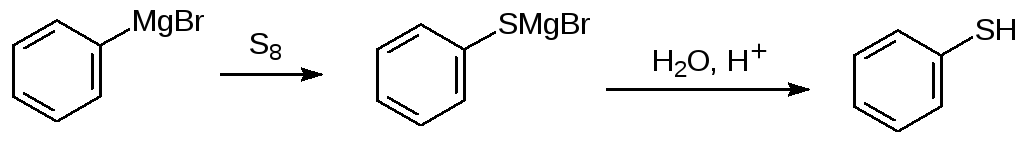
В реакцию с металлорганическими соединениями вступают дисульфиды, легко образующиеся из тиольных соединений при окислении, при этом в качестве окислителя может выступать даже кислород воздуха. В качестве примера можно привести получение несимметричных тиоэфиров в результате взаимодействия диэтилдисульфида с литийорганическим соединением:
![]()
Понятно, что образовавшуюся в качестве побочного продукта литиевую соль этантиола также можно перевести в тиоэфир действием, например, бутилбромида:
![]()
Как отмечалось выше, тиоэфиры образуются в качестве побочных продуктов при получении тиолов алкилированием и арилированием сульфидов.
При взаимодействии с алкилгалогенидами диалкилсульфиды превращаются в сульфониевые соединения:
![]()
Сульфониевые соединения переносят алкильные группы на нуклеофильные центры. Эта реакция используется живой природой для метилирования различных субстратов. В роли метилирующего средства при этом выступает S-аденозилметионин, образующийся при алкилировании метионина аденозинтрифосфатом:
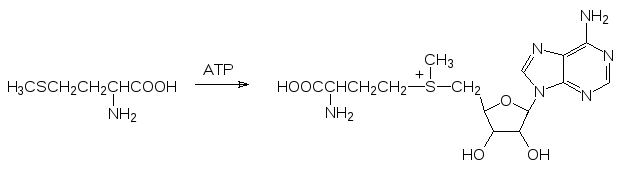
Тиольные соединения значительно легче чем спирты образуют с карбонильными соединениями тиоацетали и, соответственно, тиокетали. В качестве примера можно привести взаимодействие глюкозы с этантиолом. Карбонильная группа глюкозы участвует в образовании циклического полуацеталя (пиранозная форма глюкозы). При нагревании с метанолом в присутствии кислоты с сохранением пиранового цикла этерифицируется аномерная гидроксильная группа и образуется метилглюкозид, представляющий собой полный ацеталь, тогда как взаимодействие глюкозы с этилмеркаптаном приводит к раскрытию цикла и к образованию дитиоацеталя глюкозы линейного строения:
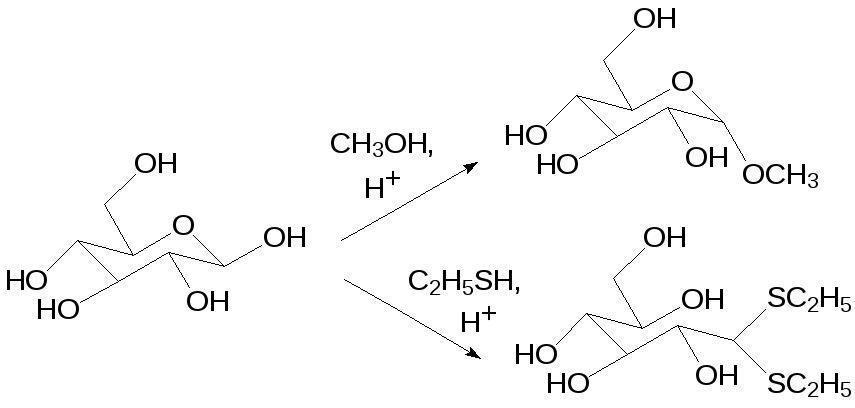
При действии оксида ртути дитиоацетали снова превращаются в карбонильные соединения, а в реакции с никелем Ренея оба атома серы в дитиоацеталях заменяются на атомы водорода. В соответствии с этим образование дитиоацеталя и последующее превращение его в реакции с никелем Ренея можно использовать для перевода карбонильной группы С=О в группу СН2.
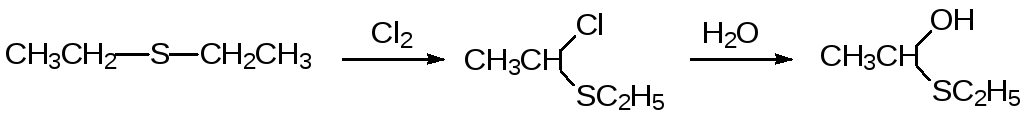
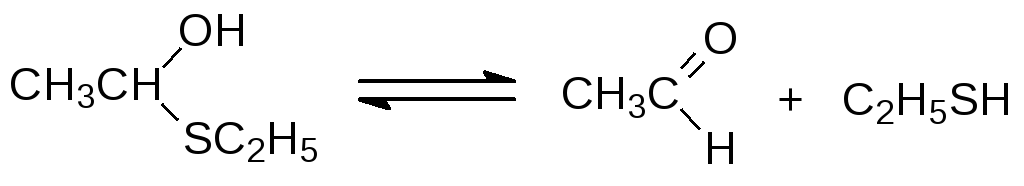
Атом серы повышает подвижность атомов водорода в соседних СН‑связях. Тиоэфиры легко хлорируются в α‑положение к атому серы. Образующиеся продукты хлорирования гидролизуются водой с образованием полутиоацеталей:
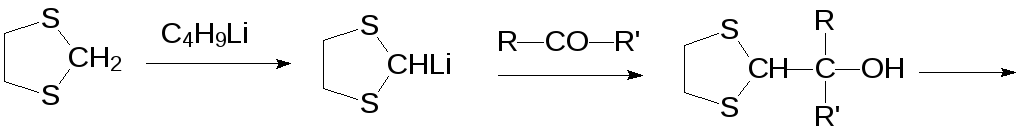
Активированные атомы водорода СН-связей в тиоэфирах могут замещаться атомами лития в реакциях, например, с бутиллитием. Эту особенность можно использовать в синтезе самых разных соединений. В качестве примера можно привести получение α‑гидроксизамещенного альдегида по схеме:
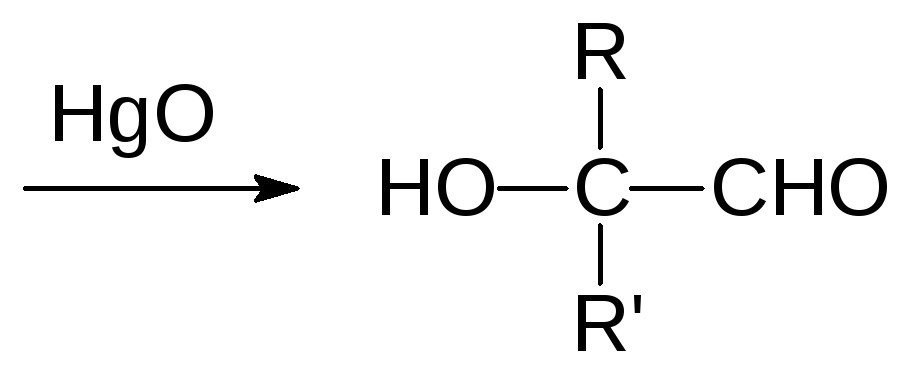
Один из способов образования СS-связи представлен реакцией неорганических роданидов с алкилгалогенидами, например:
![]()
Полученное в соответствии с представленной схемой соединение используется в качестве инсектицида Летан 384 (Регулар) с токсичностью для мышей около 90 мг/кг. При выделении органических роданидов из реакционной массы следует принимать во внимание, что при нагревании они изомеризуются в изотиоцианаты: