Материал: сера и селен дом
Свободные сульфиновые кислоты неустойчивы, особенно это относится к сульфиновым кислотам алифатического ряда. При хранении и при нагревании они диспропорционируют на сульфокислоты и S-эфиры тиосульфокислот:
![]()
В соответствии с этим сульфиновые кислоты хранят в виде солей со щелочными металлами, из которых они легко выделяются действием соляной кислоты. Ароматические сульфиновые кислоты представляют собой плохо растворимые в воде кристаллические вещества.
Основные способы получения сульфиновых кислот представлены восстановлением производных сульфокислот, превращением органических серосодержащих соединений в которых атом серы имеет ту же степень окисления +4, окислением тиольных соединений и нуклеофильным расщеплением сульфонов.
Наиболее исследованным препаративным способом получения сульфиновых кислот является реакция восстановления сульфохлоридов. При этом в качестве восстановителей могут быть использованы сульфит натрия, сульфид натрия, цинк и дихлорид олова. В реакции бензолсульфохлорида с цинковой пылью образуется цинковая соль бензолсульфиновой кислоты, которую переводят в натриевую соль действием карбоната натрия:
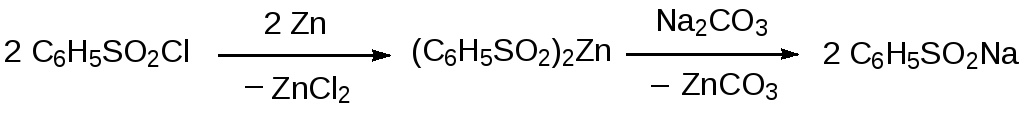
Восстановление бензолсульфохлорида сульфитом натрия протекает в соответствии с уравнением:
![]()
Металлорганические соединения, в частности, литийорганические соединения и реактивы Гриньяра, реагируют с диоксидом серы при охлаждении с образованием соответствующих солей сульфиновых кислот:
![]()
Есть также сообщения о получении сульфиновых кислот по реакции солей диазония с диоксидом серы в присутствии металлической меди или её солей.
Получение сульфиновых кислот окислением тиолов проводят действием галогенов, пероксида водорода или надкислот. При этом важно подобрать условия проведения реакции так, чтобы исключить дальнейшее окисление образующихся сульфиновых кислот до сульфокислот. Избирательным окислителем тиолов до сульфиновых кислот является м‑хлорнадбензойная кислота (mCPBA):
![]()
Ароматические сульфиновые кислоты получают с высоким выходом окислением соответствующих тиолов 30 %-ным пероксидом водорода при комнатной температуре.
Известны реакции расщепления сульфонов, протекающие с образованием сульфиновых кислот, например:
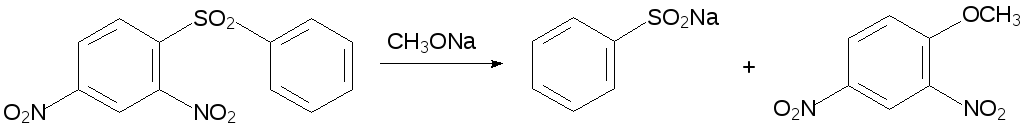
По аналогичной схеме протекает также расщепление SС-связей в сульфонах с алифатическими радикалами, содержащими электроноакцепторные функциональные группы.
Алкилирование солей сульфиновых кислот протекает по правилу Пирсона (правило ЖМКО) в соответствии с распределением электронных плотностей в сульфинатном анионе:
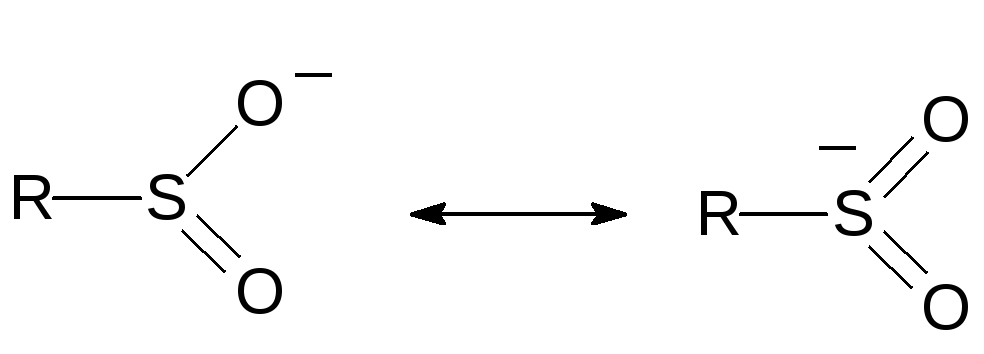
К «мягким» алкилаторам, действие которых направлено на атом серы, относятся алкилгалогениды:
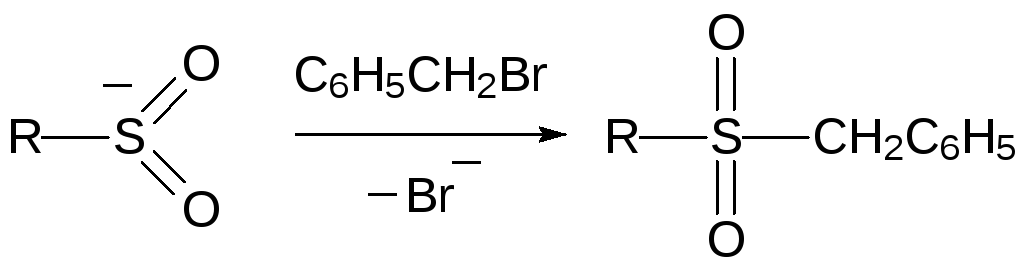
Эфиры сульфиновых кислот образуются в реакции их солей с «жесткими» акилаторами, например, с тетрафторборатом триэтилоксония (соль Меервейна):
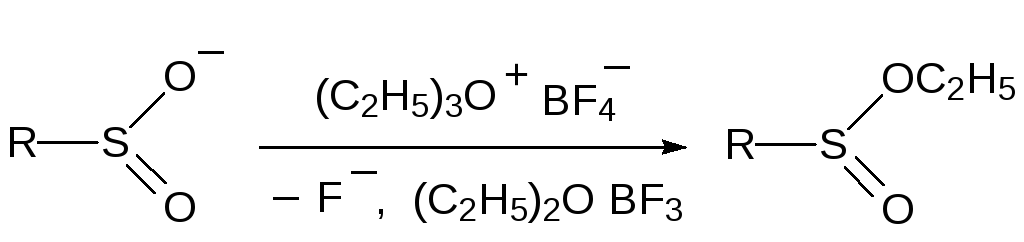
Определенное влияние на направление реакции сульфинатов с алкилаторами оказывают и растворители.
В реакции сульфинатов с оксиранами образуются β‑гидроксиалкилсульфоны:
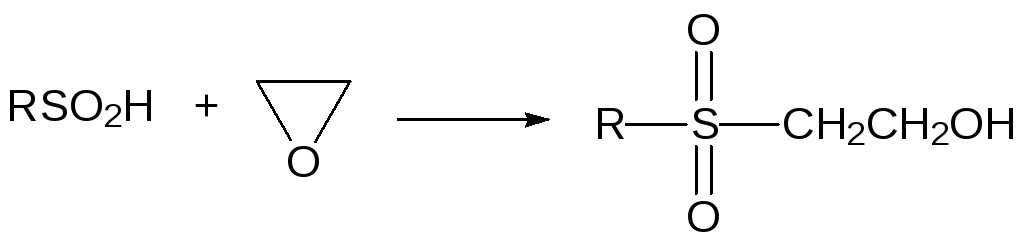
В реакции с сульфиновыми кислотами раскрываются также циклы β- и γ‑лактонов. Эти реакции протекают с образованием соответствующих карбоксиалкилсульфонов, например:
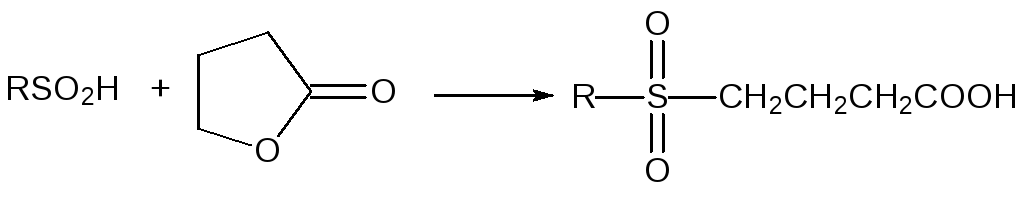
α-Гидроксизамещенные сульфоны образуются в реакции сульфиновых кислот с карбонильными соединениями:
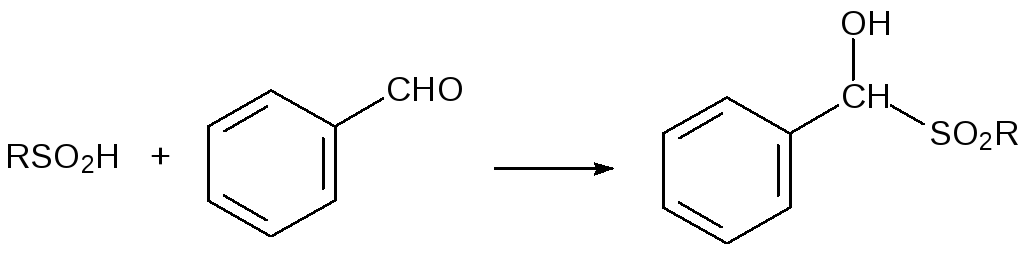
Однако широко используемый в текстильной промышленности гидроксиметилсульфинат натрия (ронгалит) получают по реакции дитионита натрия с формальдегидом:
![]()
Ронгалит используют в качестве стабильного при хранении восстановителя. Алкилирование ронгалита алкилгалогенидами приводит к образованию сульфонов, например:
![]()
По аналогии с реакцией Манниха с образованием α-аминозамещенных сульфонов протекает взаимодействие сульфиновых кислот с альдегидами в присутствии вторичных аминов:
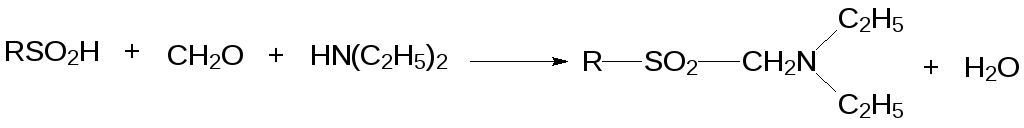
Необычный способ получения функциональной группы сульфиновой кислоты представлен реакцией пероксида водорода с тиомочевиной:
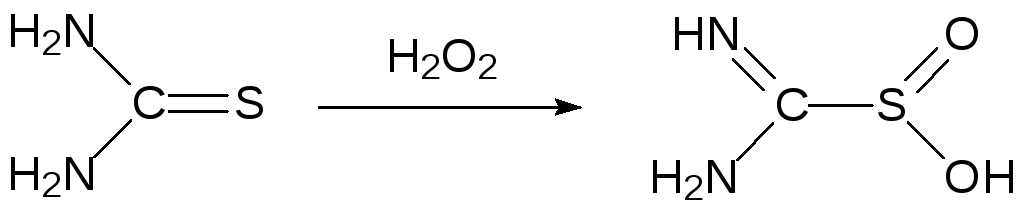
Образующуюся при этом формамидинсульфиновую кислоту называют диоксидом тиомочевины.
Ронгалит и диоксид тиомочевины используют в качестве восстановителей и отбеливателей, антиоксидантных добавок к полимерным материалам и фотосенсибилизаторов.
Сульфиновые кислоты являются хорошими восстановителями. Пероксиды, гипохлориды и даже кислород воздуха окисляют их до сульфокислот.
Получение хлорангидридов сульфиновых кислот по реакции кислот с тионилхлоридом протекает с очень низким выходом. Основной способ получения сульфинхлоридов представлен реакцией хлорирования дисульфидов в уксусном ангидриде в соответствии с уравнением:
![]()
Промежуточным продуктом в этой реакции является окрашенный в оранжевый цвет сульфенхлорид RSCl.
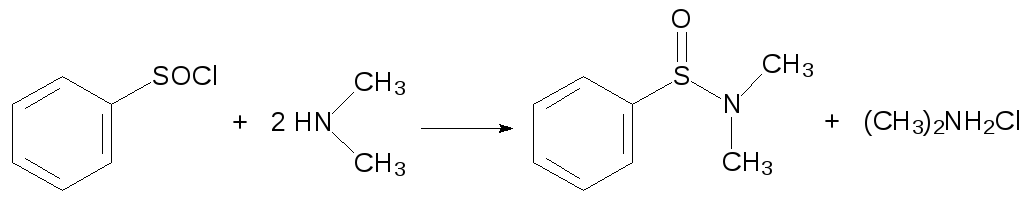
Хлорангидриды сульфиновых кислот могут быть использованы для получения их амидов, например:
Сульфиновые кислоты используют в качестве катализаторов полимеризации стирола, бутадиена и метакрилатов. В текстильной промышленности они находят применение в качестве отбеливателей и средств, улучшающих окрашиваемость натуральных и синтетических волокон. В тонком органическом синтезе их можно использовать в качестве исходных соединений для получения сульфонов.
Сульфоновые кислоты
Сульфоновым кислотам, чаще всего называемым сульфокислотами, соответствует общая формула RSO2ОH. Они представляют собой гигроскопичные кристаллические вещества с нечёткой температурой плавления.
Сульфоновые кислоты можно получать исчерпывающим окислением любых сероорганических соединений - тиолов, дисульфидов, сульфидов или даже роданидов RSCN. Однако чаще всего для их получения используют реакцию сульфирования исходных продуктов концентрированной серной кислотой или олеумом. В эту реакцию вступают соединения как алифатического, так и ароматического ряда. Сульфирование алифатических углеводородов идёт в жёстких условиях неизбирательно, но алканкарбоновые кислоты достаточно легко сульфируются в α‑положение к карбоксильной группе. Так, например, получают сульфоянтарную кислоту, используемую в качестве исходного соединения в производстве поверхностно-активных веществ:
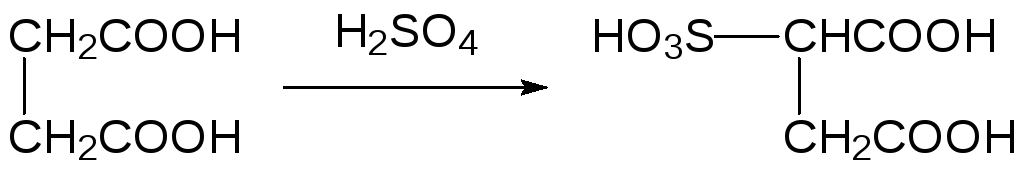
В более мягких условиях идёт сульфирование алифатических соединений хлорсульфоновой кислотой или аддуктами триоксида серы с диоксаном или пиридином, например:
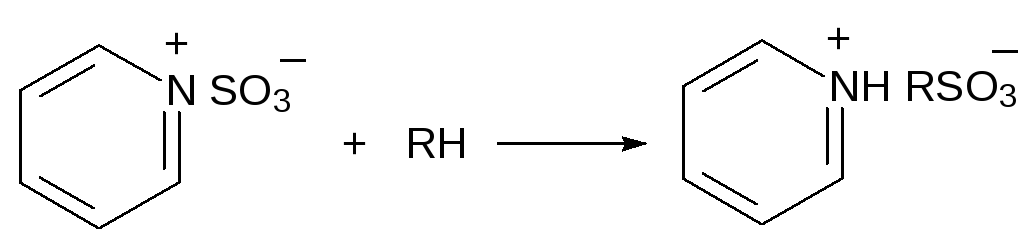
Интересно, что с помощью таких реагентов можно даже избирательно сульфировать алифатические структурные элементы в составе ароматических соединений:
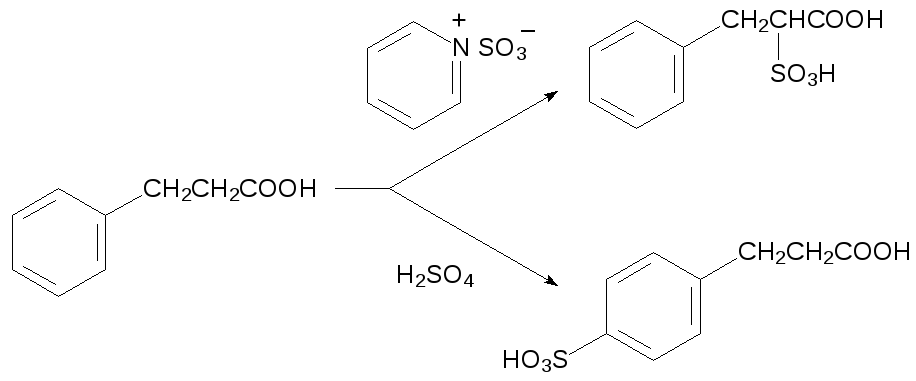
Алифатические сульфокислоты можно также получать алкилированием солей сернистой кислоты. Так, например, в реакции бисульфита калия с этиленоксидом образуется соль 2‑гидроксиэтансульфокислоты:
![]()
Ароматические соединения сульфируются значительно легче алифатических. В качестве сульфирующего реагента используются концентрированная серная кислота или олеумы с содержанием триоксида серы от 5 до 70 %. В реакции сульфирования серной кислотой выделяется вода, замедляющая или даже блокирующая замещение. Поэтому для получения сульфокислот из ароматических соединений берут большой избыток концентрированной серной кислоты или добавляют триоксид серы (олеум), реагирующий с водой с образованием серной кислоты. Можно также удалять образующуюся в реакции сульфирования воду в вакууме или азеотропной отгонкой с растворителем, который не реагирует с серной кислотой.
Скорость сульфирования и направление реакции зависят от строения реагирующего ароматического соединения. Понятно, что электронодонорные заместители значительно ускоряют реакцию сульфирования, тогда как даже такой слабый ориентант второго рода, как карбоксильная группа, значительно замедляет реакцию сульфирования. Ориентация замещения в общем случае соответствует известным правилам нуклеофильного замещения ароматических соединений, но соотношение доли замещения в орто- или пара-положения в значительной мере определяется природой сульфирующего регента, его концентрацией, температурой реакции и средой, в которой протекает реакция. Так, например, для сульфирования чувствительных к действию серной кислоты соединений можно использовать в качестве растворителей ацетонитрил, ледяную уксусную кислоту и уксусный ангидрид, жидкий диоксид серы, петролейный эфир и четырёххлористый углерод.
Ароматические сульфокислоты гидролизуются по СS-связи при нагревании с разбавленной серной или соляной кислотой при температуре до 200 °С под давлением. Эту реакцию можно использовать для введения в состав ароматического соединения функциональных групп в такие положения, в которые их нельзя ввести прямым замещением. В качестве примера можно привести получение 2,6-динитроанилина. Синтез этого вещества начинают с сульфирования хлорбензола. Полученную 4‑хлорбензолсульфокислоту нитруют, замещают атом хлора на аминогруппу и отщепляют сульфогруппу нагреванием с разбавленной соляной кислотой:
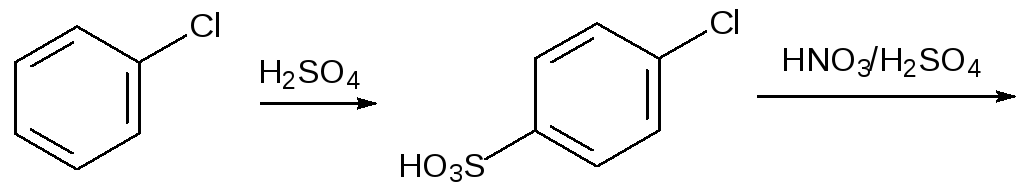
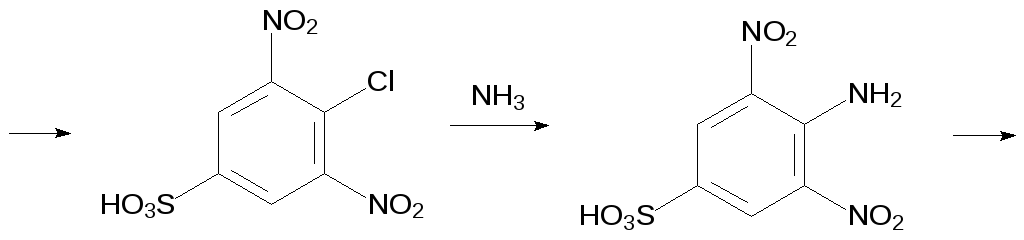
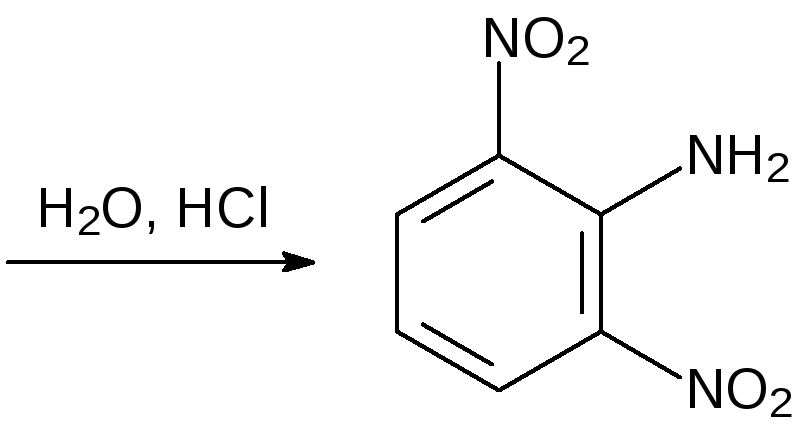
Скорость гидролитического отщепления сульфонатных групп зависит от заместителей в ароматическом кольце. В общем случае действует правило — чем легче идёт сульфирование — тем легче гидролизуется образовавшая сульфокислота. Известен, например, способ выделения м‑дихлорбензола из смеси продуктов хлорирования бензола. При сульфировании смеси о-, м- и п-дихлорбензола с самой высокой скоростью идёт образование 2,4-дихлорбензолсульфокислоты из м‑дихлорбензола. Для получения чистого мета‑изомера её отделяют от непрореагировавших орто- и пара-изомеров и гидролизуют нагреванием с соляной кислотой.
С разрывом CS-связи соли ароматических сульфокислот реагируют при сплавлении с гидроксидами щелочных металлов. Эта реакция представляет собой один из способов получения фенолов:
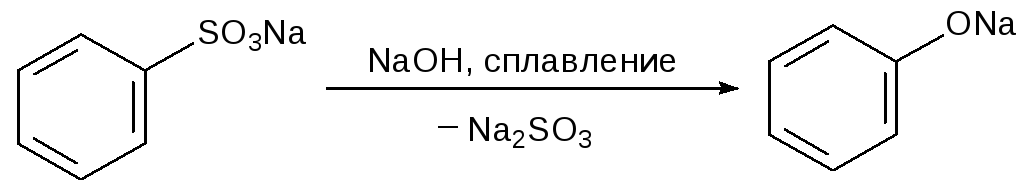
При сплавлении с цианидами щелочных металлов сульфонатная группа замещается на цианогруппу. Так, например, из образующейся при сульфировании пиридина пиридин-3-сульфокислоты получают нитрил никотиновой кислоты:
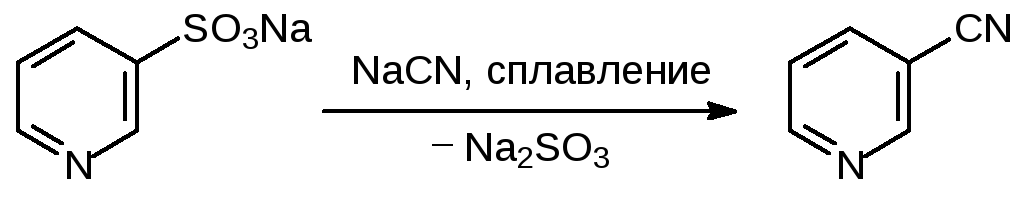
Синтез эфиров и амидов сульфокислот прямым замещением кислотных гидроксильных групп на алкоксигруппы (этерификация) или на амидные группы не реализуем. Поэтому серьёзное препаративное значение имеют хлорангидриды сульфокислот. Для их получения можно использовать реакцию тионилхлорида или пентахлорида фосфора с сульфокислотами:
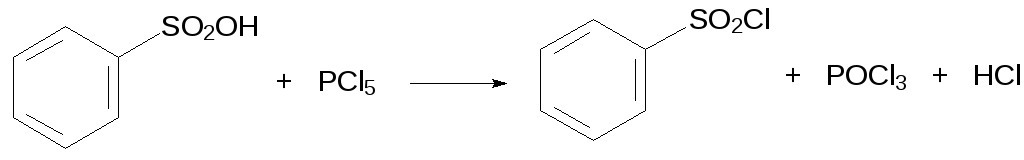
Сульфохлориды образуются также при взаимодействии ароматических соединений с избытком хлорсульфоновой кислоты:
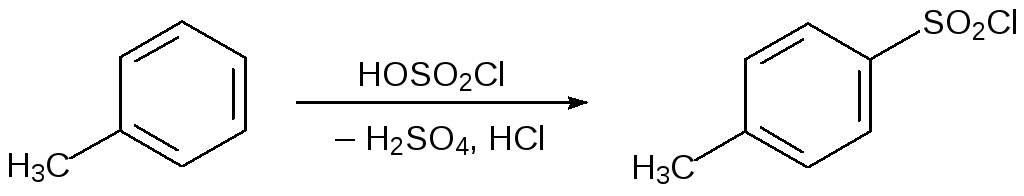
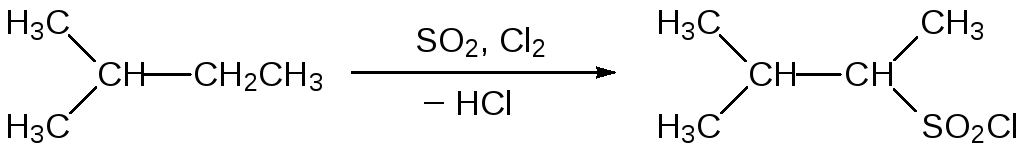
По свободнорадикальному механизму с образованием хлорангидридов сульфокислот протекает сульфохлорирование алифатических соединений диоксидом серы и хлором. Сульфохлорирование высших углеводородов по этой реакции протекает неизбирательно, но с некоторыми углеводородами выходы одного из возможных продуктов взаимодействия оказываются достаточно высокими, поскольку атомы водорода у вторичного атома углерода замещаются легче, чем у первичного, а третичные СН-связи в реакцию сульфохлорирования не вступают из-за стерических затруднений. В соответствии с этим, например, при сульфохлорировании 2‑метилбутана основным продуктом реакции становится хлорангидрид 3‑метилбутан-2-сульфокислоты:
Ещё один способ получения сульфохлоридов представлен взаимодействием солей диазония с диоксидом серы, которое, как и все реакции Зандмейера, проводят в присутствии солей одновалентной меди:
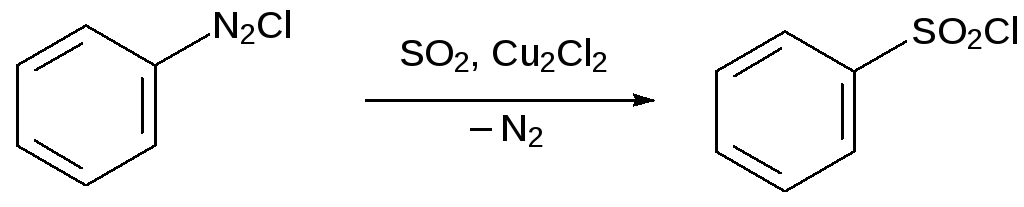
Обычно эту реакцию используют для получения амидов сульфокислот. Для этого, не выделяя из реакционной массы достаточно устойчивый к действию воды в кислой среде сульфохлорид, к реакционной массе добавляют соответствующий амин и извлекают из неё образовавшийся амид.
Сульфохлориды образуются также при хлорировании тиольных соединений в воде:
![]()
Важное место в арсенале бактерицидных средств занимают сульфаниламидные препараты. Механизм их действия основан на ингибировании биосинтеза дигидрофолиевой и тетрагидрофолиевой кислот вследствие блокировки фермента дигидроптероатсинтазы. Простейший представитель этого класса антимикробных препаратов амид сульфаминовой кислоты является антиметаболитом 4-аминобензойной кислоты, которая участвует в образовании фолиевой кислоты. Сульфаниламид, известный под названием стрептоцид, синтезируют из ацетанилида по схеме:
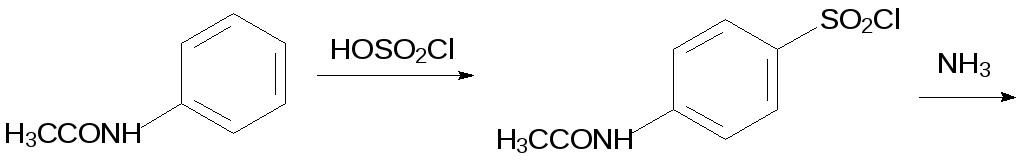
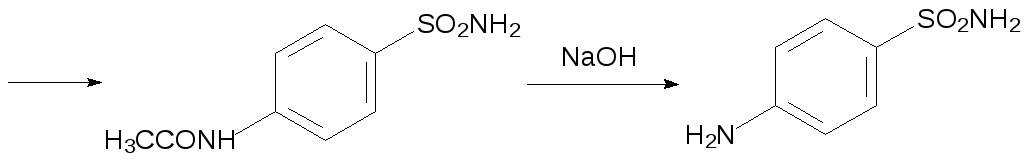
В качестве примера других соединений этого ряда с более широким спектром антибактериальной активности можно привести структуры сульфодиметоксина и норсульфазола:
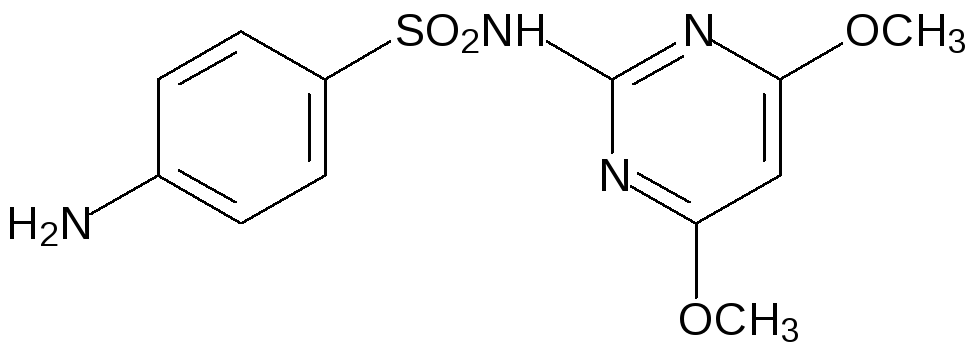
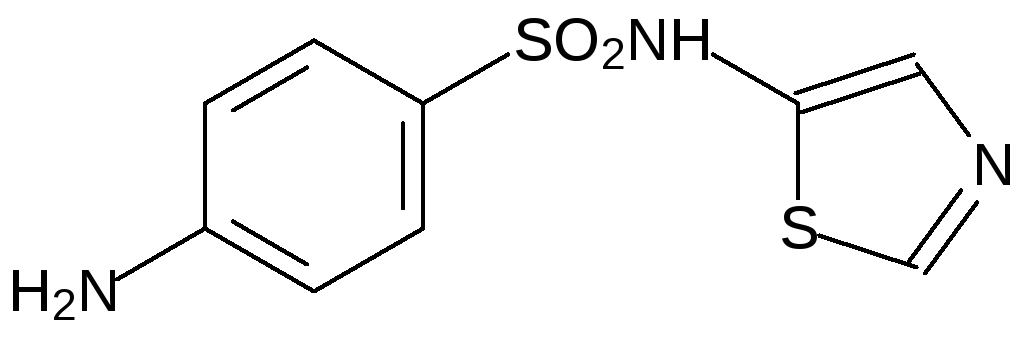
Сульфокислоты находят широкое применение в лабораторной практике, в производстве лекарственных средств и в промышленности. Метансульфокислота (её соли и эфиры часто называют мезилатами) и п‑толуолсульфокислота (её соли и эфиры – тозилаты) используются в качестве катализаторов химических реакций. Так, например, первый способ получения диэтилового эфира был основан на катализируемом серной кислотой взаимодействии двух молекул этилового спирта с отщеплением воды (поэтому его называют серным эфиром), однако в этой реакции серная кислота выступает также в качестве окислителя. Это приводит к непроизводительному расходованию серной кислоты и загрязнению серного эфира продуктами окисления этанола. В отличие от серной кислоты п-толуолсульфокислота не является окислителем и практически не расходуется при катализе превращения этанола в диэтиловый эфир.
Очень сильной кислотой (суперкислотой) является трифторметан-сульфокислота (её соли и эфиры – трифлаты). Современный способ получения трифторметансульфокислоты основан на электрохимическом фторировании метансульфокислоты во фтористоводородной кислоте. Трифторметансульфокислота термически и химически стабильна, что отличает её от других суперкислот, например, от хлорной кислоты HClO4, которая является сильным окислителем.
Сульфокислотные функциональные группы входят в состав многих красителей и ионобменных смол. Многие анионогенные синтетические поверхностно-активные вещества также являются солями сульфокислот.