Материал: Руководство к лабораторным занятиям по микробиологии (МГУПП)
Периодическое культивирование.
Глубинное культивирование микроорганизмов можно проводить по периодической или непрерывной схеме.
При периодическом режиме культивирования весь объем питательной среды засевают посевной культурой, и выращивание ведут в оптимальных условиях определенный период времени до накопления нужного количества целевого продукта, т.е. процесс осуществляется в закрытой системе.
При таком режиме клетки все время находятся вменяющихся условиях. Сначала они имели в избытке питательные вещества, затем постепенно наступает недостаток питания и отравление вредными продуктами обмена. В результате непрерывно изменяется скорость роста культуры, ее физиолого-биохимические и морфологические показатели. В таких условиях роста культура проходит несколько фаз развития, из которых можно выделить четыре основные: (рис. 3.2).
l
I
II III
IV

 g
N
g
N

l

 gN2
gN2
l
 gN1
gN1

τ1 τ2 τ ,час
продолжительность культивирования
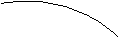
Рис.3.2. Фазы развития культуры микроорганизмовпри периодическом культивировании.
I – лаг-фаза; II – логарифмическая фаза; III – стационарная фаза; IV – фаза отмирания.
N – численность микробных клеток;
Первая фаза – называется «лаг-фаза», или фаза задержки роста, следует непосредственно за внесением посевного материала в питательную среду. В этой фазе микроорганизмы не размножаются, а адаптируются к новым условиям среды. Наблюдается увеличение содержания нуклеиновых кислот в клетках и увеличение их размеров. Численность культуры не увеличивается.
Вторая фаза - фаза логарифмического роста (или экспоненциальная) характеризуется высокой скоростью размножения клеток, так как в среде высока концентрация питательных веществ и незначительное количество вредных продуктов клеточного обмена. Численность популяции увеличивается с максимальной скоростью. В благоприятных условиях микробные клетки делятся каждые 20-30 мин, их число увеличивается в геометрической прогрессии.
Способы культивирования микроорганизмов.
Культивирование микроорганизмов можно поводить поверхностным или глубинным, периодическим или непрерывным методами, в аэробных или анаэробных условиях. Большое значение при выборе способа культивирования имеет отношение выбранного культивируемого микроорганизма к молекулярному кислороду и конечная цель культивировании, которой может быть либо накопление биомассы клеток, либо получение определенного метаболита (спирта, фермента, витамина, аминокислоты и т.д.).
Поверхностное культивирование.
При поверхностном культивировании микроорганизмы развиваются на поверхности питательной среды. Среды могут быть плотными, сыпучими или представлять собой тонкий слой жидкой среды. Практически метод применим только для культивирования аэробных микроорганизмов. В этом случае микроорганизмы получают кислород непосредственно из воздуха. Важным условием реализации метода является большая площадь соприкосновения поверхности питательной среды с окружающим воздухом. В жидких средах аэробные микроорганизмы часто растут, образуя на поверхности пленку. Факультативные анаэробы развиваются не только на поверхности, но и в толще жидкой среды, вызывая более или менее равномерное ее помутнение.
Поверхностное культивирование микроорганизмов применяют в лабораторной практике.
Глубинное культивирование.
Глубинный метод культивирования является более совершенным по сравнению с поверхностным. При этом микроорганизмы растут и развиваются во всем объеме питательной среды. При глубинном культивировании применяют жидкие питательные среды. Метод можно использовать для выращивания аэробов и анаэробов.
Образующиеся при глубинном культивировании остатки питательной среды, растущие в ней микроорганизмы и продукты их жизнедеятельности называют культуральной жидкостью.
При глубинном культивировании аэробные микроорганизмы используют растворенный в среде кислород. Вместе с тем растворимость кислорода в воде невелика, поэтому для нормального роста аэробных микроорганизмов в толще среды, ее необходимо постоянно аэрировать - подводить кислород во всю толщу жидкой среды. В результате питательная среда насыщается кислородом воздуха и создаются благоприятные условия для развития аэробов.
В лабораторной практике способ глубинного культивирования реализуется путем использования специальных установок – качалок, обеспечивающих встряхивание или вращение колб и пробирок со скоростью 100-200 об/мин и более. Чем больше скорость вращения, тем больше поверхность соприкосновения среды с воздухом и выше насыщение ее кислородом. Помимо перемешивания, аэрировать питательную среду можно продуванием (барботированием) через ее толщу стерильного воздуха. Этот способ аэрации используется в лабораторной практике и в промышленности. где его применяют при производстве антибиотиков, ферментов, витаминов, органических кислот, микробной биомассы. В промышленных масштабах глубинное культивирование осуществляют в специальных аппаратах – ферментаторах.
Глубинное культивирование имеет ряд преимуществ по сравнению с поверхностным – это сокращение производственных площадей, возможность автоматизации, удобство выделения конечного продукта, и главное - возможность осуществления процесса непрерывного культивирования.
Третья фаза - стационарная (фаза зрелости). Размножение микроорганизмов замедляется, скорость роста уменьшается вследствие истощения питательных веществ и накопления продуктов обмена. В результате скорость роста выравнивается со скоростью отмирания культуры и какое-то время число клеток остается постоянным, т.е. наблюдается состояние динамического равновесия.
Четвертая фаза - фаза отмирания, когда скорость отмирания клеток превышает скорость роста. Это происходит вследствие истощения питательной среды, накопления в ней токсичных продуктов обмена и автолиза культуры.
Недостаток периодического культивирования– постоянное изменение условий и нерациональные затраты времени на прохождение всех четырех стадий развития культуры, причем период самой активной фазы – логарифмической - занимает небольшую часть цикла. Этот недостаток устранен в схеме непрерывной схеме.
Непрерывное культивирование.
Сущность метода заключается в поддержании постоянных условий среды, а, следовательно, и культуры микроорганизмов в определенном, наиболее активном физиологическом состоянии.
Реализуется этот способ непрерывной подачей в ферментатор стерильной питательной среды и одновременным непрерывным отбором культуральной жидкости. Посевной материал при этом выращивается до стадии логарифмического роста и однократно вносится в питательную среду в начале процесса. Основным условием метода является равенства скорости притока питательной среды, скорости отбора культуральной жидкости и удельной скорости роста культуры. При таком условии культура постоянно поддерживается в логарифмической фазе роста (рис. 3.3.).
I II

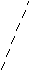 lg
N
lg
N


продолжительность культивирования, τ ,час
Рис.3.3. Развитие культуры при непрерывном культивировании:
I – лаг-фаза; II – логарифмическая фаза;
N – численность микробных клеток
Получение чистой культуры
Получение чистой культуры (ЧК) из сообщества микробных клеток очень трудоемкий и сложный процесс, включающий несколько стадий:
- получение накопительной культуры;
- выделение из накопительной культуры чистой культуры;
- проверка чистоты и идентификация выделенной чистой культуры.
Накопительная культура – это культура, состоящая из микроорганизмов со схожими физиологическими свойствами. Накопительную культуру получают при выделении чистой культуры микроорганизма из какого-либо материала или природного субстрата (например, воды, воздуха, почвы), в котором данный микроорганизм находится в небольшом количестве. Накопительную культуру получают в элективных условиях, способствующих развитию выделяемого микроорганизма и ограничивающих рост сопутствующих. Указанные условия можно создать путем использования элективных сред. В результате накопительная культура будет содержать преимущественно клетки одного вида микроорганизма, так как элективные среды в сочетании с элективными условиями ограничивают развитие сопутствующих микроорганизмов. О получении накопительной культуры судят визуально, по появлению характерных признаков роста выделяемых микроорганизмов – помутнению среды, изменению цвета среды, появлению пленки, осадка, пузырьков газа. Помимо визуальной оценки, культуральную жидкость микроскопируют и выявляют присутствие выделяемых форм. В некоторых случаях о получении накопительной культуры свидетельствуют характерные химические изменения в составе среды, которые должны сопровождать процесс накопления выделяемых микроорганизмов. Это может быть образование аммиака, сероводорода и т.п.
После получения накопительной культуры приступают к выделению чистой культуры. Чистая культура может быть получена из отдельной колонии или из одной клетки.
Получение чистой культуры из одной клетки производится капельным методом, с помощью микроманипулятора и с помощью микроселектора.
Капельный метод (метод Линднера) применим при работе с крупными микроорганизмами – дрожжами, мицелиальными грибами, водорослями. Для выделения готовят сильно разбавленные разведения накопительной культуры с таким расчетом, чтобы в небольшой капельке разведения были единичные клетки микроорганизмов. Затем на поверхность стерильного покровного стекла стерильной пастеровской пипеткой наносят ряд капель из этого разведения. Стекло с нанесенными каплями используют для приготовления препарата «висячая капля». Капли микроскопируют и отмечают те, где обнаружена только одна клетка. Затем препарат «висячая капля» переносят в чашку Петри и инкубируют в течение 12-24 час. После инкубации отмеченные капли снова микроскопируют и те, в которых произошло размножение, осторожно снимают с покровного стекла кусочком стерильной фильтровальной бумаги и бумагу переносят в пробирку с жидкой стерильной питательной средой.
При использовании микроманипулятора выделение единичных клеток из суспензии проводится под контролем микроскопа при помощи специальной микроскопической пипетки. Извлеченные клетки переносят в пробирки с жидкой питательной средой.
Микроселектор представляет собой стеклянный микрокапилляр с прямоугольным сечением, что позволяет хорошо просматривать его содержимое при микроскопировании с иммерсионным объективом. Капилляр заполняют исследуемой суспензией клеток и при большом увеличении микроскопа находят участок с одной клеткой. Затем под микроскопическим контролем специальным приспособлением этот участок капилляра стерильно выбивают в приемник, из которого затем перенося в стерильную питательную среду.
Основным методом выделения чистой культуры микроорганизмов из отдельной колонии до настоящего времени является метод, предложенный Р.Кохом. Принцип метода базируется на утверждении, что отдельная колония является результатом развития одной клетки и состоит в высеве накопительной культуры на дифференциально-диагностические среды с целью получения из отдельных клеток суспензии изолированных колоний.
При выделении чистых культур аэробных микроорганизмов высев накопительной культуры проводят на поверхность плотной среды. Накопительную культуру или ее разведение наносят на поверхность среды и осторожно распределяют по поверхности стеклянным стерильным шпателем Дригальского. Накопительную культуру на поверхность среды можно наносить и бактериологической петлей в виде «истощающего штриха». После рассева чашки Петри инкубируют в течение 1 – 7 суток, так как скорость роста различных микроорганизмов неодинакова. Чашки просматривают ежедневно и отмечают появление изолированных колоний ( рис.3.4). Выросшие изолированные колонии отсевают петлей в пробирки на поверхность скошенной плотной среды или в жидкую среду.
При выделении чистых культур факультативных аэробов и факультативных анаэробов высев накопительной культуры (или ее разведений) проводят глубинным способом. Для этого 0,5-1,0 см3 клеточной суспензии вносят в стерильную чашку Петри и туда же приливают 10-15 см3 расплавленной и остуженной до 48-50ºС питательной среды. Чашку закрывают и осторожно, круговыми движениями на плоской поверхности, тщательно перемешивают ее содержимое и оставляют до полного застывания среды. После того, как среда застынет, чашки помещают в термостат. При таком способе посева часть колоний оказывается в толще среды. Такие колонии вырезают и переносят в жидкую среду, благоприятную для развития выделяемых микроорганизмов.
При выделении анаэробных микроорганизмов требуется создание условий, ограничивающих доступ кислорода к культуре. Разведения накопительной культуры и посев в чашки Петри с плотной питательной средой проводят так же, как и при глубинном посеве. Чашки с посевами помещают в специальные приборы – анаэростаты, из которых затем откачивают воздух. Остаточное давление не должно превышать 2 – 3 кПа. Анаэробные условия можно создать и в отдельной чашке Петри Для этого высеваемое разведение и питательную среду вносят не в донышко чашки, а в ее крышку. После застывания среды на нее ставят донышко чашки («донышко вошло» в перевернутую крышку) и образовавшийся между ними зазор заливают парафином. Посевы термостатируют и после появления изолированных колоний их извлекают и переносят в жидкую среду, благоприятную для развития выделяемой культуры.