Материал: Руководство к лабораторным занятиям по микробиологии (МГУПП)
Основные технические характеристики микроскопа
Общее увеличение микроскопа – определяется произведением увеличения объектива на увеличение окуляра. Так общее увеличение, которое позволит максимально увеличить объект при использовании микроскопа БИОМЕД-4, составит 10 х 100 = 1000 раз.
Однако общее увеличение еще не характеризует всех возможностей микроскопа. Увеличенное изображение может оказаться как четким, так и нечетким.
Отчетливость получаемого изображения определяется разрешающей способностью микроскопа, т.е. той наименьшей величиной объектов или их деталей, которые можно увидеть с его помощью. Следовательно, чем меньше размер частицы, видимой в микроскоп, тем больше его разрешающая способность.
Пользуясь биологическим микроскопом, можно рассмотреть предмет размером не менее 0,2мкм 1.
Порядок работы со светопольным микроскопом
Обращение с микроскопом требует навыков, поэтому, приступая к работе с ним, необходимо усвоить основные правила пользования микроскопом.
1. На рабочем столе микроскоп БИОМЕД помещают ручкой от себя, на расстоянии 3…5 см от края стола. Перед началом работы следует осторожно мягкой тканью, пропитанной капелькой этилового спирта, потереть фронтальные линзы объективов.
2. Устанавливают правильное освещение поля зрения микроскопа. Для этого, включают осветитель. С помощью револьвера ставят в рабочее положение объектив с увеличением 4х. Легкий упор и звук щелчка пружины револьвера свидетельствует о том, что объектив установлен по оптической оси. Макрометрическим винтом опускают объектив на расстояние 0,5…1,0 см от предметного столика. Полностью открывают ирисовую диафрагму и поднимают конденсор вверх до упора. При правильной установке поле зрения микроскопа будет иметь форму хорошо и равномерно освещенного круга. При микроскопировании окрашенных препаратов верхняя линза конденсора должна находиться на уровне предметного столика. При просмотре неокрашенных препаратов желаемую степень освещения регулируют, слегка опустив конденсор и
-------------------------------------------------------------------------------------------------
1 Микрометр – тысячная доля миллиметра (0,001 мм)
прикрыв ирисовую диафрагму.
Правила работы с сухими объективами.
Приготовленный препарат помещают и закрепляют с помощью держателя (6) на предметном столике. Сначала препарат рассматривают с объективом 10х, а затем переходят к большим увеличениям. Необходимо помнить, что чем меньше увеличение объектива, тем больше при установке препарата на фокус будет свободное рабочее расстояние (расстояние между объективом и препаратом).
С помощью сухого объектива с увеличением 10х просматривают несколько полей зрения. Передвигают предметный столик с помощью ручки перемещения препарата (16). Нужный для исследования участок препарата устанавливают точно в центре поля зрения. Вращением револьвера переводят объектив с увеличением 40х. Наблюдая сбоку, макрометрическим винтом поднимают предметный столик почти до соприкосновения с препаратом (не касаясь его). Затем, смотря в окуляр, тем же винтом очень медленно опускают столик до появления изображения изучаемых объектов. После этого вращением микрометрического винта в ту или другую сторону (но не более чем на 2…4 деления) производят его точную фокусировку. Если при повороте микровинта на 2…4 деления (пол-оборота) в ту или иную сторону изображение не найдено, снова возвращаются к поиску изображения с использованием макрометрического винта, а затем переходят к работе с микрометрическим винтом. При смене объективов необходимо регулировать степень освещения препарата с помощью конденсора. Так, при просмотре препарата с объективом 10х конденсор опускают, а при переходе на объектив 40х конденсор несколько поднимают.
Правила работы с иммерсионным объективом.
На препарат (лучше фиксированный и окрашенный) наносят каплю иммерсионного масла. С помощью держателя препарата (6) закрепляют препарат на предметном столике. Поворачивают револьвер и устанавливают по центральной оптической оси иммерсионный объектив с увеличением 100х. Конденсор поднимают вверх до упора. Ирисовую диафрагму конденсора открывают полностью. Глядя сбоку, предметный столик с помощью макрометрического винта поднимают до погружения объектива в масло, почти до соприкосновения его фронтальной линзы с предметным стеклом препарата. Это нужно проводить очень осторожно, чтобы фронтальная линза объектива не получила повреждения. Смотрят в окуляр, очень медленно вращают макрометрический винт от себя и, не отрывая объектив от масла, опускают тубус до появления грубого изображения. При этом следует помнить, что свободное рабочее расстояние в иммерсионном объективе равно 0,09…0,10 мм. Затем точную фокусировку производят микрометрическим винтом. Рассматривают в препарате несколько полей зрения, передвигая столик с помощью ручки перемещения препарата (16).
По окончании работы с иммерсионным объективом опускают предметный столик, снимают препарат и осторожно протирают фронтальную линзу объектива сначала сухой мягкой хлопчатобумажной салфеткой, затем той же салфеткой, но смоченной капелькой спирта. Оставлять масло на поверхности линзы нельзя, так как оно способствует оседанию пыли, высыхает и со временем может привести к повреждению оптики микроскопа. Препарат освобождают от масла сначала кусочком фильтровальной бумаги, затем обрабатывают стекло бензином или спиртом.
Для микроскопирования микроорганизмов необходимо соответствующим образом приготовить препарат. Препараты обычно готовят на предметном стекле. Нередко требуется еще и покровное стекло. Все стекла должны быть совершенно чистыми и обезжиренными.
Приготовление витальных препаратов микроорганизмов
Препарат типа «раздавленная капля». Этот препарат готовят для рассматривания микроорганизмов в живом состоянии. Для этого на середину предметного стекла наносят каплю водопроводной воды и в нее вносят небольшое количество исследуемых микроорганизмов (или каплю, суспензии микроорганизмов), размешивают и покрывают покровным стеклом. Культуру, выращенную на плотной питательной среде, переносят в каплю воды бактериологической петлей (рис.2); культуру, выращенную в жидкой среде, - стерильной пипеткой. Капля исследуемого материала должна быть настолько мала, чтобы после прижимания ее покровным стеклом не было избытка жидкости, выступающего из-под него. В противном случае избыток жидкости необходимо удалять фильтровальной бумагой, которую затем сразу же опускают в дезинфицирующий раствор.
Препарат «висячая капля». Такой препарат используют для исследования подвижности микроорганизмов, прорастания спор и т.д. Для этого каплю суспензии микроорганизмов петлей наносят на покровное стекло, края которого предварительно смазывают вазелином, затем поворачивают каплей вниз и помещают на специальное предметное стекло с лункой в центре. Капля должна свободно висеть, не касаясь краев и дна лунки (рис.3).
Препараты живых клеток рассматривают с «сухими системами» микроскопа. Препараты, работа с которыми закончена, прежде чем вымыть, выдерживают в дезинфицирующем растворе.
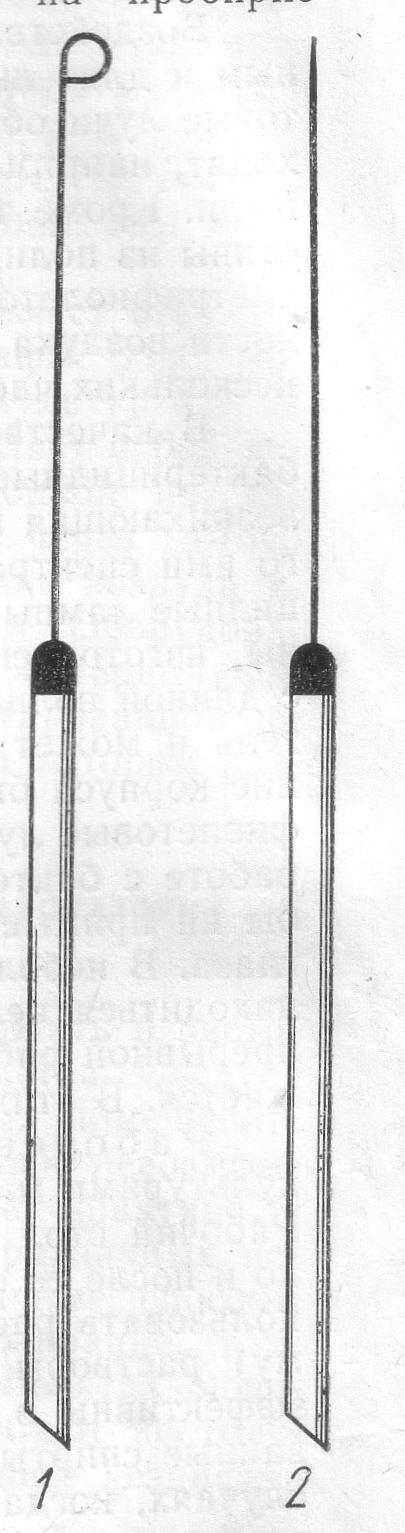
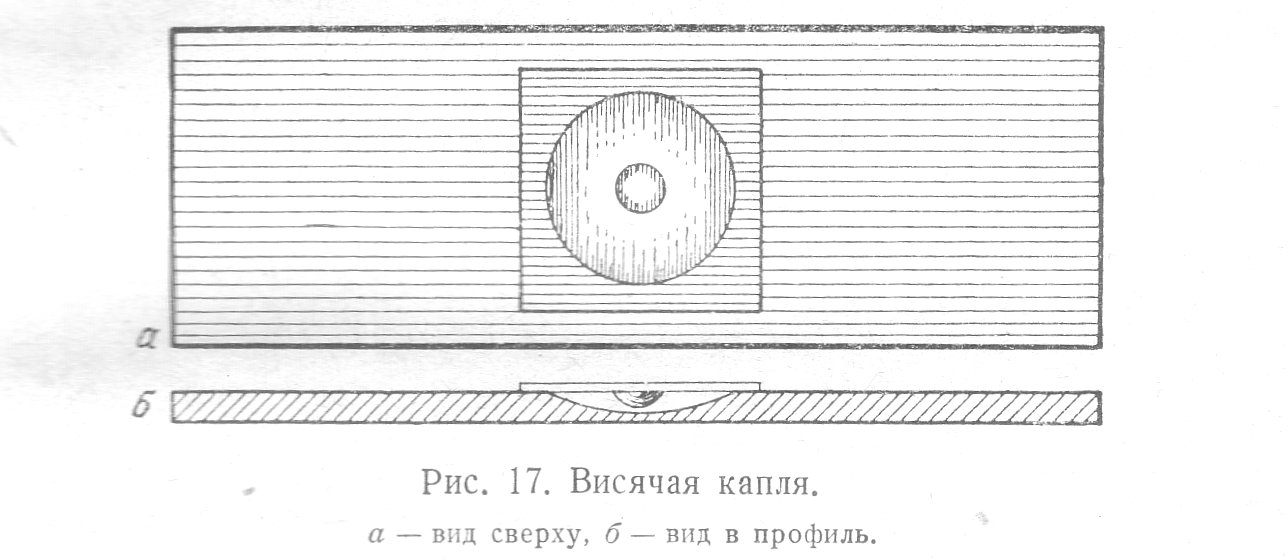
Рис.3. Препарат «висячая капля»
Рис.2 Бактерио-
логическая пет-
ля (1) и препаро-
вальная игла (2)
Лабораторная работа 1
Тема занятия:
Устройство оптического микроскопа типа «Биолар-4». Приготовление препаратов микроорганизмов
«Приготовление витальных препаратов микроорганизмов и правила работы с сухими системами».
Цель занятия. Усвоить правила пользования микроскопом «Биолар-4».
Задания. 1. Ознакомиться со светопольной системой микроскопа.
2. Изучить устройство микроскопа, правила пользования им в микробиологической практике (обратить внимание на работу с сухими системами) и иммерсионным объективом).
Оборудование и материалы. Микроскопы, флаконы с кедровым маслом, готовые окрашенные микробные препараты («раздавленная капля» и «мазок») – по числу студентов.
План проведения занятия
-
Ознакомиться с устройством микроскопа и правилами работы с ним.
-
Приготовить и промикроскопировать препарат хлебопекарных дрожжей типа «раздавленная капля» с сухими системами (с объективами 10х, 40х).
Препараты фиксированных окрашенных клеток
Приготовление фиксированных окрашенных препаратов включает следующие этапы: приготовление мазка, высушивание фиксацию и окраску. Способы окрашивания делят на простые и сложные. Различные способы окраски основаны на физико-химических особенностях микробной клетки и взаимодействии структур и веществ ее с используемыми реактивами.
При простых способах окрашивания используют один краситель. Простое окрашивание применяется для ознакомления с морфологией бактерий.
-
Приготовление мазка. На обезжиренное предметное стекло наносят маленькую каплю водопроводной воды и переносят в нее петлей небольшое количество исследуемого материала. Полученную суспензию равномерно размазывают петлей на площади 1-2см3 возможно более тонким слоем. Мазок должен быть настолько тонок, чтобы высыхал почти тотчас же после приготовления.
-
Высушивание мазка. Полученный мазок высушивают при комнатной температуре на воздухе или (для ускорения) в потоке теплого воздуха высоко над пламенем горелки, держа стекло мазком вверх (не допуская нагрева стекла).
-
Фиксация. Цели фиксации: убить микроорганизмы, т.е. сделать безопасным дальнейшее обращение с ними; обеспечить лучшее прилипание клеток к стеклу; сделать мазок более восприимчивым к окраске. Стекло с сухим мазком трижды проводят через наиболее горячую часть пламени горелки, держа предметное стекло мазком вверх.
-
Окраска. Охлажденный фиксированный препарат помещают на параллельные стеклянные рейки, лежащие над кюветой (рис.4), наносят 1…2 капли фуксина и, после выдерживания в течение 1…3 мин, смывают с него краску слабой струей воды из промывалки до тех пор, пока стекающая вода не станет бесцветной. Затем препарат высушивают, вначале осторожно промокая
фильтровальной бумагой, а затем –
на
воздухе до
полного его высыхания. 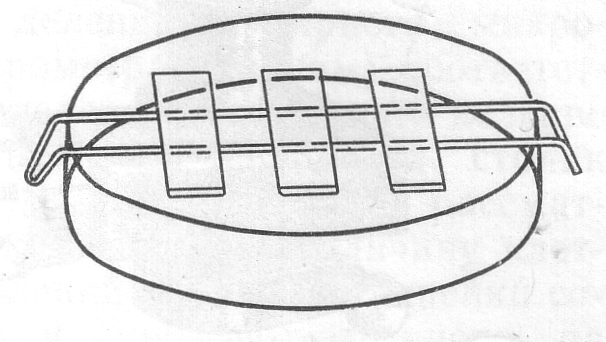
На препарат наносят каплю иммерсион-
ного масла и микроскопируют с объек-
тивом 100х.
Рис.4 Кювета с параллельными
рейками для окрашивания
препарата
При сложных способах окрашивания применяют два или более красящих вещества. Кроме красящих, используют различные обесцвечива-ющие вещества (спирт и др.). Такие способы окрашивания называют диф-ференциальными. Дифференциальныая окраска предполагает окрашивание определенных структур клетки. С ее помощью выявляют некоторые клеточ-ные структуры, запасные вещества и включения.
Окраска по Граму.
-
На обезжиренном предметном стекле делают мазки разных бактерий: в центре мазок исследуемой культуры, слева и справа – контрольных культур (рис.5), одна из которых должна быть грамположительной (Sarcina), другая – грамотрицательной (Escherichia coli). Мазки готовят, как и при простом способе (см. с. ).
-
На мазки наносят 2…3 капли раствора кристаллического фиолетового и через 2…3 мин окрашивания краску смывают водой.
-
Наносят 2…3 капли раствора Люголя и по истечении 1…2 мин смыва-ют водой (препарат чернеет).
-
Препарат обесцвечивают 0,5…1,0 мин 96%-ным этиловым спиртом, быстро промывают водой и дополнительно окрашивают 1…2 мин водным фуксином. Препарат промывают водой, высушивают и
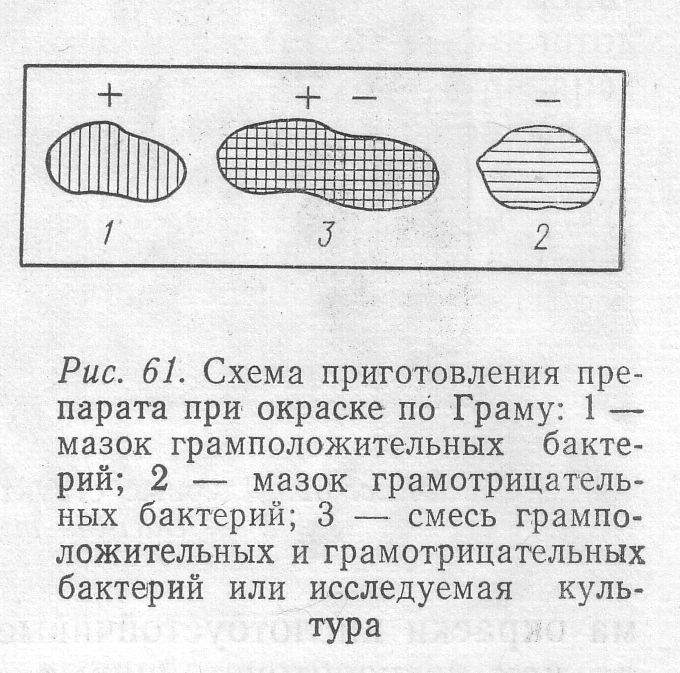
Рис.5. Схема приготовления препарата при окраске по Граму:
1 – мазок грамположительных бактерий; 2 – мазок грам-
отрицательных бактерий; 3 – исследуемая культура.
микроскопируют с иммерсионной системой. При правильном окрашивании грамположительные бактерии имеют сине-фиолетовый, грамотрицательные – розово-красный цвет.
Контрольные вопросы
-
Из каких частей состоит микроскоп?
-
Каково назначение макро- и микрометрического винтов? Как ими пользоваться?
-
Что такое сухие и иммерсионные объективы?
-
Зачем и как используют иммерсионное масло при работе с иммерсионным объективом?
-
Как определяют общее увеличение микроскопа?
-
Как регулировать степень освещенности препарата?
-
Как готовить препарат «раздавленная капля»? С какими объективами его микроскопируют?
-
Как можно дифференцировать мертвые и живые клетки в приготовленной суспензии хлебопекарных дрожжей?
-
Что такое витальный способ окраски дрожжей? Для чего его применяют?
Лабораторная работа 2
Тема занятия:
Устройство оптического микроскопа типа «Биолар-4». Приготовление препаратов микроорганизмов (продолжение).
«Приготовление препаратов фиксированных окрашенных клеток микроорганизмов. Правила работы с иммерсионной системой».
Препараты фиксированных окрашенных клеток
Приготовление фиксированных окрашенных препаратов включает следующие этапы: приготовление мазка, высушивание фиксацию и окраску. Способы окрашивания делят на простые и сложные. Различные способы окраски основаны на физико-химических особенностях микробной клетки и взаимодействии структур и веществ ее с используемыми реактивами.
При простых способах окрашивания используют один краситель. Простое окрашивание применяется для ознакомления с морфологией бактерий.
-
Приготовление мазка. На обезжиренное предметное стекло наносят маленькую каплю водопроводной воды и переносят в нее петлей небольшое количество исследуемого материала. Полученную суспензию равномерно размазывают петлей на площади 1-2см3 возможно более тонким слоем. Мазок должен быть настолько тонок, чтобы высыхал почти тотчас же после приготовления.
-
Высушивание мазка. Полученный мазок высушивают при комнатной температуре на воздухе или (для ускорения) в потоке теплого воздуха высоко над пламенем горелки, держа стекло мазком вверх (не допуская нагрева стекла).
-
Фиксация. Цели фиксации: убить микроорганизмы, т.е. сделать безопасным дальнейшее обращение с ними; обеспечить лучшее прилипание клеток к стеклу; сделать мазок более восприимчивым к окраске. Стекло с сухим мазком трижды проводят через наиболее горячую часть пламени горелки, держа предметное стекло мазком вверх.
-
Окраска. Охлажденный фиксированный препарат помещают на параллельные стеклянные рейки, лежащие над кюветой (рис.4), наносят 1…2 капли фуксина и, после выдерживания в течение 1…3 мин, смывают с него краску слабой струей воды из промывалки до тех пор, пока стекающая вода не станет бесцветной. Затем препарат высушивают, вначале осторожно промокая