Материал: Полимеразная цепная реакция
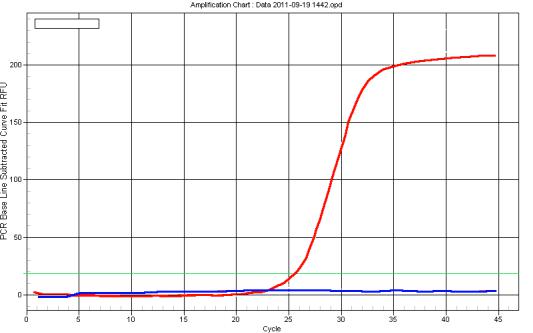
флуоресценции, а также логарифмический характер кривой флуоресценции (рис.
12).
интенсивность флуоресценции
верхнее плато
|
логарифмического |
роста |
фаза |
|
|
|
|
нижнее плато
циклы амплификации
Рис. 12. Кривая флуоресценции, полученная в ходе ПЦР «в реальном времени». Логарифмическая кривая отражает увеличения уровня флуоресценции вследствие накопление ампликонов (положительный результат реакции), горизонтальная кривая – отсутствие увеличения уровня флуоресценции (отрицательный результат).
ПЦР «в реальном времени» с интеркалирующими красителями имеет существенный недостаток: кривая флуоресценции позволяет отслеживать накопление двухцепочечной ДНК, но не дает возможности проконтролировать специфичность реакции, т.е. действительно ли полученные ампликоны являются копиями фрагмента ДНК выявляемого микроорганизма. При использовании ПЦР с электрофоретической детекцией контроль специфичности осуществляется путем оценки размера ампликонов (см. выше). В ПЦР «в реальном времени» с интеркалирующими красителями специфичность реакции определяется по температуре плавления.
Температура плавления
В двухцепочечной ДНК цепи связаны между собой с помощью водородных связей. При низкой температуре практически все молекулы ДНК двухцепочечные, однако при повышении температуры водородные связи теряют прочность, и определенный процент двухцепочечных ДНК распадается на одноцепочечные молекулы. При достижении температуры свыше 90°С остаются только одноцепочечные молекулы ДНК (именно это происходит в ПЦР на этапе денатурации, при температуре 95ºС).
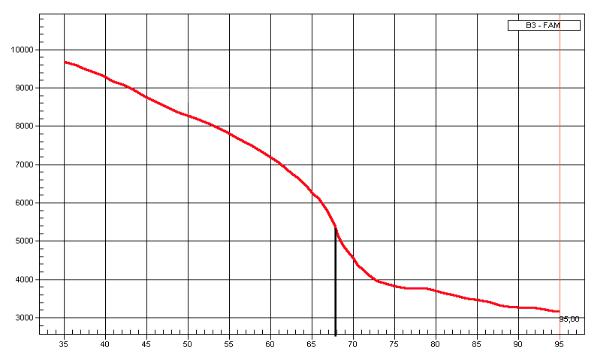
После завершения ПЦР амплификатор постепенно нагревает пробирку с продуктами реакции от 45ºС до 95ºС, одновременно регистрируя уровень флуоресценции. В результате прибор выстраивает кривую плавления, отражающую зависимость уровня флуоресценции от температуры (рис. 13). Так как уровень флуоресценции зависит от количества двухцепочечных ДНК в реакционной смеси, то при повышении температуры этот показатель будет снижаться. Температура, при которой распадаются 50% молекул ДНК (а остальные 50% остаются 2-цепочечными) получила название температуры плавления (если быть более точным, температуре плавления соответствует точка перегиба функции кривой плавления). Для разных молекул ДНК кривая плавления, и, следовательно, температура плавления, различаются. Температура плавления зависит от:
1)Размера молекулы ДНК. В длинных молекулах больше водородных связей и, следовательно, они более «тугоплавкие».
2)От соотношения между G+C/A+T. Гуанин и цитозин образуют 3 водородные связи, а аденин и тимин – 2, поэтому ДНК, обогащенная гуанином и цитозином, имеет более высокую температуру плавления.
интенсивность флуоресценции
Tm
температура
Рис. 13. Кривая флуоресценции. Тm – температура плавления.
Таким образом, оценка температуры плавления позволяет проконтролировать специфичность реакции и дифференцировать ампликоны, полученные из ДНК выявляемого микроорганизма, от побочных продуктов ПЦР. Однако точность такого контроля невысока: по температуре плавления можно дифференцировать лишь значительно различающиеся по размеру и нуклеотидной последовательности молекулы ДНК. По этой причине ПЦР «в реальном времени»
с интеркалирующими красителями используется все реже и постепенно замещается ПЦР с мечеными пробами.
ПЦР «в реальном времени» с меченными флуорофорами пробами
Проба – контрольный праймер, который не является затравочным. Нуклеотидная последовательность пробы подбирается так, чтобы она была комплементарна определенному участку амплифицируемого фрагмента ДНК. К пробе присоединены флуорофор и гаситель флуоресценции.
Флуорофор, входящий в состав пробы, не должен быть интеркалирующим. В настоящее время для изготовления проб используются несколько десятко различных флуорофоров, самые распространенные из которых FAM, HEX, JOE, ROX и другие.
Вобычных условиях флуорофор поглощает ультрафиолет и излучает свет с большей длиной волны. Гаситель флуоресценции – вещество, поглощающее излучение флуорофора и рассеивающее его в виде тепла. Сближение флуорофора
игасителя приводит к подавлению флуоресценции.
Внастоящее время используются несколько типов проб, самыми распространенными из которых являются разрушаемые пробы и пробы- «скорпионы».
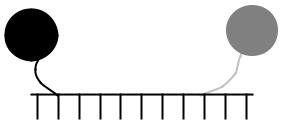
Разрушаемая проба представляет собой праймер длиной около 15 оснований, к которому присоединены флуорофор и гаситель. Флуорофор и гаситель сближены друг с другом, поэтому при освещении УФ излучение флуорофора поглощается гасителем (рис. 14).
флуорофор |
гаситель |
контрольный праймер
Рис. 14. Структура праймера-разрушаемой пробы.
На рисунке 15 представлена схема ПЦР с использованием разрушаемой пробы. Ампликон подвергается денатурации, после чего на стадии отжига к образовавшимся одноцепочечным молекулам присоединяются затравочные праймеры; к одной из цепей присоединяется также проба. На стадии элонгации ДНК-полимеразы достраивают комплементарные цепочки ДНК. За счет наличия у ДНК-полимеразы экзонуклеазной активности, она разрушает пробу, что приводит к разобщению флуорофора и гасителя. Высвободившийся флуорофор восстанавливает способность давать излучение.
Таким образом, каждое удвоение ампликона сопровождается высвобождением молекулы флуорофора, и интенсивность флуоресценции нарастает пропорционально росту числа образовавшихся ампликонов. Итоговая
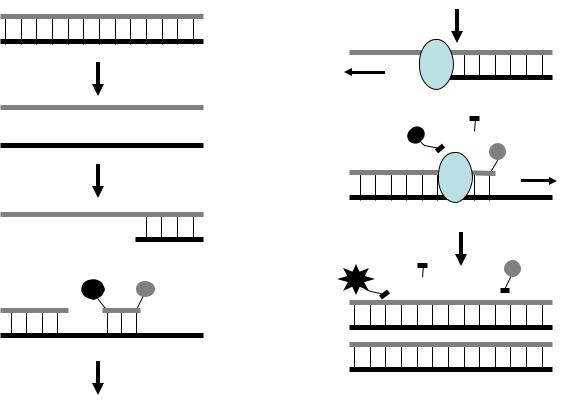
кривая роста флуоресценции выглядит так же, как при ПЦР «в реальном времени» с использованием интеркалирующих красителей.
амплифицируемый фрагмент ДНК
ДНКполимераза
денатурация
Ф
ДНКполимераза |
Г |
|
элонгация и разрушение проб
|
Ф |
Г |
Ф |
|
|
Г разрушаемая |
|
проба
отжиг праймеров и проб
удвоение ДНК и флуоресценция красителя
Рис. 15. Схема ПЦР «в реальном времени» с разрушаемыми пробами. Ф – флуорофор, Г – гаситель флуоресценции.
Проба, помимо того, что выполняет функцию индикатора амплификации, одновременно является контролем специфичности реакции. Нуклеотидная последовательность пробы подбирается так, чтобы она присоединялась в пределах амплифицируемого фрагмента. В случае, если амплификации подвергнется балластная ДНК, разрушения проб происходить не будет, и флуоресценция реакционной смеси не проявится.
Проба-«скорпион» представляет собой сложную структуру, в которой объединены затравочный праймер и контрольный праймер (проба).
Проба-«скорпион» состоит из 2 частей:
1)На 3’-конце пробы находится затравочный праймер.
2)На 5’-конце пробы находится «шпилька» с контрольным праймером.
«Шпилька» – элемент вторичной структуры молекулы одноцепочечной ДНК, который образуется в том случае, если один из участков молекулы оказывается комплементарен другому участку. В этом случае между комплементарными участками ДНК формируются водородные связи, как в двухцепочечной молекуле. «Шпильки» могут образовываться в праймерах, а также в ампликонах, что приводит к снижению эффективности ПЦР, поэтому их формирования обычно стараются избегать. Однако в пробах-«скорпионах» шпилька является функционально значимым элементом, и нуклеотидная последовательность пробы подбирается так, чтобы два ее участка были
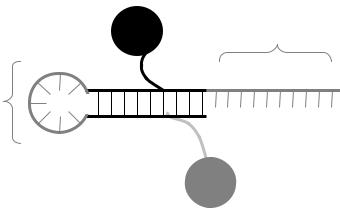
комплементарны друг другу. К одному из этих участков присоединен флуорофор, к другому – гаситель. При образовании между комплементарными участками шпильки флуорофор и гаситель оказываются сближены друг с другом, что проводит к подавлению флуоресценции. Головку «шпильки», расположенную между комплементарными учстками, образует контрольный праймер (рис. 16).
флуорофор
праймер
контрольный праймер
«шпилька»
гаситель
Рис. 16. Структура пробы-«скорпиона».
При проведении ПЦР с использованием пробы-«скропиона» на стадии денатурации происходит разъединение амплифицируемого фрагмента. На стадии отжига к одной из цепей присоединяется затравочный праймер пробы- «скропиона» (для упрощения схемы вторая цепь удалена), после чего на стадии элонгации происходит досторойка комплементарной цепи.
Во время следующего цикла ПЦР на стадии денатурации происходит разъединение цепей получившегося ампликона, при этом проба-«скорпион» оказывается частью вновь синтезированной цепи. Одновременно происходит разъединение шпильки.
Контрольный праймер, образующий головку шпильки, комплементарен определенному участку вновь синтезированной цепи. На стадии отжига происходит связывание контрольного праймера с цепью. Флуорофор и гаситель оказываются разобщены, что устраняет подавление гасителем флуоресценции
(рис. 17).
Таким образом, используемые в ПЦР «в реальном времени» пробы, меченные флуорофорами и гасителями, позволяют отслеживать накопление ампликонов по уровню флуоресценции и одновременно являются контролем специфичности реакции. Флуоресценция пробы возможна лишь после ее связывания с комплементарной нуклеотидной последовательностью в составе ампликона. Контроль с использованием проб обладает значительно более высокой специфичностью, чем приблизительная оценка размера ампликонов с помощью электрофореза или оценка температуры плавления с помощью интеркалирующих красителей.