Материал: Полимеразная цепная реакция
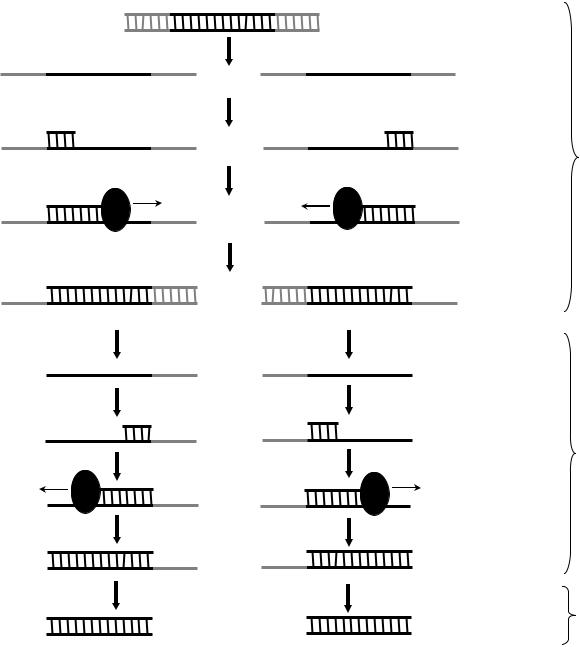
На этапе элонгации происходит достройка комплементарных цепей ДНК с участием ДНК-полимеразы, использующей праймеры в качестве затравок. Движение ДНК-полимеразы происходит от 3'-конца к 5'-концу матричной цепи и, соответственно, достройка комплементарных цепей происходит в этом же направлении.
По завершении цикла на матрице одной молекулы ДНК синтезируются 2 дочерние молекулы ДНК. У каждой из дочерних молекул ДНК вновь синтезированная цепь ограничена со стороны 5’-конца праймером (в одной из дочерних молекул ДНК – прямым праймером, в другой – обратным).
3’
F
3’
F
3’
5’
3’
5’
5’
5’
3’
5’
3’
5’
5’
3’
-ДНК полиме раза
R
ДНКполиме раза |
R |
|
5’_
5’_
3’ +
5’
5’
5’
3’
5’
3’
3’
3’
3’
_
_
_
+
_
+
+
+
+
3’ |
+ |
исходная ДНК |
|
|
_ |
|
|
5’ |
|
|
|
5’ |
|
3’ + |
денатурация |
|
|
R |
|
5’ |
|
3’ + |
отжиг |
|
ДНКполиме раза |
R |
|
|
|
элонгация |
|
5’ |
|
|
|
|
3’ + |
|
|
3’ |
|
5’_ |
|
|
|
|
конец цикла |
5’ |
|
3’ + |
|
3’ |
|
5’_ |
денатурация |
|
|
||
F |
|
|
|
3’ |
|
5’_ |
отжиг |
|
|
||
F |
|
-ДНК полиме раза |
|
|
|
|
|
3’ |
|
5’ _ |
элонгация |
5’ |
|
3’ + |
|
|
|
5’ _ |
конец цикла |
3’ |
|
|
|
5’ |
|
3’ + |
|
3’ |
|
5’ _ |
|
I ц и к л
II ц и к л
III ц и к л
Рис. 5. Схема амплификации ДНК в ПЦР (пояснение в тексте). Черным цветом выделен амплифицируемый фрагмент ДНК. «+» и «–» – соответственно, «плюс»- и «минус»-цепи ДНК. Стрелками указано направление движения ДНКполимеразы. На II цикле ПЦР (этап денатурации) для упрощения схемы
оставлены лишь укороченные с 5'-конца цепочки ДНК. III цикл реакции подробно не описан, представлены лишь конечные продукты цикла: двухцепочечные ампликоны.
II цикл ПЦР.
В следующем цикле ПЦР происходит денатурация обеих дочерних молекул ДНК с образованием 4-х одноцепочечных молекул. Для удобства в схеме рассматриваются лишь две достроенные в ходе предыдущего цикла цепи ДНК, ограниченные со стороны 5'-конца. На этапе отжига к этим цепям присоединяются праймеры. К цепи, затравкой которой служил прямой праймер, присоединяется обратный праймер, и, наоборот, к цепи, инициированной обратным праймером, присоединяется прямой праймер. Далее на этапе элонгации синтезируются две новые комплементарные цепи, ограниченные с обеих сторон. В результате к концу II цикла ПЦР в реакционной смеси появляются молекулы ДНК, у которых одна из цепей ограничена с обеих сторон праймерами.
III цикл ПЦР.
В ходе III цикла ПЦР происходит денатурация продуктов II цикла, и к образовавшимся одноцепочечным молекулам ДНК (ограниченным с обеих сторон праймерами) достраиваются комплементарные цепи. В результате по завершении III цикла в реакционной смеси появляются 2-цепочечные ампликоны, у которых обе цепи ограничены с двух сторон праймерами.
Последующие циклы ПЦР.
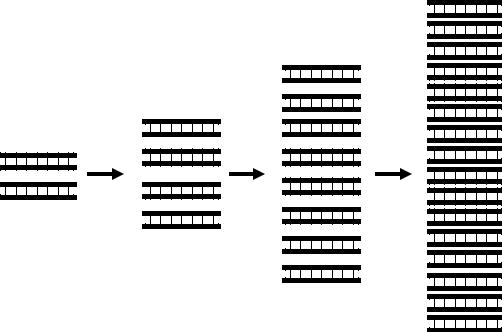
В последующих циклах ПЦР происходит репликация ампликонов. Каждая из цепей ампликона является матрицей для синтеза комплементарной цепи и, соответственно, каждый цикл ПЦР из одного ампликона синтезируются два. Таким образом, каждый цикл ПЦР приводит к удвоению числа содержащихся в реакционной смеси ампликонов (рис. 6). В результате в ПЦР рост числа ампликонов происходит в геометрической прогрессии и описывается формулой N = 2n, где N – число ампликонов в реакционной смеси, n – число циклов амплификации. К концу 30-го цикла количество ампликонов, полученных из одной молекулы ДНК микроорганизма, может достичь 1 млрд.
 …
…
III цикл
IV цикл
V цикл
VI цикл
Рис. 6. Динамика накопления ампликонов в циклах ПЦР.
Таким образом, метод ПЦР-диагностики возбудителей инфекционных заболеваний основан на многократной амплификации определенного участка ДНК микроорганизма. При этом даже из одной молекулы ДНК может быть получено практически неограниченное число ампликонов, что придает методу высокую чувствительность. Специфичность ПЦР-диагностики обеспечивается подбором праймеров, специфически присоединяющимся именно к ДНК выявляемого микроорганизма и ни к какой иной.
Амплификацию проводят в автоматическом режиме с помощью специальных приборов, амплификаторов (термоциклеров), которые, по сути, представляют собой программируемые термостаты. В амплификатор вставляют пробирки с реакционной смесью, и прибор осуществляет периодическое нагревание и охлаждение пробирок в соответствии с программой (рис. 7).

Рис. 7. Амплификатор (термоциклер).
Нагревание или охлаждение может осуществляться двумя способами. Чаще всего в амплификаторе есть специальный планшет из металла с высокой теплопроводностью, в который вставляют о пробирки с реакционной смесью. Под планшетом находятся элементы Пельтье, которые осуществляют нагрев или охлаждение планшета. В некоторых амплификаторах нагрев или охлаждение осуществляют с помощью потоков горячего или холодного воздуха. В этом случае пробирки вставлены в ротор и как бы висят в воздухе.
На 3-й стадии ПЦР-диагностики (после завершения амплификации) производится детекция образовавшихся в ходе ПЦР ампликонов. Эта задача решается методом электрофореза продуктов ПЦР в агарозном геле.
Электрофорез – разделение смеси молекул на отдельные фракции под действием электрического поля. Электрофорез продуктов ПЦР проводится в пластине из агарозного геля, помещенной между электродами. Возле края пластины, расположенного ближе к катоду, находятся лунки, куда вносят реакционную смесь с ампликонами. Под действием электрического поля молекулы ДНК движутся через гелевую пластину от катода к аноду, при этом длинные молекулы задерживаются в геле и потому мигрируют медленнее, чем более короткие. В результате происходит разделение смеси молекул ДНК по их размеру: фракции более коротких молекул ДНК мигрируют ближе к аноду, тогда как более длинные остаются ближе к катоду. Для приблизительной оценки размера молекул ДНК во фракциях используют готовую смесь из различных молекул ДНК известной длины: в ходе электрофореза эти молекулы разделяются по размеру и образуют своеобразную измерительную шкалу, по которой можно оценить размер получившихся в ПЦР ампликонов (рис. 8).
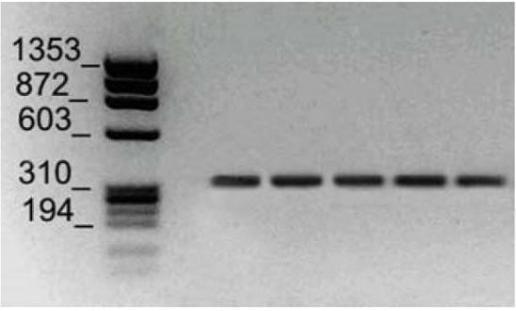
Рис. 8. Электрофорез ДНК в агарозном геле (окраска бромидом этидия, фото в ультрафиолете). Слева контрольная шкала из готовых фрагментов ДНК известной длины; справа полоски, образованные ампликонами, полученными в ПЦР.
После электрофореза гелевую пластину окрашивают раствором бромида этидия, флуоресцирующего красителя, имеющего свойство включаться в двухцепочечные ДНК. После окраски гелевую пластину просматривают в ультрафиолете, окрашенные бромидом этидия фракции ДНК выглядят как полоски розового цвета.
Оценка размера образовавшихся в ходе ПЦР ампликонов позволяет проконтролировать специфичность реакции, так как в реакционной смеси может содержаться балластная ДНК, не принадлежащая выявляемому микроорганизму. В балластной ДНК могут присутствовать нуклеотидные последовательности, комплементарные праймерам. В этом случае есть риск получения неспецифических ампликонов балластной ДНК. Размер полученных в ходе ПЦР ампликонов является доказательством того, что амплификации подвергся именно фрагмент ДНК выявляемого микроорганизма. Вероятность совпадения размеров ампликонов, полученных из ДНК выявляемого микроорганизма, и побочных продуктов ПЦР, крайне мала.
Положительным результатом реакции считается выявление четкой полосы, образованной фрагментами ДНК подходящей длины.
ПЦР С ОБРАТНОЙ ТРАНСКРИПЦИЕЙ (ОТ-ПЦР)
Большинство вирусов являются РНК-геномными (вирус гепатита С, вирусы гриппа, ВИЧ, вирусы группы клещевого энцефалита и т.д.), и их выявление методом ПЦР сопряжено с проблемой: ДНК-полимераза не может