Материал: Основные понятия и определения в иммунологии, Годовалов, Южанинова, 2017
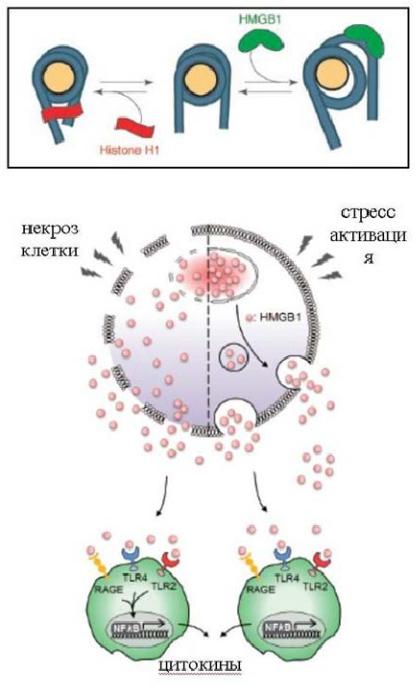
HMGB-1 (High mobility group box 1, амфотерин) ‒ убиквитарный, высоко консервативный, негистоновый ядерный белок. На верхнем рисунке в рамке схематично изображены некоторые функции HMGB-1 в ядре нормально функционирующей клетки. Взаимодействие HMGB-1 с нуклеосомой приводит к ослаблению связи ДНК с гистонами и повышению доступности ДНК для хроматинремоделирующего комплекса. (Гистон Н1 связываясь с ДНК в том же участке, приводит к конденсации хроматина (Bianchi et al., 2005)). В цитоплазме HMGB-1 препятствует агрегации белков, вызванной физическим или химическим воздействием, и определяет баланс между аутофагией и апоптозом.
HMGB-1 приобретает функции DAMP (нижняя часть рисунка), когда он оказывается во внеклеточном пространстве и становится доступным для рецепторов врождённого иммунитета на других клетках. Высвобождение HMGB-1 может происходить при некрозе и апоптозе клетки, а также путём активной секреции из макрофага при его активации LPS или провоспалительными цитокина-
ми (Lee et al., 2014).
15
внеклеточное
пространство
цитоплазма
передача
сигнала в клетку
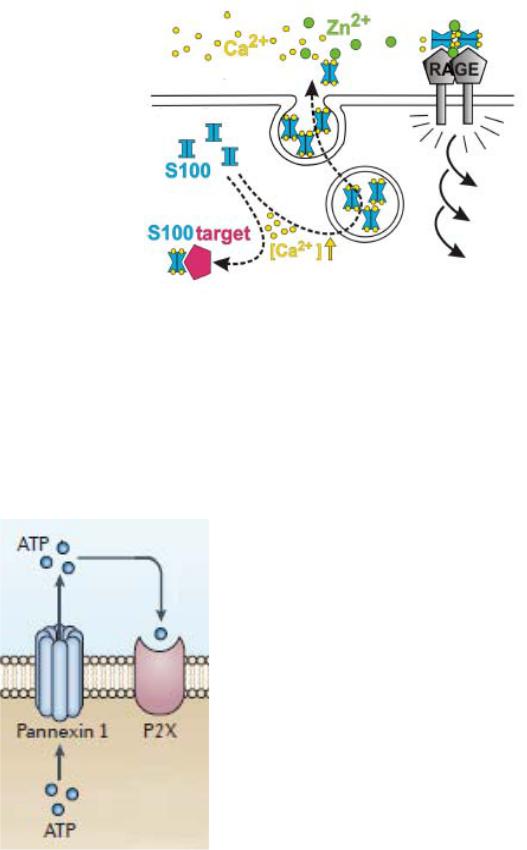
В здоровой клетке белки S100 функционируют как Ca2+-сенсоры и участвуют в передаче сигнала: при повышении концентрации Ca2+ в цитоплазме они связывают катион и взаимодействуют с другими белками (на рисунке они обозначены голубым цветом), изменяя их функциональное состояние.
Некоторые белки S100 становятся DAMPs, когда секретируются во внеклеточное пространство, связывают ионы Zn2+, димеризуются и взаимодействуют с соответствующим клеточным рецептором врождённого иммунитета, в данном случае с RAGE, от которого в клетку поступает активи-
рующий сигнал (по Marenholz et al., 2004).
Находясь в цитоплазме клетки, АТФ выполняет хорошо известную функцию носителя энергии. Однако АТФ может оказаться во внеклеточном пространстве в результате некроза клетки. Либо клетка может самостоятельно секретировать АТФ, находясь в интактном состоянии, в состоянии активации или при стрессе. Внеклеточно расположенная АТФ распознаётся различными пуринэргическими рецепторами и выполняет иные функции: 1) аутокринного и паракринного регулятора активности клеток и 2) функции DAMP. Так, при активации хемоаттрактантами нейтрофилы секретируют АТФ, которая аутокринно регулирует их хемотаксис. А АТФ, высвобождающаяся из умирающих клеток, усиливает фагоцитарную активность фагоцитов, расположенных рядом с погибающей клеткой (функции DAMP). На рисунке представлен один из механизмов секреции АТФ активированной клеткой. Высвобождение АТФ происходит через специальные каналы, состоящие из белка паннексина 1. P2X ‒ пуринергический рецептор, принадлежащий подсемейству P2X (Junger, 2011).
16
3.3. Антигены
Antigen=Antibody generation
Вещества, несущие признаки генетически чужеродной информации, могут нарушить генетическую индивидуальность (однородность) организма. Такие вещества присутствуют в микроорганизмах, чужеродных в генетическом отношении клетках и тканях (измененных в результате мутаций, зараженных вирусами, трансформированных опухолевых клетках и т.п.), а также в продуктах жизнедеятельности и макромолекулярных компонентах этих клеток (белках, полисахаридах, нуклеиновых кислотах и др.). То есть количество генетически чужеродных и потенциально опасных веществ бесконечно.
Для обеспечения распознавания и последующей (если необходимо) их элиминации в ходе эволюции возникает адаптивная иммунная система, способная формировать рецепторы к бесконечному количеству веществ в течение жизни одного организма.
Как уже говорилось в начале раздела 3, объекты, распознаваемые рецепторами клеток адаптивного иммунитета, мы называем антигенами. Сводя воедино это положение и рассуждения о ходе эволюционного процесса, можно сказать, что анти-
гены ‒ это вещества, несущие признаки генетически чужеродной информации, способные нарушить генетическую индивидуальность (однородность) организма и распознаваемые рецепторами клеток адаптивного иммунитета.
Антигены собственного организма называются аутоантигены. Реакция элиминации против аутоантигенов возможна при нарушении функций иммунной системы.
Иммуногены - субстанции, которые вызывают ответ адаптивной иммунной системы. Не все антигены являются иммуногенами, но все иммуногены - антигены.
Уникальность антигена определяется наличием у антигена антигенных детерминант ‒ эпитопов. Эпитоп ‒ часть макромолекулы, которая непосредственно распознается антителами, В- и Т-клеточными рецепторами. Большинство эпитопов имеют трехмерную структуру. Исключение ‒ линейные эпитопы, которые представляют собой первичную структуру протеина.
17
|
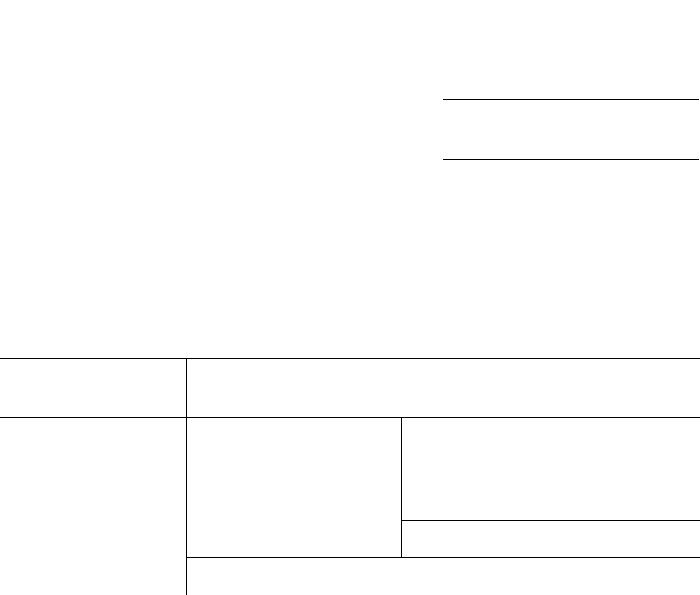
Основные отличия антигенов от РАМР |
|||
признаки |
|
антигены |
|
РАМР |
|
|
|||
|
|
|
|
|
наличие у человека |
|
да |
|
нет |
|
|
|
|
|
особенности строения |
|
имеют индивидуальное |
|
строение сходно у группы ор- |
|
строение |
|
ганизмов |
|
|
|
|
||
|
|
|
|
|
жизненно важные |
|
нет |
|
да |
структуры |
|
|
||
|
|
|
|
|
|
|
|
|
|
генетическая стабиль- |
|
нет: |
|
да (относительно редко мути- |
ность |
|
- антигенный дрейф, |
|
|
|
|
руют) |
||
|
|
- антигенный шифт |
|
|
|
|
|
|
|
|
|
|
|
|
АНТИГЕНЫ
как биологические как участники иммунологических реакций маркеры
определяют индивииммуногенность - споантигенная специфичность - сподуальность каждого собность индуцировать собность к взаимодействию со организма иммунный ответ строго определенным антителом,
либо BCR, либо TCR
ГАПТЕНЫ
ПОЛНЫЕ АНТИГЕНЫ
18
Классификация эпитопов 1. Линейные или секвенционные эпитопы представляют собой линейную по-
следовательность аминокислот, т.е. первичную структуру протеинов. Так как белки имеют сложную пространственную конфигурацию, они должны быть подготовлены к участию в иммунологических реакциях. Для этого клетки нашего организма разрушают третичную или четвертичную структуру белкового антигена в лизосоме на маленькие пептиды, которые распознаются рецепторами лимфоцитов.
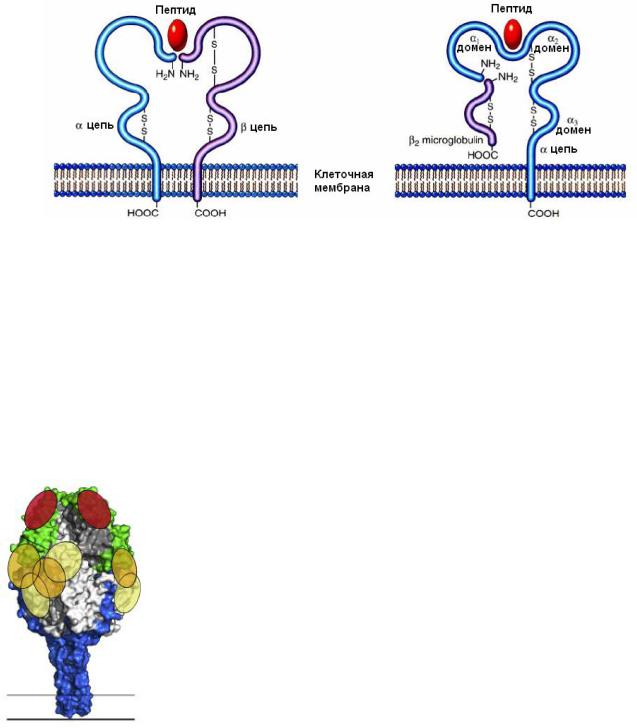
Пример линейных эпитопов. Клетка помещает линейный антиген (обозначены красным цветом) в молекулу МНС (major histocompatibility complex; на рисунке обозначен фиолетовыми и синими линиями). В таком виде антиген распознается Т-клеточным рецептором.
2. Конформационные ─ эптопы, образованные крупными полимерами, имеющими сложную пространственную организацию (третичная и четвертичная структура белков, крупные полисахаридные молекулы и т.д.). Мономеры антигена, контактирующие с рецептором, могут не следовать друг за другом.
Пример конформационных эпитопов. Показана 3D-модель F протеина респираторно-синцитиального вируса. Протеин встроен в оболочку вируса. Овалами показаны участки контакта антигенраспознающих участков нейтрализующих антител, специфичных к F протеину. Цвет овала кодирует эффективность нейтрализации протеина антителами: красный - максимальная, бежевый - средняя, желтый - слабая (Graham et al., 2015).
19