Материал: Основные понятия и определения в иммунологии, Годовалов, Южанинова, 2017
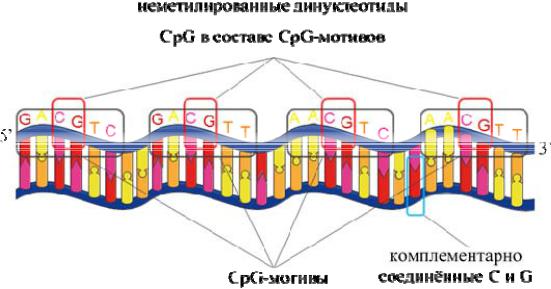
CpG-мотив ‒ это участок двуцепочечной ДНК с определённой последовательностью из 6 нуклеотидов. Все нуклеотиды в CpG-мотиве расположены на одной стороне двуцепочечной ДНК. CpG-мотив состоит из трёх компонентов: 1) центрально расположенного неметилированного динуклеотида CpG, в котором после цитидина (С) в направлении 5’-3’ следует гуанозин (G), а нуклеотиды разделены остатком фосфорной кислоты (р), 2) двух пуриновых остатков с 5′-конца и 3) двух пиримидиновых остатков с 3′-конца. Наиболее часто в геномах встречаются последовательности GACGTC, GACGTT, AACGTC, AACGTT. CpG-динуклеотиды не следует путать с комплементарно соединёнными C и G на противоположных цепях ДНК (Weaver et al., 2017).
CpG-мотивы с неметилированным цитидином содержатся в прокариотической ДНК и обуславливают её иммуностимулирующие свойства (Krieg et al., 1995). Следует отметить, что ДНК эукариот также содержит CpG-мотивы. Однако их количество у эукариот около 1 на 50 оснований, тогда как в прокариотической ДНК их намного больше ‒ примерно 1 на 16 оснований. Кроме того, практически все CpG-мотивы эукариот метилированы, что отменяет их иммуностимулирующие свойства (Kline et al., 2010).
10
Пептидогликан клеточной стенки грам-отрицательных бактерий заключён между внутренней и внешней мембранами. А на поверхности этих бактерий находится самый известный и хорошо изученный патогенассоциированный молекулярный паттерн ‒ липополисахарид (ЛПС; Lipopolysaccharide, LPS). Другое название этой молекулы, которое часто используется как его синоним, ‒ эндотоксин. Термин «эндотоксин» был введён Ричадом Пфайфером (коллега Р. Коха) при исследовании патогенности холерного вибриона. Оказалось, что, несмотря на иммунизацию подопытных животных возбудителем холеры, инокуляция микроба вызывала их смерть. Существенно, что в организме животных при этом не обнаруживалось живых вибрионов. Такой же исход экспериментов наблюдался при введении микробов, обезвреженных воздействием высокой температуры. Это означало, что какой-то термостабильный небелковый компонент, высвобождающийся из бактерии при её гибели, способен вызывать мощную воспалительную реакцию макроорганизма, приводящую к его смерти.
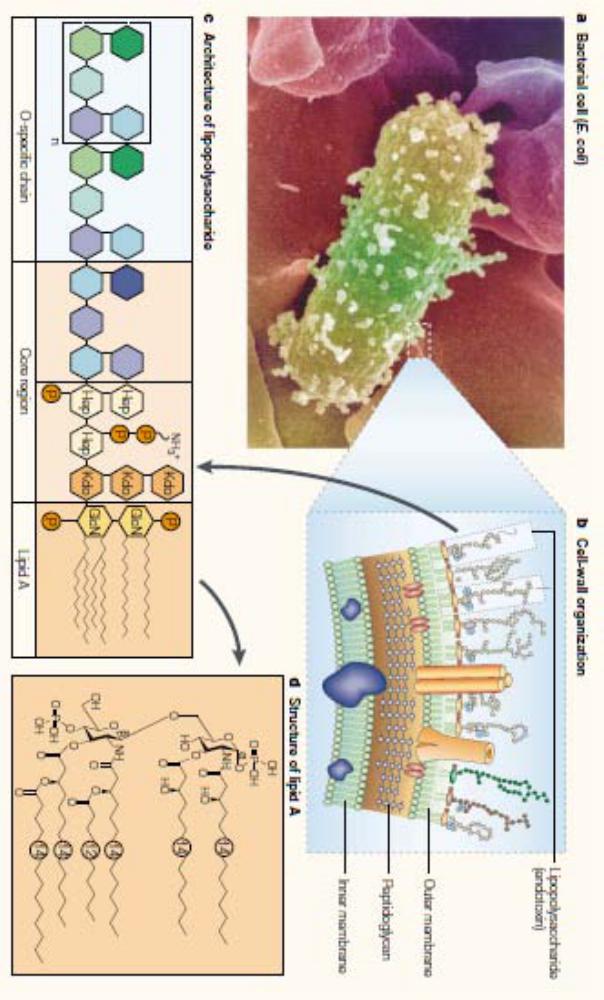
На рисунке (стр. 12 ) показана схема строения стенки грам-отрицательных бактерий на примере Escherichia coli. а ‒ внешний вид E. coli (электронная микрофотография). b ‒ поперечный срез клеточной стенки грам-отрицательной бактерии; указаны внутренняя мембрана (Inner membrane), слой пептидогликана (Peptidoglycan), расположенный в середине, и внешняя мембрана (Outer membrane), в которой заякорены молекулы липполисахарида (Lipopolysaccharide, сокр. LPS или ЛПС). с ‒ строение молекулы LPS. В молекуле выделяют О-специфическую цепь (O-specific chain), центральный регион (Core region) и липид А (Lipid A). Именно липид А обуславливает токсические и порогенные свойства LPS. d ‒ химическая структура липида А: GlcN ‒ D- глюкозамин, Hep ‒ L-глицеро-D-манно-гептоза, Kdo ‒ 2-кето-3-деокси-октулозоновая кислота, P ‒
фосфат. (Beutler et al., 2003).
Клетки и компоненты иммунной системы взаимодействуют с липополисахаридом по-разному. О-антиген распознаётся антителами (один из компонентов сыворотки крови) и В-клеточными рецепторами, то есть компонентами адаптивного иммунитета. На этом основано серологическое типирование видов и штаммов бактерий. Липид А взаимодействует с паттернраспознающими рецепторами врождённой иммунной системы (Park et al. 2009). Именно липид А обуславливает токсические и пирогенные свойства LPS.
Молекула LPS является примером того, что один и тот же объект может являться и антигеном и паттерном одновременно. Микроорганизмы как более сложно устроенные объекты микромира также одновременно являются и антигенами и паттернами.
11
12

3.2. Эндогенные сигналы стресса (damage associated molecular pattern, DAMP).
Потенциальные DAMPs являются компонентами нормально функционирующих клеток и тканей. Такие молекулы либо пассивно высвобождаются из клеток в случае повреждения последних, либо активно синтезируются и секретируются клетками в состоянии стресса и, в итоге, становятся доступными для рецепторов врожденного иммунитета.
Полли Матзингер впервые высказала идею о том, что работа иммунной системы заключается не столько в распознавании и удалении «чужого», сколько в обнаружении и ликвидации «опасности», возникающей при деструкции тканей и клеток организма (Matzinger P., 1994).
Полли Матзингер
1947
К молекулам собственного организма, которые приобретают свойства DAMP при стрессе или повреждении клеток и тканей, относятся:
1.Компоненты клеточного дебриса: белки теплового шока (БТШ), мембранные фосфолипиды, пуриновые метаболиты, семейство кальцийсвязывающих белков
S100, гистоны, HMGB1 и т.д.
2.Продукты синтеза активированных клеток: антимикробные белки (кателицидины, дефензины, нейротоксин эозинофилов), ИЛ-1, HMGB1 и т.д.
4.Мочевая кислота, кристаллы холестерина, β-амилоид, внеклеточная АТФ.
5.Молекулы, подобные МНС 1.
13
Белки теплового шока (heat shock proteins, HSP) это большая группа цитоплазматических белков, основная часть которых выполняет функции шаперонов (от англ. «chaperone» ‒ учитель, наставник, сопровождающий группу молодёжи), то есть белков, осуществляющих укладку или разборку полипептидов. Согласно современной классификации в группу HSP входят семейства белков HSPA (HSP70) и HSPH (HSP110), которые объединены в суперсемейство HSP70, семейства DNAJ (HSP40), HSP90/HSPC, HSPB (семейство маленьких белков теплового шока), а также шаперонины и связанные с ними белки. В каждом их этих семейств насчитывается до нескольких десятков членов. Номер в назывании белка указывает на его молекулярную массу в килодальтонах
(Kampinga et al., 2009).
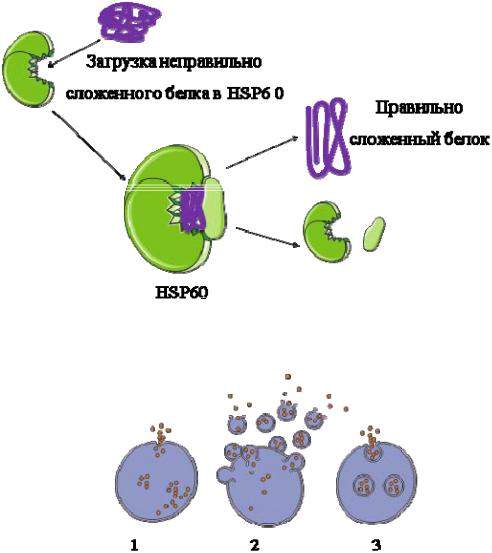
На верхнем рисунке показаны функции белка HSP60 в нормально функционирующей клетке. Некорректно сложенный белок (обозначен сиреневой линией) загружается в HSP60, камера внутри HSP60 закрывается, сложение белка изменяется, и он выгружается в цитоплазму (по https://www.ncbi.nlm.nih.gov/books/NBK26829/figure/A1105/?report=objectonly). Экспрессия HSP
повышается в результате физиологического стресса или физического/химического воздействия на клетку (Wu, 1995), то есть в ситуациях, когда число некорректно сложенных белков может увеличиваться.
HSP приобретают свойства DAMP's, когда оказываются вне клетки на её поверхности, либо во внеклеточном пространстве (Graner, 2016). На нижнем рисунке показаны варианты высвобождения HSP из клетки: 1 ‒ в результате некроза клетки, 2 ‒ в результате секреции (например, HSP70) в пузырьках с последующим их разрушением, 3 ‒ в эндолизосомах, которые сливаются с мембраной клетки, высвобождая HSP70 (по Mambula et al., 2007).
14