Материал: Основные понятия и определения в иммунологии, Годовалов, Южанинова, 2017

|
|
ПАЛЕОИММУНИТЕТ |
НЕОИММУНИТЕТ |
||
|
|
innate immunity |
adaptive immunity |
||
|
|
врожденный иммунитет, |
адаптивный иммунитет, |
||
|
|
неспецифическая резистентность |
лимфоцитарный иммунитет, |
||
|
|
|
приобретенный иммунитет |
||
|
|
|
|
||
1. |
Клетки |
I. работают, в основном, путём |
Т- и В-лимфоциты |
||
|
|
фагоцитоза: нейтрофилы, моно- |
|
|
|
|
|
циты/макрофаги, дендритные |
|
|
|
|
|
клетки; |
|
|
|
|
|
II. работают, в основном, путём |
|
|
|
|
|
экзоцитоза: эозинофилы, базо- |
|
|
|
|
|
филы, тучные клетки, NK- |
|
|
|
|
|
лимфоциты |
|
|
|
|
|
|
|
||
2. |
Рецепторы для |
PRR – паттерн-распознающие |
Т- и В-клеточные рецепторы |
||
распознавания |
рецепторы |
(TCR и BCR) |
|||
объектов |
|
|
|
|
|
|
|
|
более 1022 для BCR; |
||
3. |
Количество ва- |
десятки, сотни |
|||
риантов специ- |
|
более 10 |
22 |
для TCR |
|
фичностей рецеп- |
|
|
|||
|
|
|
|
||
торов |
|
|
|
|
|
|
|
|
|
||
4. |
Механизмы фор- |
зародышевые гены и структуры |
случайное объединение, не- |
||
мирования разно- |
|
точная стыковка генных сег- |
|||
образия рецепто- |
|
ментов, кодирующих актив- |
|||
ров |
|
ные центры |
|||
|
|
|
|
||
5. |
Что распознает? |
DAMP (син. алармины), РАМР |
антиген |
||
|
|
|
|
||
6. |
Распознавание |
есть |
есть |
||
и элиминация |
|
|
|
|
|
|
|
|
|
||
7. |
Иммунная па- |
нет |
есть |
||
мять |
|
|
|
|
|
|
|
|
|
||
8. |
Скорость вклю- |
немедленно, после обнаруже- |
начиная с 4-х суток после |
||
чения в защиту по- |
ния мишеней (PAMP, DAMP) |
контакта с АГ (необходима |
|||
сле распознавания |
|
пролиферация и дифферен- |
|||
объекта |
|
цировка лимфоцитов) |
|||
|
|
|
|
|
|
Иммунитет = распознавание + элиминация + иммунная память
5

3. Объекты распознавания
Объекты, которые распознаются клетками, классифицируются на основании того, какими рецепторами они распознаются.
Если в распознавании участвуют рецепторы врожденного иммунитета, то объект называется паттерн, что в переводе с английского языка означает "образец, модель, принцип организации чего-либо". А если объект распознается рецепторами адаптивного иммунитета, то мы называем его антиген.
Источником паттернов могут быть чужеродные организмы, тогда паттерны называются РАМРs (pathogen-associated molecular patterns). В случае поврежде-
ния клеток и тканей собственного организма некоторые их компоненты становятся паттернами и называются DAMPs (damage associated molecular patterns). Источ-
ником антигенов являются как чужеродные организмы и вещества, так и собственный организм.
Вещества, образующиеся в организме или поступающие в него извне, можно разделить на следующие три категории:
1) неорганические |
2) простые органические соеди- |
3) крупномолекулярные со- |
соединения |
нения, а также соединения, не |
единения, биополимеры жи- |
|
являющиеся продуктами обмена |
вотного, растительного и |
|
веществ (например, лекарствен- |
микробного происхождения |
|
ные препараты) |
|
|
|
|
КСЕНОБИОТИКИ ‒ инактивируются биохимиче- |
|
|
скими ферментными системами: системой микросо- |
ПАТТЕРНЫ И АНТИГЕ- |
|
мального окисления печени, конъюгированием ток- |
||
сических соединений с глюкуроновой кислотой и |
НЫ ‒ распознаются и утили- |
|
т.д. Выводятся почками, печенью, легкими, кожей. |
зируются иммунной системой |
|
|
|
|
6

3.1. Патогенассоциированные молекулярные паттерны (pathogen-associated molecular pattern, РАМР)
Это “маленькие” молекулярные мотивы, постоянно обнаруживаемые у патогенов и отсутствующие в организме-хозяина (человека). Эти молекулы для патогенов жизненно необходимы и не могут быть удалены или изменены при мутации (эволюционно консервативны, или постоянны). Распознавание PAMPs клетками нашего организма служит сигналом о внедрении не просто чужеродного, а биологически агрессивного агента.
Следует отметить, что РАМРs присутствуют не только у патогенных микроорганизмов, но и у представителей нормальной микрофлоры человека. Клетки иммунной системы не активируются РАМРs нормальной микрофлоры до тех пор, пока эти организмы находятся в своей экологической нише и физически недосягаемы для наших клеток. При транслокации за пределы ниши и контакте с клетками макроорганизма последние будут распознавать РАМРs комменсалов и активироваться.
Ч. Джэнуэй предположил, что рецепторы будут распознавать какие-то химические структуры, характерные для целого класса патогенов.
“Иначе просто не хватит генов!”
Чарльз Джэнуэй
1943—2003
Примеры некоторых РАМРs: мурамилдипептид, липополисахарид, флагеллин, липотейхоевая кислота, пептидогликан, нуклеиновая кислота (СрG), манноза, липопротеины, грибковые гликаны.
Свойства РАМР
1.отсутствуют у человека,
2.имеют сходное строение у группы организмов,
3.генетически стабильны (относительно редко мутируют),
4.жизненно важные структуры
7
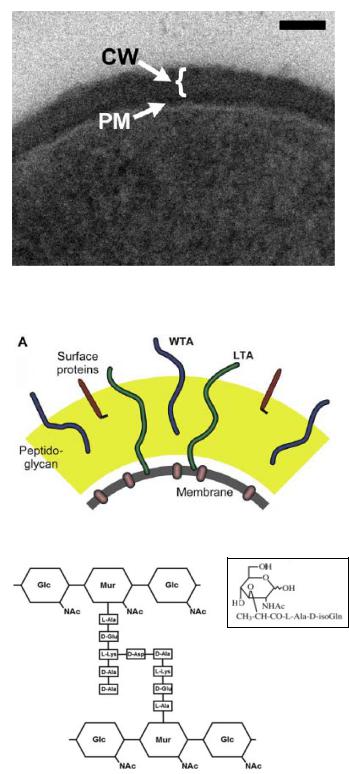
Относительные размеры компонентов клеточной стенки золотистого стафилококка (электронная микроскопия). PM ‒ плазматическая мембрана, CW ‒ клеточная стенка.
Линейка 50 нм (Matias et al., 2006).
Схема строения клеточной стенки грамположительных бактерий на примере золотистого стафилококка. Снизу вверх: плазматическая мембрана бактерии (Membrane), пептидогликан (Peptidoglycan), поверхностные белки (Surface proteins, заякорены в слое пептидогликана), тейхоевые кислоты, заякоренные в клеточной стенке (WTA, wall teichoic acid), липотейхоевые кислоты, заякорены в плазматической мембране бактерии (LTA, lipoteichoic acid) (Xia et al., 2010).
Пептидогликан состоит из цепи чередующихся гликанов: N-ацетилглюкозамина (Glc) и N-ацетилмурамовой кислоты (Mur), соединённых β-1,4 связями и перекрёстно соединённых пептидными цепочками (Johnson et al., 2016). В растущей бактериальной клетке пептидогликан подвергается постоянному ремоделированию, поэтому продукты его распада образуются постоянно. Они могут попадать в клетки нашего организма через специальные транспортные системы или из эндосом (FI2013). Минимальной структурной единицей пептидогликана является мурамилдипептид (см. вставку в рамке). Мурамилдипептид вызвает синтез провоспалительных цитокинов в клетках нашего организма после её заимодействия с внутриклеточным PRR ‒ NOD2 (Uehori et al., 2005).
8
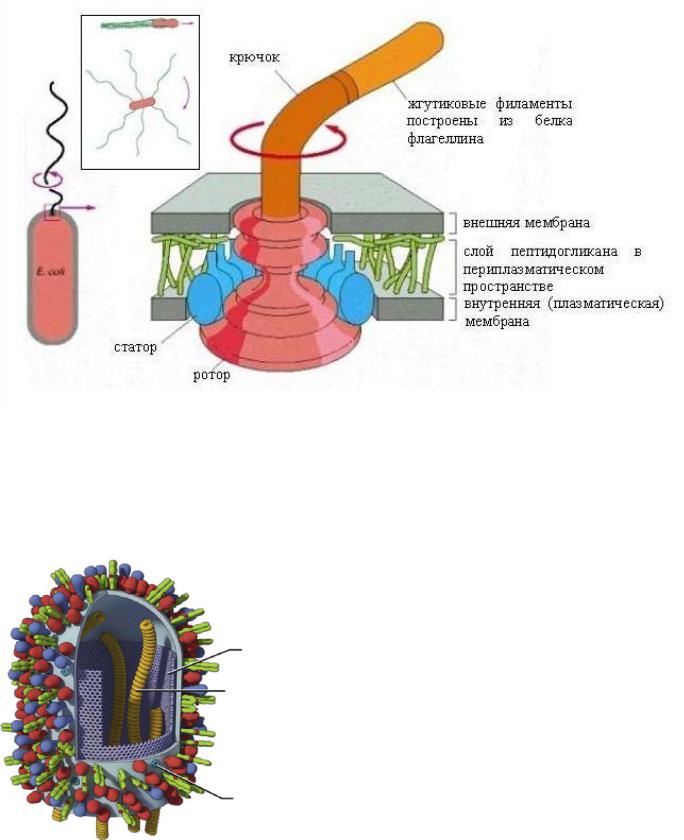
Жгутики бактерий построены из белка флагеллина, являющегося лигандом TLR5. Вставка в рамке: способы работы жгутиков и соответствующие им типы движения бактерии (указаны стрел-
ками). Из книги «Molecular Biology of the Cell» https://www.ncbi.nlm.nih.gov/books/NBK21054/.
белок матрикса
нуклеопротеин
SH (small hydrophobic)
протеин
На поверхности респираторносинцитиального вируса, который является основным возбудителем тяжёлых инфекций нижних дыхательных путей, находится F (от «fusion» ‒ слияние)-протеин. F- протеин необходим вирусу для проникновения в эпителиальные клетки хозяина и формирования синцития. Протеин может находится в двух конформационных состояниях: пре-F (функциональный; обозначен красным цветом) и пост-F (нефункциональный; обозначен синим цветом). Зелёные фигуры - G-гликопротеин
(Graham et al., 2015). F-протеин распозна-
ётся TLR4 на клетках макроорганизма, что вызывает их мощную реакцию в виде секреции провоспалительных цитокинов.
9