Материал: ОХТ в вопросах и ответах Ч2
обладает основными свойствами, CO2 имеет кислые свойства, а сама реак-
ция является реакцией нейтрализации. Учитывая природу веществ, можно с большой вероятностью предположить, что процесс не будет лимитиро-
ваться химической реакцией. Тогда скорость процесса определяется по уравнению диффузионной кинетики [3, с. 88], согласно которому для ин-
тенсификации процесса хемосорбции целесообразно увеличить поверх-
ность контакта фаз, давление, степень турбулентности контактирующих потоков и снизить температуру.
Вопрос. Какой будет технологическая схема МЭА-очистки?
Ответ. Очистка конвертированного газа от диоксида углерода осуществ-
ляется в соответствии со схемой, содержащей два основных аппарата аб-
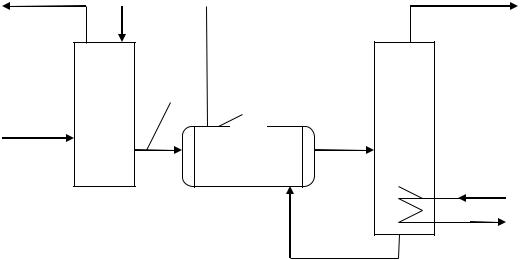
сорбер и десорбер (рис. 3.4).
H2 , N2 |
МЭА |
CO2 |
МЭАотр |
3 |
1 |
2 |
|
H2 , N2
CO2
4 Пар
МЭА
Рис. 3.4. Технологическая схема МЭА-очистки:
1 – абсорбер; 2 – теплообменник; 3 – десорбер, 4 – подогреватель
В схеме МЭА-очистки используется известный приём регенерация с рециклом, который позволяет наиболее эффективно использовать обору-
дование и сырьевые ресурсы. После поглощения СО2 отработанный рас-
31

твор моноэтаноламина (МЭАотр) подогревают в теплообменнике 2 и
направляют в десорбер 3, обогреваемый паром. При нагревании выделяет-
ся СО2 как побочный продукт, а раствор МЭА возвращают в абсорбер 1.
Схема работает с минимальными потерями сорбента раствора МЭА и получением дополнительного продукта CO2, который используют в дру-
гих производствах (для получения карбамида, «сухого» льда и т.д.).
Вопрос. В чём заключаются физико-химические основы синтеза аммиака?
Ответ. Синтез аммиака представляет собой каталитический процесс с об-
ратимой экзотермической реакцией, протекающей с уменьшением объёма:
N2 + 3H2 2NH3 + 103,6 кДж
Под физико-химическими основами процесса синтеза аммиака по-
нимают влияние параметров (температуры, давления) на равновесие, ско-
рость реакции и степень использования внутренней поверхности катализа-
тора. Эти знания позволяют предложить оптимальный режим синтеза ам-
миака и в последующем выбрать реактор, в котором обеспечивается мак-
симальная скорость реакции и достигается наибольшая степень превраще-
ния азотоводородной смеси.
Вопрос. Как выразить константу равновесия, если исходная азотоводород-
ная смесь имеет стехиометрический состав?
Ответ. Для стехиометрической смеси двух реагентов степени превращения каждого из них одинаковые. Если исходная стехиометрическая смесь со-
держала 1 моль N2 и 3 моля Н2, то при равновесной степени превращения xр останется молей N2 (1 xр) и Н2 3(1 xр), образуется 2xр молей NH3, а
общий объём уменьшится и станет равным (4 2xр) молей. Объёмные кон-
центрации для Н2, N2 и NH3 станут равными, соответственно,
1 xр |
, |
3(1 xр ) |
и |
2xр |
. |
4 2x |
|
4 2x |
|
4 2x |
|
р |
|
р |
|
р |
|
32

Равновесие реакции синтеза аммиака опишем уравнением:
|
|
|
P |
2 |
|
|
|
|
4 |
2 |
2 x |
|
x |
2 |
|
|||
K |
|
|
|
NH |
3 |
|
|
|
|
|
p |
|
p |
|
||||
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
p |
|
P |
|
|
P |
|
|
|
3 |
P |
|
|
|
|
4 |
||
|
|
|
N |
2 |
H |
2 |
равн |
|
|
|
|
|
1 |
x |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
p |
|
|||||
.
Вопрос. Как влияет температура и давление на равновесие реакции синте-
за аммиака?
Ответ. Согласно принципу Ле-Шателье понижение температуры и повы-
шение давления сдвигает равновесие реакции в сторону увеличения со-
держания аммиака. Зависимости хр(Т), хр(Р) приведены в [3, рис. 2, c. 18].
Вопрос. Как влияют температура и давление на скорость реакции синтеза аммиака?
Ответ. Для оценки влияния параметров на скорость обратимой реакции удобно воспользоваться уравнением (37) или (38) в [3, c. 27] в соответ-
ствии с которым, на неё влияют концентрация (давление) и температура.
Скорость реакции с увеличением температуры проходит через максимум,
как и для всех других обратимых экзотермических реакций (в [3, рис. 5, c.
28]). Чтобы достигнуть наибольшей степени превращения азотоводород-
ной смеси или максимального содержания аммиака в реакционной смеси при минимальном времени пребывания, процесс следует вести при макси-
мально возможной скорости. Катализатор синтеза аммиака активен при температурах 920–1100 К. Максимальная скорость реакции обеспечивает-
ся, если она осуществляется в режиме, близком к линии оптимальных тем-
ператур (ЛОТ).
С ростом давления возрастает равновесное содержание аммиака в реакционной смеси, что приводит к увеличению движущей силы обрати-
мой реакции, растёт также концентрация компонентов азотоводородной смеси. Поэтому давление влияет положительно на скорость синтеза амми-
ака.
Вопрос. Как выбирают оптимальное давление синтеза аммиака?
33
Ответ. При атмосферном давлении (0,1 МПа) превращение компонентов азотоводородной смеси очень мало. Промышленно важная область давле-
ний синтеза аммиака, при которых степень превращения будет более 20 %,
составляет выше 20 МПа. Техноэкономическое обоснование процесса по-
казало, что оптимальным будет осуществление процесса при давлении около 30 МПа. Более высокое давление резко увеличивает затраты на обо-
рудование и компрессию, а снижение давления увеличивает затраты на выделение аммиака.
Вопрос. Какой является структурная схема процесса синтеза аммиака?
Ответ. Выходящий газ из промышленного реактора содержит 16 об.%
аммиака. Для полноты использования азотоводородной смеси применяют фракционный рецикл (см. рис. 1.2, схема 7 на с.8).
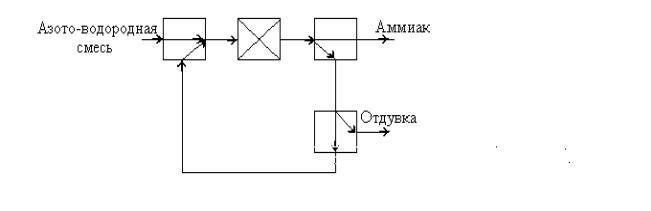
Рис 3.5. Подсистема синтеза аммиака
Для этого после реактора из реакционной смеси выделяют аммиак путём его конденсации, а не прореагировавшие H2 и N2 возвращают в реак-
тор. В поступающей смеси содержится до 1,2 % инертных веществ (СH4 и
Ar, вносимый с воздухом). При увеличении содержания инертных газов в цикле синтеза аммиака снижается концентрация водорода и азота, что приводит к уменьшению интенсивности процесса синтеза аммиака. С це-
лью недопущения накопления инертов в цикле синтеза аммиака содержа-
ние их в циркулирующем газе поддерживают на определённом уровне
34
(10 15 об. %) путём вывода (отдувки) части рециркулирующего газа (рис. 3.5). Отдувка составляет около 8 об.% от потока свежей азото-водородной смеси.
Вопрос. Какие реакторы можно предложить для эффективного проведения синтеза аммиака?
Ответ. Реакция синтеза аммиака – обратимая и экзотермическая. Макси-
мальная скорость реакции и высокая степень превращения обеспечивают-
ся, если процесс вести в режиме, близком к ЛОТ. Режим процесса, близкий к оптимальному, можно организовать в трубчатом реакторе с охлаждением или в многослойном реакторе с промежуточным теплообменом. Схемы ре-
акторов показаны на рис. 3.6.
Холодный газ |
в |
l |
l |
l |
|
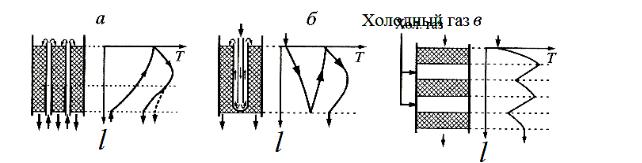
Рис. 3.6. Схемы реакторов синтеза аммиака и профили температур по высоте l:
а – с простыми противоточными трубками;б – с двойными трубками (трубками Фильда); в – многослойный реактор
Вопрос. Как осуществить синтез аммиака в трубчатом реакторе?
Ответ. В трубчатом реакторе тепло из реакционной зоны отводится к све-
жей реакционной смеси (рис. 3.6а). Реактор, в котором теплоотвод от ре-
акционной зоны осуществляется не посторонним носителем, а самой реак-
ционной смесью, носит название автотермического реактора. Катализатор располагают в межтрубном пространстве. Газ поступает в трубки, нагрева-
ется и затем входит противотоком в слой катализатора. По мере продвиже-
ния газа возрастает содержание аммиака z и одновременно происходит
35