Материал: ОХТ в вопросах и ответах Ч2
Ответ. Операционная модель представляет перечень основных стадий
(операций) переработки аммиачно-воздушной смеси в азотную кисло-
ту, в том числе, обеспечивающих протекание основных превращений,
таких как:
-подготовка аммиачно-воздушной смеси (АВС);
-окисление аммиака кислородом воздуха;
-окисление оксида азота до диоксида азота;
-охлаждение нитрозных газов;
-переработка оксидов азота в азотную кислоту;
-очистка отходящих газов от оксидов азота.
Вопрос. Из каких подсистем состоит функциональная схема производ-
ства азотной кислоты?
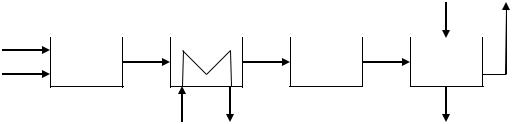
Ответ. Функциональная схема производства азотной кислоты включает в себя подсистемы подготовки АВС, окисления аммиака и утилизации тепла экзотермических реакции, охлаждения нитрозных газов, окисления монооксида азота в диоксид азота, абсорбции образующихся оксидов азота водой и очистки отходящих газов (рис. 4.1). На рис. 4.1 подсистема очистки отходящих газов не показана.
|
|
|
|
|
|
|
|
Отходящие |
|
|
|
|
|
|
|
|
газы |
Воздух |
2 |
|
3 |
|
4 |
|||
|
|
|
||||||
1 |
|
|
|
|||||
Аммиак
НNO3
Рис. 4.1. Функциональная схема производства азотной кислоты:
1 – подсистема подготовки АВС; 2 – подсистема окисления аммиака и утилизации тепла реакции; 3 – подсистема окисления оксида азота и охлаждения нитрозных газов;
4 – подсистема абсорбции диоксида азота
Вопрос. Каковы физико-химические основы процесса окисления аммиа-
ка?
41
Ответ. Реакция окисления аммиака относится к классу сложных, экзотер-
мических, каталитических реакций. При окислении аммиака в зависимо-
сти от условий ведения процесса можно получить оксид азота (ІІ), элемен-
тарный азот и оксид азота (І):
4NH3 |
+ 5O2 |
= 4NO + 6H2O + 904 кДж |
(4) |
4NH3 |
+ 3O2 |
= 2N2 + 6H2O + 1269 кДж |
(5) |
4NH3 |
+ 4O2 |
= 2N2O + 6H2O + 1105 кДж |
(6) |
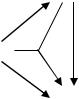
Схема превращения аммиака включает четыре химические реак-
ции, кроме (4), (5) в неё входят также следующие побочные реакции:
4NH3 + 6NO = 5N2 + 6H2O |
(7) |
2NO = N2 + O2 |
(8) |
так как при температуре процесса 1100–1200 К практически не образуется
NO по реакции (6).
NO
4
7 8
NH3
5
N2
Расчёты этих реакций показывают, что наибольшую термодинами-
ческую вероятность имеет реакция (5), характеризующаяся наибольшим изменением энергии Гиббса (∆G):
Реакция, (номер) |
(4) |
(5) |
(6) |
∆G, кДж/моль при Т= 298 К |
-246,21 |
-326,85 |
-274,75 |
Реакции окисления аммиака (4)–(6) протекают практически необра-
тимо, и поэтому направление процесса определяется соотношением ско-
ростей реакций. В отсутствии катализатора окисление аммиака идёт в ос-
новном с образованием азота по реакции (5). Для производства азотной
42
кислоты необходимо наиболее полное окисление аммиака по реакции (6),
поэтому применяют катализаторы, селективно (избирательно) ускоряю-
щие её. В качестве катализатора используется платина или сплав платины с палладием и родием. Теплоты, выделяющейся в результате реакции, до-
статочно, чтобы процесс протекал автотермично.
Процесс окисления аммиака относится к гетерогенно-
каталитическим процессам. Скорость реакции окисления аммиака при температуре проведения процесса 1073–1273 К значительно выше по сравнению со скоростью диффузионной стадии, вследствие слабой зави-
симости коэффициента диффузии от температуры по сравнению с темпе-
ратурной зависимостью константы скорости реакции. Поэтому скорость процесса лимитирует перенос вещёства и тепла из объёма газового потока к внешней поверхности катализатора, т.е. процесс протекает во внешне-
диффузионной области. В этих условиях нет необходимости применять катализатор с развитой внешней поверхностью, поэтому катализатор представляет собой сетку, сплетённую из металлической проволоки диа-
метром 0,09 мм. Благодаря сетчатой форме создаётся большая внешняя поверхность катализатора.
Вопрос. Как влияет температура и давление на процесс окисления аммиа-
ка?
Ответ. Повышение температуры приводит к увеличению скорости реак-
ции и возрастанию выхода оксида азота NO. При температуре процесса
1123–1193 К выход оксида азота достигает максимального значения.
Дальнейшее повышение температуры приводит к ускорению побочных реакций (7) и (8), имеющих более высокие значения энергии активации,
что приводит к снижению выхода оксида азота. Кроме того, при повыше-
нии температуры увеличиваются потери дорогостоящей платины.
43
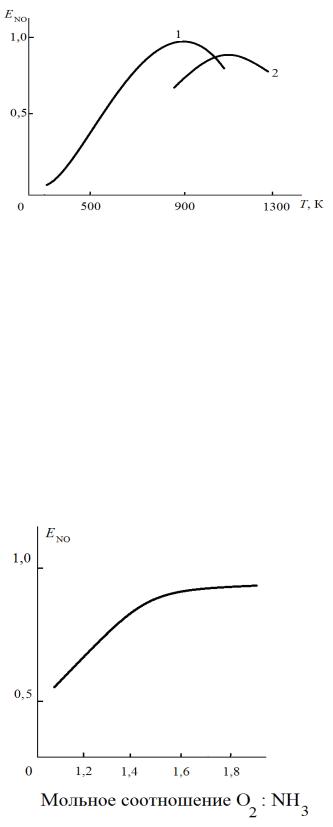
Рис. 4.3. Зависимость выхода оксида азота при окислении аммиака
от температуры:
1 – давление 0,1 МПа; 2 – давление 0,7 МПа
Вопрос. Какое количественное отношение О2:NH3 в аммиачно-
воздушной смеси (АВС) применяют при окислении аммиака?
Ответ. По стехиометрическому уравнению (1) отношение О2 : NH3 со-
ставляет 1,25, что соответствует содержанию аммиака в АВС 14,4 об. %.
При этом отношении выход оксида азота не превышает 60–70 % (рис. 4.4).
Рис. 4.4. Зависимость выхода оксида азота от мольного отношения О2:NH3
44
При увеличении отношения О2 : NH3 выход NO возрастает. Избыток кислорода необходим для того, чтобы поверхность катализатора всегда была покрыта кислородом. При недостатке кислорода окисление аммиака ведёт к образованию N2. Кроме того, аммиачно-воздушная смесь (АВС)
при концентрации аммиака выше 13,8 % (нижний предел взрываемости)
при атмосферном давлении становится взрывоопасной. Поэтому в произ-
водственных условиях содержание аммиака в аммиачно-воздушной смеси поддерживают в пределах 9,5–11,5 об. %, т.е. О2 : NH3 = 1,7–2.
Вопрос. Как зависит выход NO от времени пребывания аммиачно-
воздушной смеси на катализаторе?
Ответ. Скорость каталитического окисления аммиака по реакции (4)
очень высокая. Поэтому за короткое время контакта (порядка 10–4 с) ам-
миак полностью окисляется. При более длительном контакте газа с ката-
лизатором выход NO снижается за счёт протекания побочных реакций: (7)
– взаимодействия полученного оксида азота с аммиаком и (8) – разложе-
ния оксида азота. При времени пребывания меньше, чем 10–4 с наблюдает-
ся уменьшение выхода NO за счёт проскока через катализатор аммиака,
частично превращающегося в азот по реакции (7).
Вопрос. Что представляет собой контактный аппарат окисления аммиака?
Ответ. Контактный аппарат окисления аммиака (реактор) состоит из двух частей: верхней в виде усеченного конуса и нижней цилиндрической ча-
сти (рис. 4.5). Между ними на колосниках расположены катализаторные сетки. Природный газ сжигают в печи 1, а горючие газы из технологиче-
ского процесса – в реакторе-окислителе 2. Затем смесь газов с температу-
рой 1320 К поступает в газовую турбину 3 для привода компрессора и вы-
работки энергии. Далее газы с температурой 1020 К смешиваются с этилбензолом и направляются в реакторы дегидрирования (4 и 6). В теп-
45