Материал: ОХТ в вопросах и ответах Ч2
превращения и движущей силы обратимой реакции, равной (хр – х). Зави-
симость скорости реакции от давления проходит через максимум. Таким образом, необходимо некоторое избыточное давление для достижения максимальной скорости паровой конверсии метана.
С увеличением избытка водяного пара равновесие реакции сдвигает-
ся вправо, возрастает xр и движущая сила в кинетическом уравнении ско-
рости реакции. Однако создание избытка водяного пара больше двукрат-
ного нецелесообразно, так как при этом снижается концентрация метана и скорость его превращения.
Вопрос. Какая форма зерна катализатора в условиях паровой конверсии метана обеспечит высокую эффективность его использования при относи-
тельно небольшом гидравлическом сопротивлении слоя?
Ответ. При температуре процесса 1070 1200 К значения константы скоро-
сти и скорости реакции значительные, так что химическая реакция не мо-
жет быть лимитирующей стадией процесса. Если скорость реакция боль-
шая, при контакте реагентов с зерном катализатора они мгновенно реаги-
руют на его внешней поверхности.
Процесс паровой конверсии метана протекает во внешнедиффузион-
ной области, и согласно закону Фика интенсивность массопереноса про-
порциональна внешней поверхности зерна. Развитие у зерна катализатора внутренней поверхности и пористости становится бесполезным (даже вредным), так как это приводит к снижению его механической прочности.
Поэтому с точки зрения эффективности процесса конверсии метана, ми-
нимизации загрузки и затрат на катализатор в реакторе целесообразно ис-
пользовать катализатор с высокой внешней поверхностью (например, фи-
гурные зёрна в форме звездочек или колец). Одновременно при этом обес-
печивается значительная доля свободного объёма в слое катализатора, что будет способствовать снижению гидравлического сопротивления и соот-
26
ветственно уменьшению энергозатрат на транспортировку реакционной смеси через реактор.
Вопрос. Как выбирается оптимальное давление процесса паровой конвер-
сии метана?
Ответ. Оптимальное давление процесса паровой конверсии метана при размещении реактора в технологической схеме рассчитывается с учётом минимизации затрат на компримирование азотоводородной смеси. На ста-
дии синтеза аммиака оптимальное давление составляет 30 МПа. После па-
ровой конверсии метана в соответствии со стехиометрией реакции значи-
тельно увеличивается объём реакционной смеси.
Техноэкономические расчёты показали, чтобы избежать чрезмерных затрат на сжатие после реакции и минимизировать таким образом затраты на компримирование газа в производстве аммиака, давление на стадии конверсии метана должно составлять около 4 МПа. Такое давление не яв-
ляется оптимальным для процесса паровой конверсии метана, но оказыва-
ется выгодным для производства в целом. Здесь проявляется одно из свойств ХТС: оптимальные условия одиночного реактора отличаются от оптимальных условий реактора, включённого в технологическую схему.
Вопрос. Чем обоснована двухстадийная схема конверсии (превращения)
метана в трубчатой печи и в шахтном реакторе?
Ответ. Для более полного превращения метана по реакции:
CH4 + H2O CO + 3H2 (1)
следует увеличить температуру процесса. На 1-й ступени это сделать за-
труднительно из-за ограничений по температуре (материал реактора до-
пускает нагрев не выше 1070 1200 К). Поэтому необходима 2-я ступень конверсии. Она представлена адиабатическим реактором, или, как его называют, шахтным конвертором. Стенки его внутри футерованы огне-
упором. Необходимую температуру создают тем, что в реактор подают
27
воздух. Часть метана сгорает, и температура повышается до 1230 1280 К.
Высокая температура и разбавление реакционной смеси инертным газом
(азотом) способствуют сдвигу равновесия реакции (1) вправо.
С воздухом вводится и азот, необходимый для синтеза аммиака, так что 2-я ступень конверсии ещё выполняет функцию поставщика азота в производство аммиака. Количество подаваемого воздуха должно быть та-
ким, чтобы соотношение водород : азот соответствовало стехиометриче-
скому для синтеза аммиака, равным 3:1.
Вопрос. В чём заключаются физико-химические закономерности процесса конверсии оксида углерода?
Ответ. Конверсия СО каталитический процесс с обратимой экзотерми-
ческой реакцией:
СО + H2O CO2 + H2 + Qp
Смещению равновесия в правую сторону благоприятствуют умень-
шение температуры и использование избытка пара по отношению к СО.
Скорость конверсии СО как обратимой реакции, можно представить в виде выражения (37) или (38) в [3, с. 27], в соответствии с которым на неё влия-
ет концентрация и температура. Использование избытка пара по отноше-
нию к СО не только сдвигает равновесие реакции вправо, но также увели-
чивает движущую силу этой обратимой реакции (хр – х) и соответственно её скорость. Однако при чрезмерном избытке пара снижается концентра-
ция полезного реагента СО и скорость реакции падает. Оптимальное со-
отношение Н2О : СО 2. Давление не влияет на равновесие, но приводит к росту концентрации реагентов и скорости реакции. Процесс проводят под повышенным давлением, близким к давлению на стадии конверсии метана.
Чтобы достигнуть наибольшей степени превращения СО при мини-
мальном времени пребывания смеси в реакторе, процесс следует вести при
28
максимально возможной скорости. Максимально возможная скорость обеспечивается, если процесс осуществляется в режиме, близком к линии оптимальных температур (ЛОТ). Для конверсии СО не существует одного типа катализатора, одинаково активного при низких и высоких температу-
рах. Используют два типа катализаторов: один активен в области высоких температур 870–970 К и неактивен при низких температурах, другой – проявляет высокую активность уже при 750–800 К.
Вопрос. Как эффективно провести процесс конверсии СО в адиабатиче-
ских условиях?
Ответ. Если реакцию конверсии СО проводят в адиабатических условиях,
необходимо секционировать реакционную зону, т.е. расположить катали-
затор по слоям, и процесс проводить с промежуточным охлаждением ре-
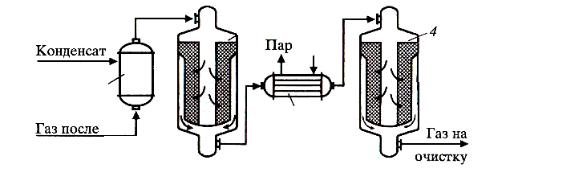
акционной смеси между слоями. Технологическая схема конверсии СО приведена на рис. 3.2.
2
1
3
конверсии сн4
Рис. 3.2. Технологическая схема процесса конверсии СО:
1 – увлажнитель; 2 – реактор с высокотемпературным катализатором; 3 – котелутилизатор; 4 – реактор с низкотемпературным катализатором
Диаграмма «Т–x» конверсии СО представлена на рис. 3.3. В первом слое реактора загружен высокотемпературный катализатор, а во втором низкотемпературный. Остаточное содержание СО не превышает 0,3–0,5 %.
29
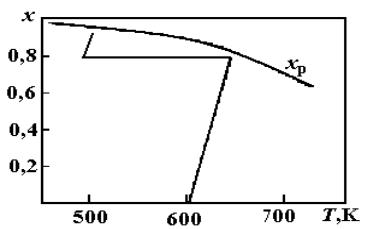
Рис. 3.3. Диаграмма «Т–х» конверсии СО:
х р – равновесные степени превращения СО; ломаная линия – режим конверсии
Вопрос. Зачем нужно чистить конвертированный газ от диоксида уг-
лерода?
Ответ. Конвертированный газ содержит до 20 об. % СО2. Необходимость очистки обусловлена следующими причинами:
-присутствие диоксида углерода в азотоводородной смеси снижает концентрации полезных компонентов, ухудшает работу стадии синтеза аммиака;
-диоксид углерод является побочным продуктом, имеет коммерче-
ское значение.
Диоксид углерода выделяют путём селективной абсорбции раство-
ром моноэтаноламина (МЭА) NH2CH2CH2OH.
Вопрос. В чём заключаются физико-химические основы процесса очистки конвертированного газа от диоксида углерода?
Ответ. Диоксид углерода абсорбируют 19 21 %-м водным раствором мо-
ноэтаноламина (МЭА-очистка):
2RNH2 + H2O + CO2 (RNH3)2CO3.
Это гетерогенный процесс с обратимой реакцией. МЭА как вещество
30