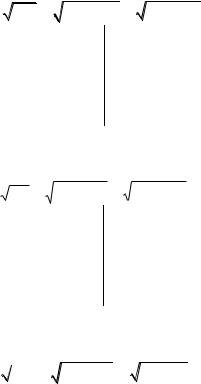
1) 4,47 10 4; 2) 4,8 10 5; 3) 6,9 10 5; 4) 7,8 10 3.
Больше всего концентрация ионов кальция в задаче № 4.
Правильный ответ: 4.
15. Запишем уравнение гетерогенного равновесия:
CdS |
Cd |
2 |
S |
2 |
|
|
(к) |
|
|
|
|
|
насыщ.р р |
Обозначим молярную концентрацию в насыщенном растворе через S (моль/л). В растворе сульфид кадмия полностью диссоциирован на ионы. Поэтому молярные концентрации
каждого иона – и |
Cd |
2 |
и |
S |
2 |
равны молярной концентрации |
|
|
содержащегося в растворе сульфида кадмия и также могут быть обозначены через S:
ПР [Cd 2 ] [S 2 ]; ПР S S; ПР S2 ; S 
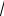 ПР.
ПР.
Можно посчитать значение растворимости, взяв ПР(CdS) из справочника.
ПР |
|
1,2 10 |
28 |
; |
|
|
|
|
|
|
|
|
|
|
|
|
(CdS) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
S |
ПР 1,2 10 |
28 |
1,09 10 |
19 |
(моль / л); |
|
|
|
|
|
|
|
|
S(г / л) S(моль / л) M |
CdS |
; |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
S(г / л) 1,09 10 |
19 |
144 |
157 10 |
19 |
1,57 |
10 |
17 |
г / л. |
|
|
|
|
|
|
Правильный ответ: 2.
16. Все эти соли состоят из двух ионов. Поэтому растворимость
каждой из них может быть найдена по формуле: |
S |
ПР , |
т.е. растворимость будет тем меньше, чем меньше величина ПР. Выпишем данные из таблицы произведений растворимости: