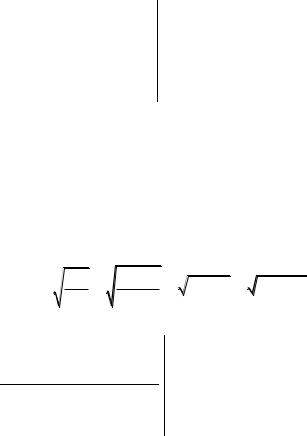объем раствора увеличивается в 2 раза, то концентрация ионов
Подставим найденные численные значения концентраций в выражение ПК:
Следовательно, раствор ненасыщенный, осадка не будет.
Правильный ответ: 1.
11. Запишем условие задачи. Дополнительно определим, будет ли выпадать осадок. Для этого из справочных таблиц возьмем значение ПР.
Дано: |
|
|
|
V |
|
|
10мл |
|
AgNO |
|
|
|
|
|
3 |
|
|
С |
AgNO |
0,01моль / л |
|
|
|
3 |
|
|
V |
|
5мл |
|
|
КС1 |
|
|
|
С |
КС1 |
0,1моль / л |
|
|
|
|
ПР |
AgCl |
1,7 10 |
10 |
|
|
|
|
|
ПК - ?
Решение:
Сначала запишем уравнение реакции ионного обмена:
Для возможного осадка хлорида серебра запишем уравнение гетерогенного равновесия:
AgCl |
(к) |
Ag |
|
Cl |
|
|
|
|
|
|
|
|
|
|
насыщ.р - р |
Запишем выражение ПР: Запишем выражение ПК:
Чтобы найти произведение концентраций ионов надо рассчитать концентрации ионов в растворе, полученном при смешивании двух исходных растворов. Общий объем раствора стал 15 мл.
Запишем уравнение диссоциации