Материал: Общая химия с физкалом
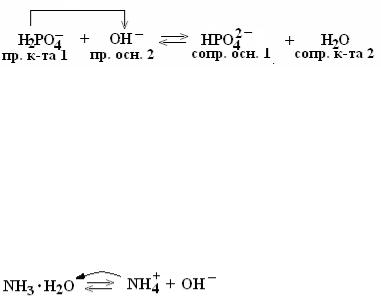
анион которой выполняет роль протолитической кислоты. Эта соль содержит больше ионов водорода.
NaH |
PO |
4 |
NaOH Na |
HPO |
4 |
H |
O |
2 |
|
2 |
|
2 |
|
(Обязательно другой, ставится знак
один компонент буфера превращается в
).
Na |
|
H |
PO |
|
Na |
|
OH |
|
2Na |
|
HPO |
2 |
H |
O |
|
4 |
|
|
|
4 |
|||||||||
|
|
2 |
|
|
|
|
|
|
|
|
2 |
|
Вывод:
эквивалентным
постороннее |
сильное |
основание |
|||
количеством |
соли |
Na |
2 |
HPO |
4 |
|
|
|
|
||
заменяется (слабого
протолитического основания), и рН раствора незначительно увеличивается.
Пример 3. Механизм буферного действия аммиачной буферной системы:
состав: это буферная система II типа, состоит из слабого основания и его соли
NH3 H2O NH4Cl
уравнения ионизации или диссоциации компонентов буферной системы:
NH |
Cl NH |
|
Cl |
|
|
|
|
|
|
|
||
4 |
|
|
|
|
|
|
|
|||||
4 |
|
|
|
|
|
|
|
|
|
|
|
|
при |
добавлении посторонней сильной кислоты, |
|||||||||||
например, НСl в действие вступит основание буфера: |
||||||||||||
NH |
H |
|
O HCl NH |
|
Cl |
|
H |
O |
|
|||
|
4 |
|
|
|||||||||
3 |
2 |
|
|
|
|
|
|
2 |
|
|
||
NH |
H |
O H |
Cl NH Cl H |
O |
||||||||
3 |
2 |
|
|
|
|
|
|
4 |
|
|
2 |
|
76
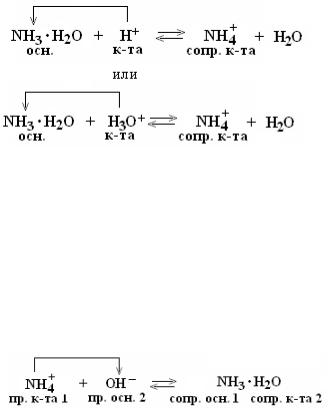
Вывод: |
посторонняя |
сильная |
кислота |
заменяется |
эквивалентным |
количеством |
соли |
NH4Cl |
(слабой |
протолитической кислоты), входящей в состав буфера, и рН раствора незначительно уменьшается.
при добавлении постороннего сильного основания, например NaOH в действие вступит соль буфера, содержащая
катион
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH4 |
, выполняющий роль протолитической кислоты: |
|||||||||||||
NH |
Cl NaOH NH |
H |
O NaCl |
|
|
|
||||||||
|
4 |
|
|
|
|
|
3 |
2 |
|
|
|
|
|
|
NH |
|
Cl |
|
Na |
|
OH |
|
NH |
H |
O Na |
|
Cl |
|
|
4 |
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
3 |
2 |
|
|
|
|
|
Вывод: постороннее сильное основание заменяется эквивалентным количеством слабого протолитического
основания |
NH |
3 |
H |
O |
, входящего в состав буфера, и рН |
|
2 |
|
раствора незначительно увеличивается.
5.5. Расчет буферной емкости
Для оценки способности буферной системы поддерживать постоянство рН при добавлении посторонних кислот и щелочей используются величины буферной емкости.
77

Буферная емкость является буферного действия.
Буферная емкость по
количественным выражением
кислоте |
Вк |
измеряется числом |
моль эквивалентов посторонней сильной кислоты, добавленных к 1 л раствора, чтобы изменить его рН на единицу.
|
|
э |
|
|
Вк |
сильн.к ты |
|
, моль экв/л |
|
рН Vбуфера |
|
|||
|
|
(л) |
||
Буферная емкость по основанию измеряется числом моль эквивалентов постороннего сильного основания, которые нужно добавить к буферу объемом 1 л чтобы изменить его рН на единицу.
|
|
э |
|
|
Во |
сильн.осн. |
, моль экв/л |
||
рН Vбуфера (л) |
||||
|
|
|
Чем выше емкость, тем больше кислоты или основания можно добавить к буферу, не вызывая сдвига рН.
5.6. Оценка буферной емкости и буферное отношение. Факторы, определяющие емкость буфера
Буферным отношением для БС I типа называют соотношение, стоящее под логарифмом в формуле для
вычисления рН:
рН рК |
|
lg |
ν |
|
к ты |
ν |
|||
|
|
|||
|
|
|
с к
.
Выражение
|
c |
/ |
k называют буферным отношением для буферных систем I |
||||||
|
|
||||||||
типа. |
|
|
|
|
|
|
|
||
|
|
|
Формула |
расчета |
pH |
для |
БС |
II |
типа |
pH 14 ( pKo lg vc ) . |
Выражение |
c / о называют |
|||||||
|
|
|
|
vo |
|
|
|
|
|
буферным отношением для буферных систем II типа.
Если буфер содержит больше протолитического основания, то его емкость по кислоте выше. При избытке
78
протолитической кислоты в буфере он будет иметь более высокую емкость по основанию.
На величину буферной емкости влияет ряд факторов:
-концентрация компонентов буфера;
-буферное соотношение;
-разведение буферного раствора.
С ростом концентрации компонентов буфера величина емкости так же возрастает. Большей емкостью обладает раствор, в котором концентрация компонентов буфера выше.
Величина буферного соотношения значительно влияет на емкость буфера. При буферном соотношении, равном 1, буферная емкость по кислоте равна емкости по основанию и значения их при этом максимальные: Вк=Во, если υк=υс.
При разведении буферного раствора буферная емкость уменьшается.
Интервал рН=рКа±1 называется зоной буферного действия.
ТЕСТОВЫЕ ЗАДАНИЯ К ТЕМЕ V. БУФЕРНЫЕ СИСТЕМЫ
Выберите один правильный ответ
1.БУФЕРНОЙ СИСТЕМОЙ I ТИПА ЯВЛЯЕТСЯ
1)пиридиновая
2)ацетатная
3)аммиачная
2.БУФЕРНОЙ СИСТЕМОЙ II ТИПА ЯВЛЯЕТСЯ:
1)фосфатная
2)ацетатная
3)аммиачная
4)гемоглобиновая
3.БУФЕРНОЙ СИСТЕМОЙ II ТИПА ЯВЛЯЕТСЯ
1)фосфатная
2)гидрокарбонатная
3)гемоглобиновая
79
4)анилиновая
4.БУФЕРНЫЕ СВОЙСТВА МОЖЕТ ПРОЯВЛЯТЬ СМЕСЬ ЭЛЕКТРОЛИТОВ
1)NaHCO3, CO2 ∙H2O
2)NH3 ∙H2O, NaCl
3)Na3PO4, K3PO4
4)CH3COOH, HNO3
5.К БУФЕРНЫМ СИСТЕМАМ ПЕРВОГО ТИПА ОТНОСИТСЯ КАЖДАЯ ИЗ ДВУХ БУФЕРНЫХ СИСТЕМ
1)аммиачная и гемоглобиновая
2)белковая и фосфатная
3) оксигемоглобиновая и пиридиновая
4)фосфатная и анилиновая
6.БУФЕРНЫЕ СВОЙСТВА МОЖЕТ ПРОЯВЛЯТЬ СМЕСЬ ЭЛЕКТРОЛИТОВ
1)КСl, СН3СООК
2)СН3СООН, СН3COONa
3)КСl, НСl
4)Na2СO3, NaOH
7.К БУФЕРНЫМ СИСТЕМАМ ВТОРОГО ТИПА ОТНОСИТСЯ КАЖДАЯ ИЗ ДВУХ БУФЕРНЫХ СИСТЕМ
1)аммиачная и пиридиновая;
2)гемоглобиновая и оксигемоглобиновая
3) фосфатная и аммиачная
4)белковая и анилиновая
8.БУФЕРНАЯ СИСТЕМА ВТОРОГО ТИПА СОСТОИТ ИЗ
1)слабого основания и соли этого основания и сильной кислоты
2)сильного основания и соли этого основания и сильной кислоты
3)сильного основания и соли этого основания и слабой кислоты
4)слабой кислоты и соли этой кислоты и сильного основания
80