Материал: Общая химия с физкалом
посторонних ОН— ионов и протолитического основания, которое нейтрализует посторонние Н+ (Н3О+) ионы в растворе. Пара протолитическая кислота – протолитическое основание в составе буферных систем отличаются на один протон Н+ .
Различают два основных типа буферных систем. Буферные системы I типа состоят из слабых кислот и
солей этих кислот и сильных оснований. К ним относятся:
Буферная |
Состав (кислота – |
Биологическая |
|||||||||
система I типа |
|
|
|
|
соль) |
|
|
|
роль |
||
Гидрокарбонат |
H |
CO |
NaHCO |
Действует в крови, |
|||||||
|
|
||||||||||
ная |
|
2 |
|
|
3 |
|
|
|
3 |
дыхательном цикле |
|
|
|
|
|
|
|
|
|
|
|||
Фосфатная |
NaH2PO4 Na2HPO4 |
Действует в крови, |
|||||||||
ЖКТ |
|||||||||||
|
|
|
|
|
|
|
|
|
|
||
Белковая |
Pt |
/ COOH |
Pt |
/ COONa |
Действует в крови, |
||||||
\ NH |
|
|
\ NH |
|
коже, слюне |
||||||
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
||||
Гемоглобинова |
HHb-KHb |
|
|
|
|
Действует в крови |
|||||
я |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
||
Оксигемоглоби |
HHbO2 |
KHbO2 |
|
Действует в крови |
|||||||
новая |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
Этой БС нет в |
|
Ацетатная |
CH |
COOH CH |
COONa |
организме. Она |
|||||||
|
|||||||||||
3 |
|
|
|
|
|
3 |
|
|
используется для |
||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
анализов |
|
Буферные системы II типа состоят из слабого основания и соли этого основания и сильной кислоты. К ним относятся:
Буферная система II типа |
Состав (основание – соль) |
|||
|
|
|
|
|
Аммиачная |
NH |
H |
O NH |
Cl |
|
3 |
2 |
4 |
|
|
|
|||
Анилиновая |
C6 H5 NH2 H2O C6 H5 NH3Cl |
|||
|
|
|||
Пиридиновая |
C5H5 N H2O C5H5 NHCl |
|||
|
|
|
|
|
Среди этих буферных систем биологическую роль играет только аммиачная БС, которая действует в выделительной системе.
71

5.2. Расчет рН буферных систем I типа
Для расчета рН буферных систем I типа используется следующая формула:
I тип |
рН рК |
|
lg |
νсоли |
; |
а |
|
||||
|
|
|
νк ты |
||
|
|
|
|
||
где: |
рКа = -lgКа |
|
|
|
|
Ка – константа ионизации слабой кислоты буферной |
|||||
системы. |
|
|
|
|
|
ν = СV или |
э Сэ V , т.е. число моль или моль |
||||
эквивалентов. |
|
|
|
|
|
5.3. Расчет рН и рОН буферных систем II типа
Для расчета рОН буферных систем II типа используется
формула:
рОН рК |
|
lg |
С |
соли |
V |
|
|
|
|
соли |
. |
||||
осн |
C |
|
V |
||||
|
|
|
|
||||
|
|
|
осн |
|
|||
|
|
|
|
|
осн |
|
|
Для расчета рН буферных систем II типа используется формула:
II тип
рН (рК |
осн |
lg |
|
|
νсоли )
νосн
,
где: рКb = -lgКb
К – константа ионизации
ν = СV или эквивалентов.
слабого основания буферной системы.
|
э |
э |
V , т.е. число моль или моль |
|
С |
5.4. Механизм буферного действия
Буферным действием называют способность данной системы сохранять постоянство рН при добавлении сильных кислот или оснований. Сущность механизма буферного действия заключается в том, что компоненты буфера вступают в химическое взаимодействие с ионами Н+ и ОН- посторонних кислот и оснований и переводят их в связанное состояние, т.е в состав малодиссоциированных электролитов. Реакции носят характер протолитических. В буферных системах I типа, состоящих из слабой кислоты и соли этой кислоты и сильного
72
основания, роль протолитической кислоты выполняет кислота буфера, а роль протолитического основания выполняет анион соли.
Буферная |
|
Состав |
Протоли- |
Протолитическое |
||
система |
|
тическая |
||||
(кислота – соль) |
основание |
|||||
I типа |
кислота |
|||||
|
|
|
|
|||
Гидрокарбо |
H |
CO |
NaHCO |
Н2СО3 |
НСО3- |
|
натная |
|
|||||
2 |
3 |
3 |
|
|
||
|
|
|
|
|
||
Фосфатная |
NaH2PO4 |
Na2HPO4 |
Н2РО4- |
НРО42- |
||
Белковая |
Pt / COOH Pt / COONa |
Pt / COOH |
Pt / COO |
|||
|
\ NH2 |
\ NH2 |
\ NH 2 |
\ NH 2 |
||
Гемоглобин |
|
HHb-KHb |
HHb |
Hb- |
||
овая |
|
|
||||
|
|
|
|
|
||
Оксигемогл |
HHbO2 |
KHbO2 |
HHbО2 |
HbО2- |
||
обиновая |
|
|||||
|
|
|
|
|
||
Ацетатная |
CH3COOH CH3COONa |
СН3СООН |
СН3СОО- |
|||
В буферных системах II типа,состоящих из слабого основания и соли этого основания и сильной кислоты, роль протолитической кислоты выполняет катион соли, а роль протолитического основания – основание буфера
Буферная |
|
Состав |
|
Протоли- |
Протоли- |
|||||
система |
|
|
тическая |
|
тическое |
|||||
(основание – соль) |
|
|||||||||
II типа |
кислота |
|
основание |
|||||||
|
|
|
|
|
||||||
Аммиачная |
NH |
H |
O NH |
Cl |
NH4 |
|
NH3 H 2O |
|||
|
3 |
2 |
4 |
|
|
|||||
Анилиновая |
C6 H5 NH2 H2O C6 H5 NH3Cl |
C |
H |
NH |
3 |
|
C6 H5 NH2 H 2O |
|||
|
|
|
|
|
6 |
5 |
|
|
|
|
Пиридиновая |
C5H5 N H2O C5H5 NHCl |
C5 H 5 NН+ |
C5 H5 N H 2O |
|||||||
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
Рассмотрим алгоритм записи механизма буферного действия.
Пример 1. Механизм буферного действия гидрокарбонатной буферной системы
Описание механизма буферного действия производится по следующему алгоритму:
записывается состав буферной системы
H2CO3 NaHCO3 ;
73
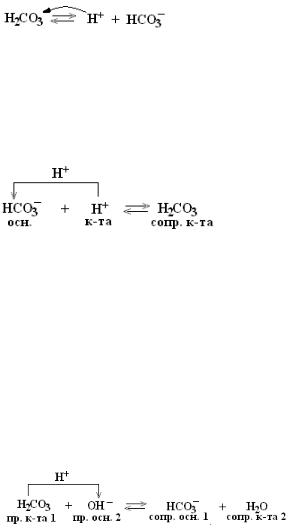
состояние компонентов буферной системы в водной среде отражают уравнения ионизации или диссоциации
компонентов БС. H2CO3 – слабая кислота, процесс ее распада
на ионы обратим – ионизация (ставим знак
).
NaHCO |
3 |
|
–
сильный электролит, диссоциирует нацело (ставим знак |
). |
Ионизация двухосновной угольной кислоты идет по первой ступени:
NaHCO |
|
Na |
|
HCO |
|
3 |
|
3 |
|||
|
|
|
|
при добавлении посторонней сильной кислоты, например, НСl в действие вступит соль буфера, т.к. она содержит анион, выполняющий роль протолитического
основания.
NaHCO |
3 |
HCl H |
CO |
3 |
NaCl |
|
2 |
|
|
Na |
|
HCO |
|
H |
|
Cl |
|
H |
CO |
|
Na |
|
Cl |
|
|
3 |
|
|
3 |
|
|
||||||||
|
|
|
|
|
|
|
2 |
|
|
|
|
|
Таким образом, посторонняя сильная кислота заменяется эквивалентным количеством слабой протолитической кислоты, входящей в состав буфера, и рН раствора незначительно уменьшается;
при добавлении постороннего сильного основания, например NaOH в действие вступит кислота буфера, т.к. с точки зрения протолитической теории кислота, как донор протонов,
служит для связывания |
OH |
|
посторонней щелочи; при этом |
|
образуется анион соли, входящей в состав буфера, выполняющий роль слабого протолитического основания.
|
|
H |
CO |
3 |
NaOH NaHCO |
3 |
H |
|
O |
||||||
|
|
2 |
|
|
|
|
|
|
|
|
2 |
|
|||
H |
CO |
Na |
|
OH |
|
Na |
|
HCO |
|
H |
O |
||||
|
|
|
3 |
||||||||||||
2 |
3 |
|
|
|
|
|
|
|
|
|
2 |
|
|
||
74
Таким образом, постороннее сильное основание заменяется эквивалентным количеством соли (слабого протолитического основания), входящей в состав буфера, и рН раствора незначительно увеличивается.
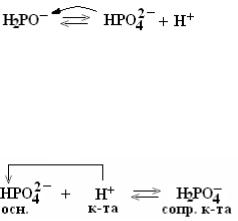
Пример 2. Механизм буферного действия фосфатной буферной системы:
состав фосфатной буферной системы:
NaH PO |
4 |
Na HPO |
4 |
2 |
2 |
уравнения ионизации буферной системы:
;
или диссоциации компонентов
NaH |
PO |
4 |
|
|
2 |
|
|
Na |
HPO |
4 |
|
2 |
|
|
|
Na |
|
H |
PO |
|
||
|
4 |
|||||
|
|
|
2 |
|
||
2Na |
|
HPO |
2 |
|||
|
4 |
|||||
|
|
|
|
|
|
|
при добавлении посторонней сильной кислоты, например, НСl в действие вступит та соль буфера, анион
которой содержит меньше ионов водорода. Анион
HPO |
2 |
|
4 |
||
|
выполняет роль протолитического основания.
Na |
HPO |
4 |
HCl NaH |
PO |
4 |
NaCl |
|
|
|
|
|
|||||||||||
2 |
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
||
2Na |
|
HPO |
2 |
H |
|
Cl |
|
Na |
|
H |
PO |
2 |
Na |
|
Cl |
|
||||||
|
4 |
|
|
|
4 |
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
||
Вывод: посторонняя сильная кислота заменяется эквивалентным количеством слабой протолитической кислоты
(соли
NaH |
PO |
4 |
2 |
|
), входящей в состав буфера, и рН раствора
незначительно уменьшается.
при добавлении постороннего сильного основания, например NaOH в действие вступит та соль буфера ( NaH2PO4 ),
75