Материал: Неорганическая химия - курс лекций-презентаций

Вопросы
Где применяются аммиак и соли аммония?
Как очистить оксид азота (II) от примеси оксида
азота (IV)?
Какие химические процессы протекают при
получении азотной кислоты из аммиака?
Каковы химические свойства азотной кислоты?
Объяснить валентность азота в азотной кислоте. Написать ее структурную формулу.
В каком количестве нитрата аммония содержится столько же азота, сколько его содержится в 17 кг
нитрата натрия? (Ответ: 8 кг.)

Общая характеристика подгруппы бора
Главную подгруппу III группы (подгруппы бора) составляют элементы бор, алюминий, галий, индий и таллий.
Все они относятся к р-элементам.
Их атомы на внешнем энергетическом уровне содержат по три электрона …s2р1-состояний, чем объясняется сходство в ряде свойств.
В химических соединениях эти элементы проявляют степень окисления, равную +3 (бор также и –3), хотя для таллия более устойчивой является степень окисления +1.
Металлические свойства элементов подгруппы бора выражены значительно слабее, чем у элементов подгруппы бериллия.
Так, элемент бор, у атомов которого электроны расположены на двух энергетических уровнях, относится к неметаллам.

Общая характеристика подгруппы бора
Внутри подгруппы с возрастанием заряда ядра (а следовательно, и числа энергетических уровней) металлические свойства усиливаются.
Алюминий – уже металл, но не типичный.
Его гидроксид обладает амфотерными свойствами.
У таллия более сильно выражены металлические свойства, а в степени окисления +1 он близок к металлам I группы.
Все элементы подгруппы бора образуют оксиды типа R2O3 (R – элемент).
Им отвечают гидроксиды состава R(OH)3.
Исключая бор, в водных растворах элементы могут находиться в
виде гидратированных ионов R3+.
Из металлов главной подгруппы III группы наибольшее значение имеет алюминий.
Алюминий
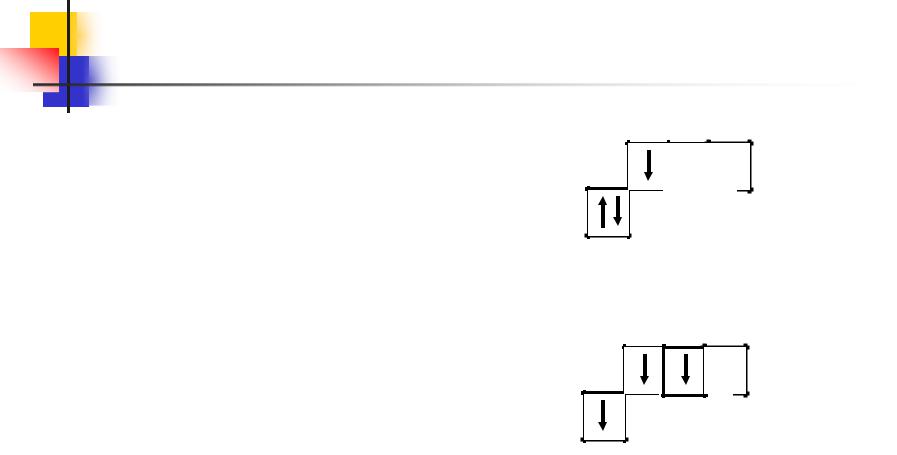
Запишем электронно-графическую формулу атома алюминия в нормальном состоянии:
13Al 1s2 2s2 2 p6 3s2 3 p1
Возбужденное состояние:
13 Al* 1s2 2s2 2 p6 3s1 3 p2
В' =1 |
3р |
3s |
В' =3 |
3р |
3s |
Степень окисления алюминия +3 :

Нахождение в природе
Среди металлов по распространенности в природе алюминию принадлежит первое место.
Содержание алюминия в земной коре составляет 8,8% по массе.
Важнейшие природные соединения алюминия:
алюмосиликаты,
бокситы,
корунд,
криолит.