Материал: Неорганическая химия - курс лекций-презентаций

Триада железа
Однако они могут отдавать электроны и с Зd-орбиталей второго снаружи уровня.
Поэтому в своих устойчивых соединениях эти элементы проявляют степени окисления +2 и +3.
Образуют оксиды состава RO и R203 (R – элемент). Им соответствуют гидроксиды состава R(OH)2 и R(OH)3.
Для элементов триады (семейства) железа характерна особенность присоединять нейтральные молекулы, например оксид углерода (II), оксид азота (II).
Кобальт и никель менее реакционноспособны, чем железо.
При обычной температуре они устойчивы к коррозии на воздухе, в воде и в различных растворах.
Разбавленные соляная и серная кислоты легко растворяют
железо и кобальт, а никель – лишь при нагревании. Концентрированная азотная кислота все три металла
пассивирует.

Триада железа
Металлы семейства железа при нагревании взаимодействуют с кислородом, парами воды, галогенами, серой, фосфором, кремнием, углем, бором.
Наиболее устойчивыми являются соединеняя железа (III), кобальта (II) и нииеля (II).
Железо, кобальт и никель в ряду стандартных электродных потенциалов расположены до водорода, платиновые металлы – после.
Поэтому первые распространены в природе в виде соединений (оксиды, сульфиды, сульфаты, карбонаты), в свободном состоянии встречаются редко – в виде железных метеоритов.

Триада железа
Платиновые металлы встречаются только в свободном состоянии.
По распространенности в природе за железом следует никель, а затем кобальт.
Соединения элементов семейства железа в степени окисления +2 очень сходны между собой.
В состоянии высших степеней окисления проявляют окислительные свойства.
Железо, кобальт, никель и их сплавы –важные материалы современной техники.
Но наибольшее значение имеет железо.

Нахождение в природе
Содержание железа в земной коре составляет 4÷5 % по массе и оно встречается в виде минералов:
Магнитный железняк (магнетит) – Fe3O4
(FeO·Fe2O3);
Красный железняк (гематит) – Fe2O3;
Бурый железняк (сидерит) – 2Fe2O3 3Н2О;
Шпатовый железняк - FeСO3;
Железный колчедан (пирит) – FeS2.
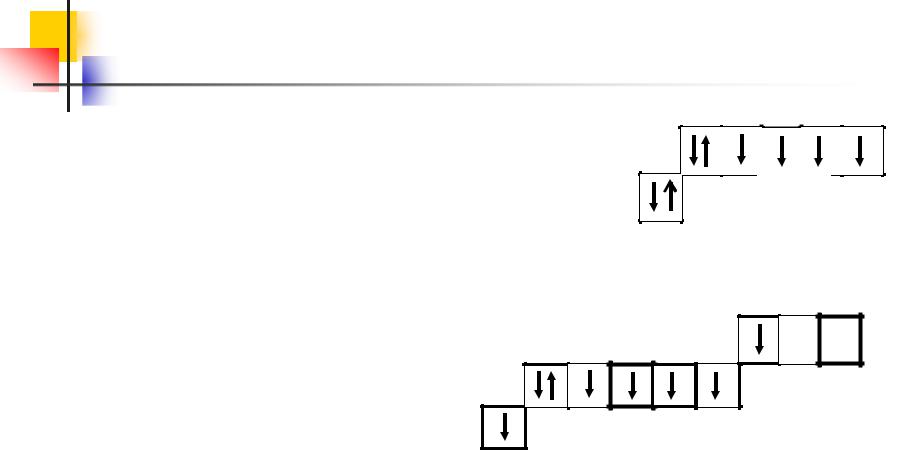
 атома железа
атома железа