Материал: Неорганическая химия - курс лекций-презентаций
Марганец
Запишем электронно-графическую формулу
атома марганца в нормальном состоянии:
25 Mn 1s2 2s2 2 p6 3s2 3 p6 4s2 3d 5 |
3d |
|
в возбужденном состоянии: |
В' =5 |
|
4s |
|
|
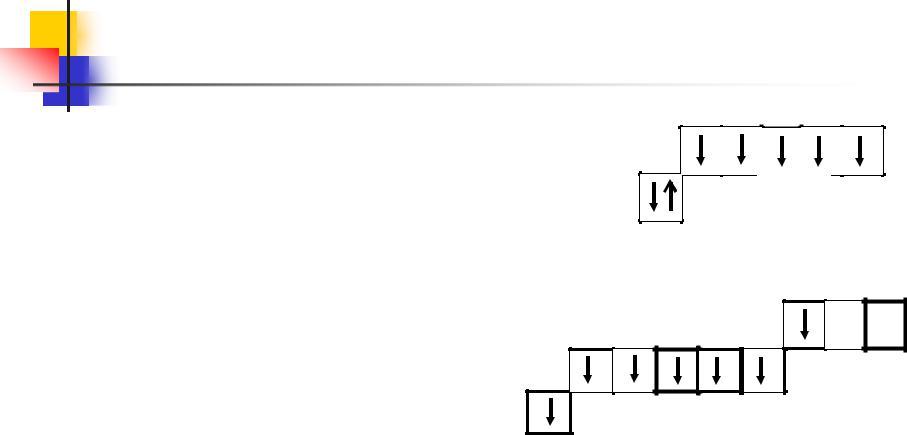
25 Mn* 1s2 2s2 2 p6 3s2 3 p6 4s13d 5 4 p1 |
|
|
|
|
4p |
3d |
|
В' = 7 |
|
|
|
4s |
|
|
Степени окисления марганца в |
|
|
соединениях: |
|
|
Mn+2, Mn+3, Mn+4, Mn+6 ,Mn+7. |
|
|

Нахождение в природе
Содержание марганца в земной коре составляет 0,1 % по массе и он встречается в виде минералов:
пиролюзита – MnO2;
браунита – Mn2O3;
гаусманита –Mn3O4;
марганцевого блеска – MnS.
По запасам руд с высоким содержанием
марганца наша страна занимает первое
место в мире.

Получение
Марганец получают карботермическим
или силикотермическим методами –
восстановлением кремнием при высокой температуре:
MnO2 +С t →Mn +СO2 ↑.
MnO2 +Si t →Mn +SiO2 .
+4
1 Mn +4e = Mn0 , в−ие,
+4
1 Si0 −4е = Si, о−ие.

Получение
Чистый металл получают электролизом раствора соли MnCl2
(см. тему «Электролиз»).
Для этого руду восстанавливают до соединений двухвалентного марганца и
растворяют в кислоте.

Физические свойства
Марганец –серебристо-белый твердый и хрупкий металл.
В зависимости от температуры кристаллизации он имеет четыре модификации.
Ниже 7070С устойчив αMn , имеющий сложную структуру, что и обусловливает его
хрупкость.
На воздухе марганец покрывается тонкой оксидной пленкой, защищающей его от дальнейшего окисления даже при нагревании.