Материал: Неорганическая химия - курс лекций-презентаций

Азот. Химические свойства
Поскольку на внешнем энергетическом уровне атома азота находится 5 электронов, то он проявляет степени окисления –3 и +5, а также +4, +3, +2,
+1, –1 и –2.
Молекула азота состоит из двух атомов.
Химическая связь в ней ковалентная
неполярная и очень прочная, так как атомы удерживаются одной σ−связью и двумя
π−связями.
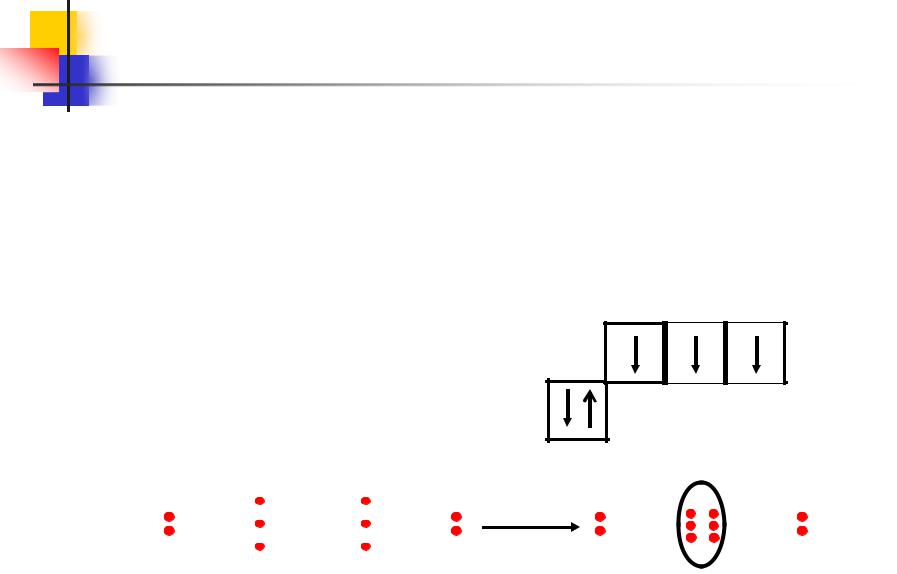
Азот. Химические свойства
В образовании молекулы азота N2 участвуют три общие пары электронов
– связь кратная (тройная).
7 N 1s |
2 |
2s |
2 |
2p |
3 |
|
B’=3 |
|
2p |
||||||
|
|
|
|
||||
|
|
|
2s |
|
|||
|
|
|
|
|
|
|
|
N |
|
+ |
|
N |
N |
N |
|
|
|
|
|||||

Азот. Химические свойства
Длина связи в молекуле N2 – 0,109 нм, энергия связи большая: – 946 кДж/моль.
Этим объясняется малая реакционная способность азота при обычной температуре.
Для химического взаимодействия азота с другими элементами надо разрушить молекулу N2 на атомы, на
что затрачивается довольно большое количество энергии: N2=2N, ∆H = 946 кДж/моль.
Поэтому азот становится реакционноспособным лишь при повышенных температурах.
При высокой температуре азот соединяется с
металлами, образуя нитриды:
3Ca + N2 = Ca3N2 −нитридкальция,
2Al + N2 = 2AlN −нитридалюминия.

Азот. Химические свойства
При комнатной температуре азот непосредственно соединяется с литием:
6Li + N2 = 2Li3N.
С водородом азот соединяется в присутствии
катализатора при высоких давлении и температуре:
N2 +3Н2 2NН3.
При температуре электрической дуги он соединяется с кислородом:
N2 +О2 2NО.

Аммиак. Получение
Азот образует с водородом несколько соединений, из которых важнейшим является аммиак.
Схема молекулы:
3 |
Н |
+ |
N |
+ |
-3 |
+ |
|
Н |
N |
Н |
Н+
В лабораторных условиях аммиак получают слабым нагреванием смеси хлорида аммония с гидроксидом кальция:
2NH4Cl +Ca(OH)2 = CaCl2 +2NH3 ↑ +2H2O.
Образующийся аммиак высушивают негашеной известью СаО.