Материал: Неорганическая химия - курс лекций-презентаций

Жесткость воды
Таким образом, ионы кальция и магния переходят из раствора в катионит, а ионы натрия – из катионита в раствор, жесткость воды при этом устраняется.
После использования бо׳льшей части ионов натрия катиониты обычно регенерируют.
Для этого их выдерживают в растворе хлорида натрия, при участии которого происходит обратный процесс: ионы натрия замещают в катионите ионы кальция и магния, которые переходят в раствор:
СаR +2Na+ = Na2R +Ca2+,
MgR +2Na+ = Na2R +Mg2+.
Регенерированный катионит снова может быть использован для
умягчения новых порций жесткой воды.

Общая характеристика подгруппы кислорода
Кислород и сера – это элементы главной подгруппы VI группы, называемой подгруппой кислорода.
К ней также относятся селен, теллур и полоний (полоний — радиоактивный элемент).
Элементы О, S, Sе, Те имеют общее название – халькогены.
У атомов халькогенов на внешнем энергетическом уровне по 6 электронов в состоянии …s2р4.
Этим объясняется сходство их химических свойств.
Присоединяя по два электрона, они превращаются в двухзарядные ионы.
Все халькогены в соединениях с водородом и металлами проявляют степень окисления –2, а в соединениях с кислородом и другими активными неметаллами – обычно +4 и +6.
Общая характеристика подгруппы кислорода
 Для кислорода не типична степень окисления,
Для кислорода не типична степень окисления,
равная номеру группы.
Он проявляет степень окисления обычно –2 и в
соединении с фтором +2.
Такие значения степеней окисления вытекают из
электронного строения внешних энергетических
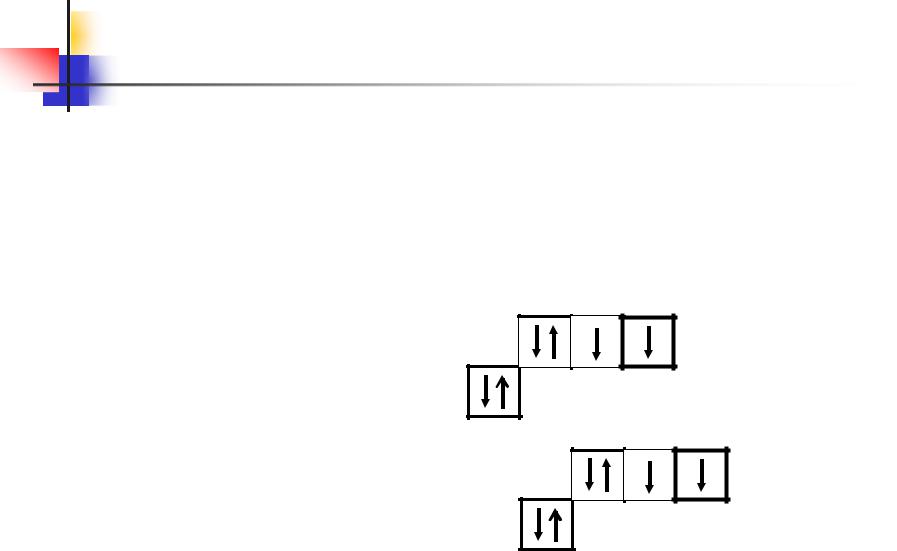
уровней атомов кислорода и серы:
8 О1s |
2 |
2s |
2 |
2p |
4 |
|
|
|
В'=2 |
|
|
|
2p |
||||||
|
|
|
|
2s |
В'=2 |
||||
|
|
|
|
|
|
|
|||
2 |
2 |
|
6 |
|
2 |
|
4 |
||
|
|
|
3p |
||||||
16 S 1s 2s 2р 3s 3p |
|
||||||||
|
3s |
||||||||
|
|
|
|
|
|
|
|
|
|

Общая характеристика подгруппы кислорода
У атома кислорода на 2р-подуровне два неспаренных электрона.
Его электроны не могут разъединяться при
отсутствии d-подуровня на внешнем (втором)
уровне, при отсутствии свободных квантовых ячеек.
Поэтому валентность кислорода всегда равна двум, а наиболее характерные степени
окисления – 2 и +2 (например, в Н2О и ОF2). Такая же валентность и степени окисления у атома серы в невозбужденном состоянии.
Общая характеристика подгруппы кислорода
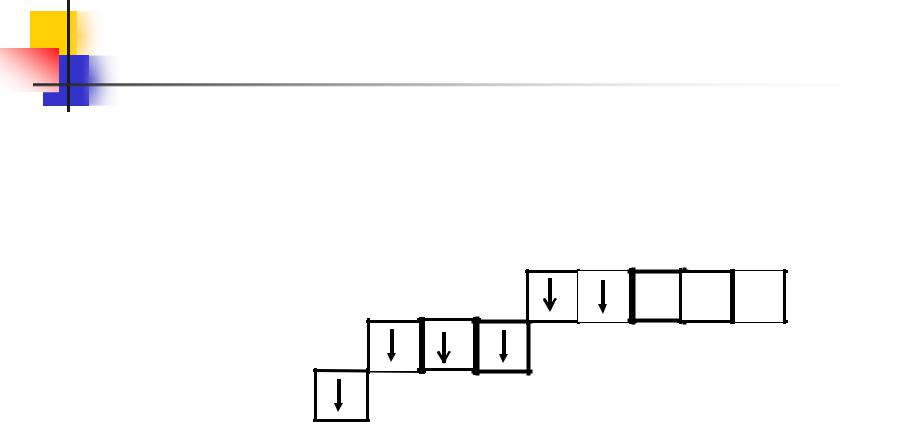
При переходе в возбужденное состояние, например при нагревании, у атома серы сначала разъединяются 3р-, а затем 3s -электроны.
**S 1s2 2s2 2p6 3s13p3 3d2
17
3p |
3s |
В’=6
3d
Число неспаренных электронов, а следовательно, и валентность в первом случае будут равны четырем (SO2), а во втором – шести (SO3).