Материал: Неорганическая химия - курс лекций-презентаций

Фосфор. Физические свойства
Известно несколько аллотропических модификаций фосфора:
белый,
красный,
черный и др.
Образование их объясняется различным
расположением атомов относительно друг друга в кристаллических решетках.
Белый фосфор — бесцветное и очень ядовитое
вещество.
Получается конденсацией паров фосфора.
Не растворятся в воде, но хорошо растворяется в сероуглероде.
При длительном слабом нагревании белый фосфор
переходит в красный.

 Фосфор. Физические свойства
Фосфор. Физические свойства
Красный фосфор – порошок красно-бурого цвета, не ядовит.
Нерастворим в воде и сероуглероде.
Установлено, что красный фосфор представляет собой смесь нескольких аллотропических модификаций, которые отличаются друг от друга цветом (от алого до фиолетового) и некоторыми другими свойствами.
Свойства красного фосфора во многом зависят от условий его получения.

Фосфор. Физические свойства
Черный фосфор по, внешнему виду похож на
графит, жирен на ощупь, обладает
полупроводниковыми свойствами.
Получается длительным нагреванием белого
фосфора при очень большом давлении (200° С
и 1200 МПа).
Природный фосфор состоит из одного стабильного изотопа 1531 Р.
Широкое применение нашел искусственный радиоактивный изотоп 3215 Р (период полураспада
14,3 суток).
Фосфор. Химические свойства
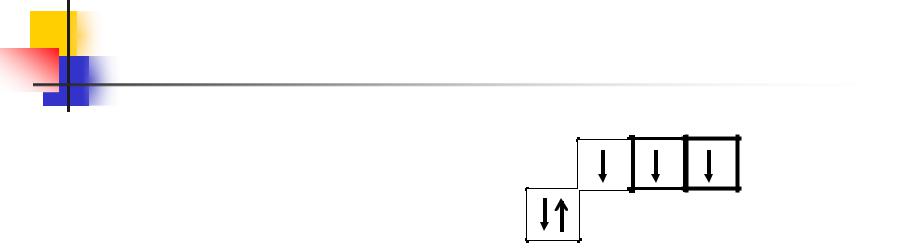
Атом фосфора на внешнем энергетическом уровне содержит 5 электронов:
15 Р1s2 2s2 2p6 3s2 3p3 |
В’=2’=3 |
|
3p |
|
2p |
|
3s |
Поэтому для фосфора характерны степени окисления – 3 и +5.
Он проявляет также степень окисления +3.
В жидком состоянии и в парах при температуре ниже 800°С молекула фосфора состоит из четырех
атомов.
При нагревании выше 800° С она распадается:
Р4 2Р2 .

 В химическом отношении белый фосфор сильно отличается от красного.
В химическом отношении белый фосфор сильно отличается от красного.