Материал: Национальная+программа+Недостаточность+витамина+Д+2018
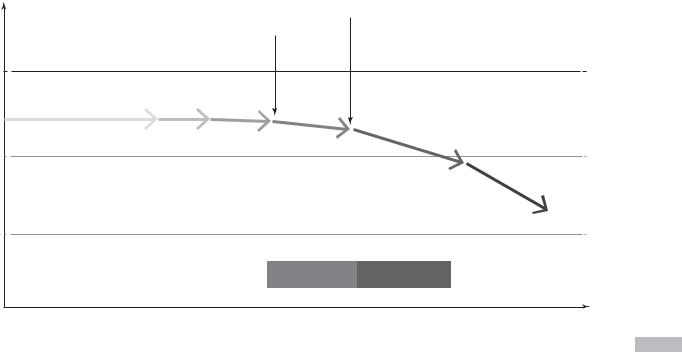
Рис. 4.11. «Эволюция» уровня кальцидиола сыворотки на разных стадиях рассеянного склероза [93]
25(ОН)D, нмоль/л
1) феномен 2) инвалидность Утхоффа
75
? ?
50
25
Первая линия родства |
РИС |
КИС |
РС (начало) |
РС (промежуточная |
|
РС (поздняя |
|
|
пациентов с РС |
|
стадия) |
|
стадия) |
|
|||
|
|
|
|
|
t |
|||
|
|
|
|
|
|
|
|
|
Примечание. РС — рассеянный склероз, РИС — радиологически изолированный синдром, КИС — клинически изолированный
синдром.
35
В аналогичном исследовании с числом участников с рассеянным склерозом 53 181 проводилась оценка неврологического статуса по расширенной шкале оценки степени инвалидизации (Expanded disability status scale, EDSS; J. F. Kurtzke, 1983) в зависимости от обеспеченности витамином D. Авторами установлено, что среди пациентов с уровнем витамина D > 50 нмоль/л оценку по шкале EDSS < 4 баллов имело в 2,78 раз большее число людей, чем в группе пациентов с уровнем кальцидиола < 50 нмоль/л (р = 0,0011). В целом наблюдалась отрицательная корреляция между уровнем витамина D и показателем EDSS (r = -0,33; р = 0,0001) [114].
В ряде работ продемонстрированы положительные эффекты приема холекальциферола, которые включают уменьшение числа и размеров очагов, установленных с помощью магнитно-резонансного исследования (р = 0,004), увеличение функциональной активности (р = 0,076), снижение числа рецидивов заболевания и риска инвалидности (р = 0,0071) [115, 116]. Отмечено, что холекальциферол имеет дополнительный эффект, когда используется в комбинации с IFN [116]. Показано, что добавки витамина D могут быть важными в период начальных проявлений рассеянного склероза, поскольку при этом снижается частота развития неврита зрительного нерва [117].
Роль дефицита витамина D в патогенезе аутоиммунных эндокринопатий (аутоиммунный тиреоидит, сахарный диабет 1-го типа)
Впоследнее время появляется все больше исследований
овзаимосвязи низкой обеспеченности витамином D и аутоиммунными эндокринопатиями, в частности аутоиммунным тиреоидитом, включая болезнь Грейвса (диффузный токсический зоб) и болезнь Хашимото; сахарным диабетом 1-го типа (СД1) [48, 118, 119].
Традиционно считается, что развитие аутоиммунных заболеваний щитовидной железы связано с несбалансированным соотношением Th1- и Th2-клеток. Наличие высокой доли Th2-клеток с повышенной секрецией IL4 провоцирует развитие болезни Грейвса. Напротив, пациенты с тиреоидитом Хашимото имеют высокую долю Th1-клеток, которые выделяют цитокин IFN . Поскольку витамин D играет
важную роль в регуляции клеток Th1, Th2 и Th17, а также регулирует секрецию IFN , IL4 и IL17, можно объяснить, почему более низкие уровни витамина D ассоциированы с аутоиммунным поражением щитовидной железы [118].
В исследовании J. Ma и соавт. было установлено, что недостаточная обеспеченность витамином D выявлена у 92,9% пациентов с болезнью Грейвса, в 94,3% случаев болезни Хашимото и в 77,1% в контрольной группе (р = 0,002) (рис. 4.12) [118].
Метаанализ 2015 года продемонстрировал, что показатель дефицита витамина D был также значительно выше
вгруппе с аутоиммунным тиреоидитом по сравнению с контрольной группой — 71,4 против 21,4% (p < 0,001). Среди пациентов с аутоиммунным тиреоидитом средний уровень 25(OH)D был значительно ниже по сравнению с контрольной группой — 16,2 ± 8,2 и 33,9 ± 12,7 нг/мл соответственно (p < 0,001). Наблюдались значительные отрицательные корреляции между концентрацией 25(OH)D и антителами против пероксидазы щитовидной железы и антителами к тиреоглобулину (антиТГ) (p < 0,001) [119].
Также доказана ассоциация низкого статуса витамина D с повышенной продукцией антител к тиреотрофиновому рецептору (анти-рТТГ) при болезни Грейвса. Таким образом, возможно, что усиленная продукция аутоантител щитовидной железы может быть следствием более низких уровней витамина D [119].
Кальцитриол играет роль в профилактике СД1 через рецептор витамина D, экспрессируемый в антигенпрезентирующих клетках, активированных Т-клетках и -клетках поджелудочной железы. На уровне островков поджелудоч-
ной железы под действием 1,25(OH)2D in vivo и in vitro снижается продукция провоспалительных хемокинов и цитокинов (например, IL6), которые участвуют в патогенезе СД1, что делает -клетки менее подверженными воспалению. Это приводит к уменьшению рекрутирования Т-клеток и инфильтрации ими, увеличению регуляторных клеток и остановке аутоиммунного процесса [48].
На уровне иммунной системы 1,25(OH)2D ингибирует дифференцировку и созревание дендритных клеток и способствует их апоптозу, предотвращая их превращение
вклетки, презентирующие антиген, что является первым
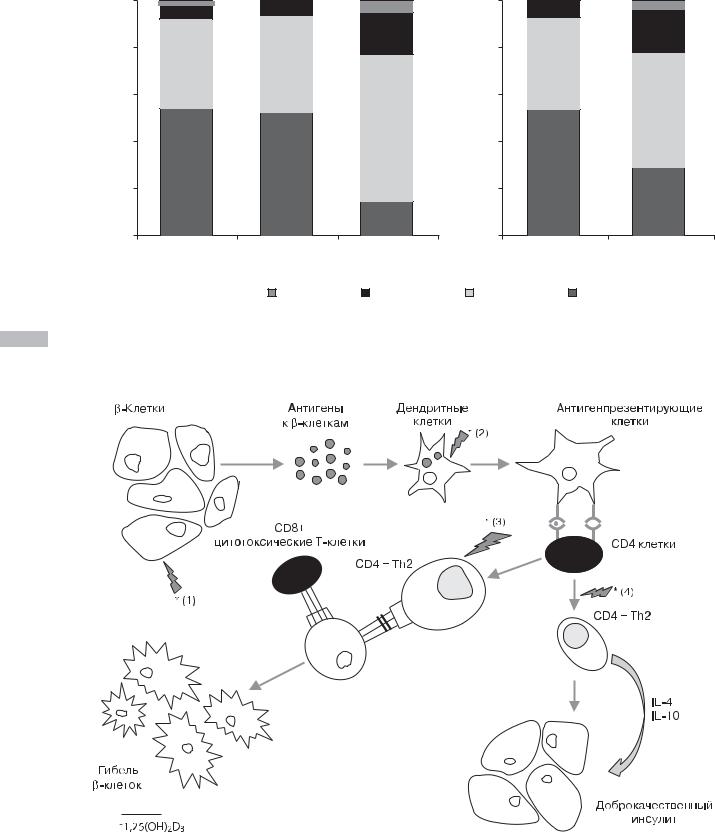
Рис. 4.12. Распространенность дефицита витамина D у пациентов с аутоиммунным тиреоидитом [118] |
|
||||||
|
* |
# |
|
|
$ |
|
|
|
100 |
|
|
100 |
|
|
|
|
80 |
|
|
|
80 |
|
|
% |
60 |
|
|
|
60 |
|
|
Частота, |
|
|
|
|
|
||
40 |
|
|
|
40 |
|
|
|
|
|
|
|
|
|
|
|
|
20 |
|
|
|
20 |
|
|
|
0 |
|
|
|
0 |
|
|
|
ДТЗ |
Тиреоидит |
Группа |
|
Послеродовый |
Группа |
|
А |
|
Хашимото |
контроля |
Б |
тиреоидит |
контроля |
|
|
|
> 75 нг/мл |
50–75 нг/мл |
|
30–50 нг/мл |
30 нг/мл |
|
Примечание. * — р = 0,009; # — р = 0,004; $ — р < 0,05 при сравнении с контрольной группой. |
|
|
|||||
36
Рис. 4.13. Роль кальцитриола в патогенезе сахарного диабета 1-го типа [48]
шагом в инициировании иммунного ответа [120]. Было также продемонстрировано, что 1,25(OH)2D восстанавливает супрессорные клетки, уменьшает продукцию цитокинов Th1, ответственных за гибель -клеток, и сдвигает иммунный ответ на путь Th2, что приводит к доброкачественному инсулиту [48, 121]. Добавление кальцитриола ингибиру-
ет продукцию IL6 — прямого стимулятора клеток Th17 [15], участвующего во многих аутоиммунных заболеваниях, включая СД1 (рис. 4.13) [48].
С другой стороны, 1,25(OH)2D оказывает антиапоптотическое действие на индуцированный цитокинами апоптоз клеток поджелудочной железы. Он индуцирует и поддерживает
высокий уровень белка гена A20, что приводит к снижению уровней оксида азота (NO), который индуцирует непосредственно -клеточную дисфункцию и их гибель — косвенно, через экспрессию Fas [122]. Fas представляет собой трансмембранный клеточный поверхностный рецептор из семейства рецепторов некроза опухолей. Он стимулируется воспалительными цитокинами, секретируемыми островковыми инфильтрационными мононуклеарными клетками. Это делает-клетки при СД1 восприимчивыми к индуцированному Fasлигандом апоптозу, опосредуемому тканепроникающими Fasлигандположительными Т-лимфоцитами. Снижение уровней NO приводит к снижению регуляции всех вышеперечисленных механизмов и позволяет усилить цитопротекторные эффекты островковых клеток. Было обнаружено, что 1,25(OH)2D способен противодействовать индуцированной цитокинами экспрессии Fas в островках поджелудочной железы человека на уровне мРНК, предотвращая апоптоз клеток [122].
Метаанализ 5 исследований показал, что риск СД1 значительно сокращался у детей, получавших добавки витамина D, по сравнению с детьми, которые не принимали витамин D (ОР 0,71; 95% ДИ 0,60–0,84) [123].
Путем обследования 128 детей с СД1 установлено, что 19 (14,8%) пациентов имели дефицит витамина D, 78 (60,9%) — недостаточность и лишь 31 (24,3%) — достаточные уровни кальцидиола сыворотки. При этом среди групп детей в воз-
расте 0–5, 6–11 и 12–18 лет доля участников с недостатком или дефицитом витамина D составляла 56; 69 и 85% соответственно (рис. 4.14). При этом во всех возрастных группах отмечалась низкая обеспеченность витамином D, дети в возрасте 12–18 лет имели достоверно более низкие показатели 25(OH)D по сравнению с группой 0–5 лет (p < 0,01) [124].
Роль дефицита витамина D в патогенезе аутоиммунных заболеваний желудочно-кишечного тракта (язвенный колит, болезнь Крона, целиакия)
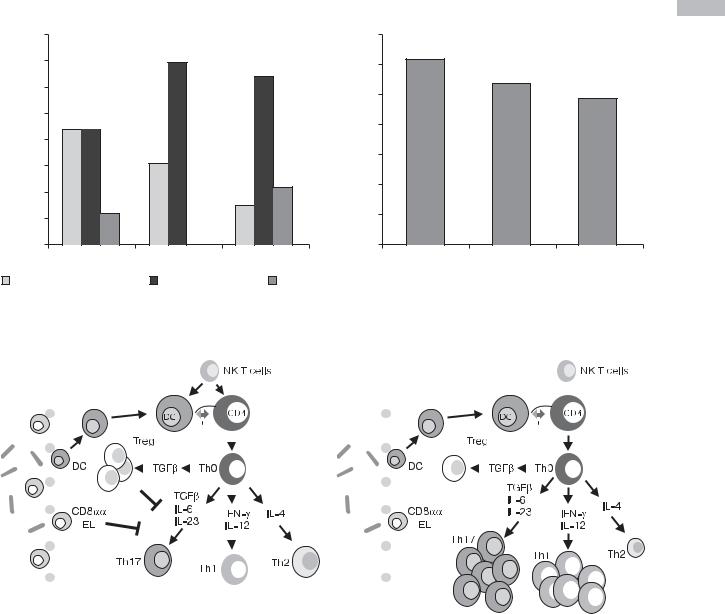
Поскольку витамин D3 влияет на баланс Th1/Th2 в пользу развития Th2-клеток путем ингибирования продукции IL12, он способен снижать активность процесса воспаления при аутоиммунных заболеваниях, в том числе и ВЗК.
Витамин D влияет также и на другой патогенетический фактор развития ВЗК — гомеостаз слизистой оболочки толстой кишки, сохраняя целостность эпителиального барьера и заживляющую способность эпителия (рис. 4.15) [125–127]. Витамин D поддерживает целостность эпителиального барьера путем увеличения экспрессии белков, отвечающих за плотное соединение эпителиальных клеток, включая окклюдин, клаудин, винкулин, зонулин (ZO-1 и ZO-2) [11], поэтому дефицит витамина D приводит к повышенной восприимчивости слизистой оболочки к повреждению и значительно увеличивает риск развития ВЗК [126].
Рис. 4.14. Статус витамина D у детей с сахарным диабетом 1-го типа [124] |
||||||||
|
80 |
|
|
|
|
|
нг/мл |
35 |
|
70 |
|
|
69 |
|
|
30 |
|
|
|
|
|
63 |
|
|||
|
|
|
|
|
|
|||
|
60 |
|
|
|
|
|
уровень 25(ОН)D, |
25 |
|
|
|
|
|
|
|
||
Частота, % |
50 |
44 |
44 |
|
|
|
20 |
|
|
|
|
|
|||||
|
|
|
|
|
|
|||
40 |
|
|
|
|
|
|
||
30 |
|
|
31 |
|
|
15 |
||
|
|
|
22 |
|
||||
|
|
|
|
10 |
||||
20 |
|
|
|
|
|
|||
|
|
|
|
15 |
|
Средний |
||
|
|
12 |
|
|
|
|||
|
|
|
|
|
|
|||
|
10 |
|
|
|
|
5 |
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
||
|
0 |
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
||
А |
|
|
0–5 |
6–11 |
12–18 |
|
Б |
|
|
Оптимальный уровень |
Недостаточность |
Дефицит |
|
|
|||
Примечание. * — р < 0,01. |
|
|
|
|
|
|||
37
30,8* |
|
|
|
26,8 |
|
|
|
24,2 |
0–5 |
6–11 |
12–18 |
|
Возраст в годах |
|
Рис. 4.15. Участие витамина D в клеточной дифференцировке при достаточной обеспеченности (А) и недостатке (Б) витамина D [127]
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
А |
|
|
|
|
|
Б |
|
|
|
||||||||||||

Исследования свидетельствуют о том, что дефицит витамина D может нарушать микробный гомеостаз толстой кишки: мыши, не имеющие рецепторов VDR в эпителиальных клетках толстой кишки, имеют повышенную восприимчивость к колиту и отчетливые различия в микробиоме кишечника по сравнению с однопометниками дикого типа с интактными VDR [11].
Многочисленными исследованиями показано, что у пациентов с ВЗК обычно диагностируется дефицит витамина D, даже в период ремиссии [11, 12, 128, 129]; более того, сниженный уровень витамина D является одним из внешних факторов, влияющих на риск обострения и прогредиентный характер течения ВЗК [11, 12]. Исследование A. N. Ananthakrishnan и соавт., включившее 3217 пациентов с язвенным колитом и болезнью Крона, показало, что дефицит витамина D связан с увеличением активности клинических проявлений, более высокими показателями госпитализации, длительной госпитализацией и увеличением потребности в хирургическом лечении кишечника у пациентов с ВЗК, а также с риском злокачественной трансформации, тогда как нормальная концентрация кальцидиола в сыворотке крови значительно уменьшает все эти показатели [129]. Интересен и такой факт: в то время как диета, богатая витамином D, подавляла воспаление на раннем этапе, дефицит витамина D в питании не вызывал более сильного воспаления по сравнению с контролем, подтверж-
38дая, что высокий уровень витамина D может препятствовать воспалению, но недостаток витамина D не ускоряет/не усу-
губляет этого процесса [11].
Витамин D может поступать в организм человека
спищей или образовываться в коже под действием солнечного излучения. Молекулы витамина D, поступающие
спищей, всасываются в тонком кишечнике, используя те же абсорбционные механизмы, что и другие жирорастворимые вещества (желчь, панкреатическую липазу и мицеллообразование) [130]. Причинами дефицита витамина D являются снижение воздействия солнечного света, неадекватная диета, заболевания желудочно-кишечного тракта, сопровождающиеся синдромом мальабсорбции [131]. Синдром нару-
шенного кишечного всасывания у пациентов с болезнью Крона связан с хроническим воспалением, особенно после резекции тонкой кишки [12], а при целиакии — с атрофией ворсинок.
Впатогенезе синдрома мальабсорбции неизбежно присутствуют нарушения кальциевого гомеостаза и метаболизма костной ткани. В результате обширного поражения тонкого кишечника — атрофического при целиакии и воспалительного при болезни Крона — нарушается всасывание витамина D. В клетках слизистой оболочки кишечника витамин D стимулирует синтез кальцийсвязывающего белка кальбиндина, необходимого для активного транспорта кальция. Действие ПТГ, проявляющееся усилением абсорбции кальция, полностью осуществляется через его стимулирующий эффект на продукцию кальцитриола почками [132]. В отсутствии витамина D способно абсорбироваться лишь 10–15% кальция, поступающего с пищей, в то время как достаточное потребление этого вещества усиливает всасывание кальция до 30–40% [130, 133]. Повышенная потеря кальция различной степени выраженности при диарее и мальабсорбция этого макроэлемента в кишечнике, возникающая у больных, приводит к гипокальциемии и, следовательно, развитию вторичного гиперпаратиреоза. ПТГ стимулирует образование кальцитриола в почках, при этом уровень кальцидиола в сыворотке может снижаться,
врезультате чего у больных целиакией развивается повышенная потребность в витамине D, что, наряду с мальабсорбцией, приводит к его недостаточности и дефициту [133].
Многочисленными исследованиями показан достоверно более низкий уровень кальцидиола сыворотки крови при сравнении со здоровыми пациентами. В метаанализе и систематическом обзоре R. Del Pinto и соавт. с участием 1891 пациента с ВЗК продемонстрирована недостаточность витамина D у 64% пациентов с ВЗК в сравнении с контрольной группой [134].
Висследовании J. Gubatan и соавт. продемонстрировано, что пациенты с рецидивом ВЗК имеют более низкую обеспеченность витамином D (медиана 29,5 нг/мл) по сравнению с пациентами, находящимися в ремиссии (медиана
Таблица 4.9. Распространенность гиповитаминоза D у пациентов с воспалительными заболеваниями кишечника
|
|
Число больных, |
Уровень 25(OH)D, |
Пациенты с низким |
|||
|
|
ниже которого |
|||||
|
|
уровнем 25(OH)D, % |
|||||
Исследование |
Страна |
вошедших |
|||||
пациент включался |
|||||||
|
|
|
|||||
|
|
в исследование |
|
|
|
||
|
|
в исследование |
Общий |
Зимой |
Летом |
||
|
|
|
|||||
|
|
|
|
|
|
|
|
Torki M. и соавт., |
|
БК — 48 |
|
|
|
|
|
Иран |
ЯК — 85 |
20 нг/мл |
39 |
- |
- |
||
2015 [136] |
|||||||
|
Всего — 133 |
|
|
|
|
||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
Suibhne T. N. и соавт., |
Ирландия |
БК — 81 |
20 нг/мл |
|
|
|
|
2012 [137] |
63 |
68 |
50 |
||||
|
|
|
|||||
|
|
|
|
|
|
|
|
Ulitsky A. и соавт., |
Висконсин, |
БК — 403 |
|
|
|
|
|
ЯК — 101 |
20 нг/мл |
49,8 |
- |
- |
|||
2012 [139] |
США |
||||||
Всего — 504 |
|
|
|
|
|||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
Bours P. H. А. и соавт., |
|
БК — 130 |
|
|
|
|
|
Нидерланды |
ЯК — 186 |
20 нг/мл |
- |
57 |
39 |
||
2011 [140] |
|||||||
|
Всего — 316 |
|
|
|
|
||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
McCarthy D. и соавт., |
Ирландия |
БК — 44 |
20 нг/мл |
35 |
50 |
18 |
|
2005 [141] |
|||||||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
Tajika M. и соавт., |
Япония |
БК — 44 |
< 10 нг/мл |
27,3 |
- |
- |
|
2004 [142] |
|||||||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
Siffledeen J. S. и соавт., |
Канада |
БК — 242 |
< 40 нмоль/мл |
22% |
- |
- |
|
2003 [143] |
|||||||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
Jahnsen J. и соавт., |
|
БК — 60 |
|
БК — 27% |
|
|
|
Норвегия |
ЯК — 60 |
12,5 нг/мл |
- |
- |
|||
2002 [144] |
ЯК — 15% |
||||||
|
Всего — 120 |
|
|
|
|||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
Примечание. БК — болезнь Крона, ЯК — язвенный колит.

Таблица 4.10. Схема и эффективность использования витамина D у пациентов с воспалительными заболеваниями кишечника
Исследование |
Страна |
Доза витамина D3 |
Поддержи- |
Результат |
|
вающая доза |
|||||
|
|
|
|
||
|
|
|
|
|
|
Holick M. F. |
|
6000–10 000 МЕ в день |
3000– |
Риск рака толстой кишки стал прогрессивно |
|
и соавт., |
США |
до достижения концентрации |
ниже после того, как 25(ОН)D увеличили |
||
6000 МЕ/сут |
|||||
2011 [148] |
|
кальцидиола более 30 нг/мл |
до 30–32 нг/мл |
||
|
|
||||
|
|
|
|
|
|
Jorgensen S. P. |
|
1200 МЕ в день у пациентов |
|
Частота рецидивов была ниже среди |
|
|
с БК (n = 46) по сравнению |
|
пациентов, получавших витамин D3 (6/46, |
||
и соавт., |
Дания |
- |
|||
с плацебо (n = 48) в течение |
или 13%), чем среди пациентов, получавших |
||||
2010 [149] |
|
|
|||
|
12 месяцев |
|
плацебо (14/48, или 29%) (p = 0,06) |
||
|
|
|
|||
|
|
|
|
|
|
|
|
10 000 МЕ в день (n = 18) |
|
Клинический рецидив БК не наблюдался |
|
Narula N. |
|
по сравнению с 1000 МЕ |
|
у пациентов, получавших 10 000 МЕ (0%), |
|
и соавт., |
Канада |
в день (n = 16) в течение |
- |
по сравнению с пациентами, получавшими |
|
2017 [150] |
|
12 месяцев у пациентов с БК |
|
ежедневно низкую дозу — 1000 МЕ (37,5%) |
|
|
|
в ремиссии |
|
(p = 0,049) |
|
|
|
|
|
|
|
Scott E.M. |
|
800 МЕ/сут витамина D + |
|
Дозы, безопасные без мониторинга. |
|
Велико- |
|
Должно быть обеспечено общее |
|||
и соавт., |
200–1000 мг в день кальция |
- |
|||
британия |
потребление кальция (включая |
||||
2000 [151] |
ежедневно постоянно |
|
|||
|
|
диетический) 1500 мг/сут |
|||
|
|
|
|
||
|
|
|
|
|
Примечание. БК — болезнь Крона.
50,3 нг/мл). Достаточный уровень обеспеченности витамином D (уровень кальцидиола < 35,0 нг/мл) ассоциировался
сэндоскопической и гистологической ремиссией в течение 12 месяцев. Таким образом, авторы данного исследования констатируют не только факт достаточной обеспеченности витамином D пациентов с ВЗК, но и уровень выше 35 нг/мл [135]. Пациенты с ВЗК в активной стадии заболевания по сравнению с группой ремиссии имели более низкие уровни 25(ОН)D (80 против 50,4%; р = 0,005) [136]. Пациенты с болезнью Крона имели значительно более низкую среднюю концентрацию 25(ОН)D по сравнению
спациентами с язвенным колитом [137].
Врандомизированном клиническом исследовании изучалась эффективность дотации витамина D больным ВЗК в дозировке 400 МЕ/сут и 2000/1000 МЕ/сут (осень- зима/весна-лето). По результатам исследования показано, что доза 2000/1000 МЕ/сут достоверно лучше подавляет активность воспаления, снижает уровень IL6, С-реактивного протеина, СОЭ, чем доза 400 МЕ/сут [138]. В табл. 4.9 приведены сводные данные по частоте выявляемости недостаточности витамина D в зависимости от страны проживания
инозологической формы ВЗК.
Исследования, посвященные изучению уровня витамина D при целиакии, анализируют данные в зависимости от периода заболевания, приверженности безглютеновой диете и сезона, в который проводился забор крови. В частности, в работе A. De Rosа не получено достоверной разницы в уровне кальцидиола сыворотки крови в различные периоды заболевания, не обнаружено влияния на него индекса массы тела пациентов, комплаенса безглютеновой диете, но выявлены различия в зависимости от сезона,
вкотором проводилось исследование [145]. Очевидно, что
влетние месяцы уровень кальцидиола выше по сравнению с зимним сезоном. Данная закономерность характерна не только для пациентов с целиакией, ВЗК, но и для здоровых детей. Закономерным итогом развивающихся при целиакии и ВЗК нутритивных нарушений и гормональных дисбалансов является снижение минерализации и прочности костной ткани, что может привести к спонтанным переломам [146].
Дозировки витамина D, рекомендуемые при целиакии, направлены на профилактику развития остеопороза и связанных с ним переломов. Риск поражения костей при ВЗК возрастает при увеличении длительности анамнеза и коррелирует с активностью воспалительного процесса, а также
сприменением глюкокортикостероидов.
Современная базисная терапия ВЗК включает препараты глюкокортикостероидов, частота применения которых, особенно при болезни Крона, составляет более 50%, а длитель-
ность приема колеблется от 3 недель до нескольких лет 39 (будесонид). Глюкокортикостероиды считаются классическим фактором риска потери костной массы и остеопоретических переломов, т.к. являются одними из основных ингибиторов
синтеза 1,25(ОН)2D [147]. Глюкокортикостероиды подавляют циркулирующий эстроген и снижают концентрацию тестостерона в крови, тем самым уменьшая их роль в ингибировании цитокина IL6, который является стимулятором остеокластической активности, а также ингибируют созревание остеобластов. В отличие от болезни Крона, остеопороз при язвенном колите обычно диагностируется не в момент манифестации заболевания, а на фоне лечения глюкокортикостероидами. Ежегодная потеря костной массы больными ВЗК в целом составляет 3%, а принимающими глюкокортикостероиды — 6% [130].
Уровень низкой минеральной плотности костной ткани у пациентов с ВЗК в настоящее время оценивается в 31–59% [131]. В исследовании, проведенном в МОНИКИ им. М. Ф. Владимирского (Москва), показано, что частота снижения минеральной плотности костной ткани у больных ВЗК достоверно увеличивается при нарастании тяжести болезни; достоверно чаще снижение минеральной плотности кости встречается у больных ВЗК с впервые установленным диагнозом, уменьшаясь по мере увеличения длительности заболевания (р = 0,01) [132]. В табл. 4.10 представлены результаты исследований, отражающих эффективность использования витамина D в комплексном лечении ВЗК.
ЛИТЕРАТУРА
1.Baeke F., Korf H., Overbergh L., van Etten E., Verstuyf A., Gysemans C., Mathieu C. Human T lymphocytes are direct targets of 1,25-dihydroxyvitamin D3 in the immune system.
J Steroid Biochem Mol Biol. 2010;121:221–227.
2.Kongsbak M., von Essen M.R., Levring T.B., Schjerling P., Woetmann A., Odum N. Vitamin D-binding protein controls T cell responses to vitamin D. BMC Immunol. 2014;15(1):35.
3.Национальная программа по оптимизации обеспеченности витаминами и минеральными веществами детей России (и использованию витаминных и витаминноминеральных комплексов и обогащенных продуктов в педиатрической практике). Союз педиатров России [и др.]. М.: ПедиатрЪ, 2017. 152 с.