Материал: Национальная+программа+Недостаточность+витамина+Д+2018
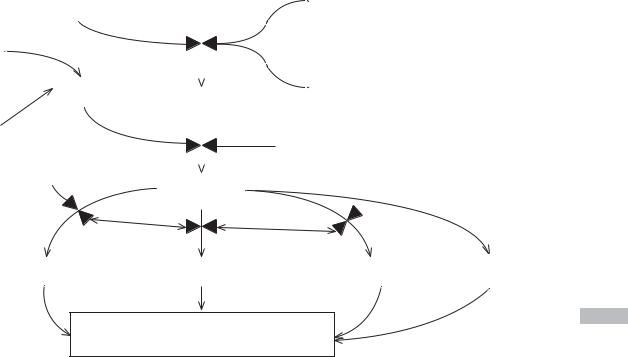
Рис. 4.16. Противоопухолевый эффект витамина D [1] |
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Препараты витамина D3 (800...3000 МЕ/сут) |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
Биосинтез витамина |
|
|
|
|
Полиморфизмы генов |
|||||
|
|
|
|
|
|
|
|
биосинтеза витамина D3 |
||||||
|
|
|
под воздействием УФО-В |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
Состояние печени |
||
|
|
Эстрогеновые |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
и почек |
|||
|
|
препараты |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Уровни |
|
|
|
|
Полиморфизмы |
|
||||
|
|
|
|
|
|
|
|
VDBP (gc1s, gc1f) |
|
|||||
|
|
|
|
эстрогенов |
Повышение уровня |
|
|
|||||||
|
Полиморфизмы |
|
|
|
||||||||||
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
1,25(ОН)2D3 в плазме |
|
|
|
|
|
||||
|
(ТА, СА, К303R) |
|
|
|
|
|
|
|
|
|
||||
|
гена рецептора |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
Полиморфизмы VDR |
|
|
|||||
|
эстрогенов ESR1 |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
(Bsml, Fokl, Taql, Apal) |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
Уровни Zn, |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
Ca, Mg |
|
|
Активация VDR |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
рецептора |
|
|
|
|
|
|
Уменьшение |
Регулирование |
Активация |
Поддержание |
пролиферации клеток |
апоптоза |
лимфоцитов |
нормальной массы тела |
45
Снижение смертности от всех онкологических заболеваний, снижение риска рака молочной
железы и толстого кишчника
Примечание. ESR1 — эстрогеновый рецептор; VDBP — витамин D-связывающий транспортный белок; VDR — витамин D-рецептор. Символ « » отображает зависимость эффекта от дополнительных условий.
» отображает зависимость эффекта от дополнительных условий.
антипролиферативным действием в отношении ткани |
4. |
Wang D., Velez de la Paz O. I., Zhai J. X., Liu D. W. Serum |
||||
молочной железы, так как эпителиоциты, выстилающие |
|
25-hydroxyvitamin D and breast cancer risk: a meta-analysis |
||||
млечные протоки, имеют аналогичную почкам фермента- |
|
of prospective studies. Tumour Biol. 2013;34(6):3509–17. |
||||
тивную систему [8, 9]. |
|
|
|
5. |
Chung M., Lee J., Terasawa T., Lau J., Trikalinos T. A. Vita- |
|
Американские исследователи доказали связь между низ- |
|
min D with or without calcium supplementation for preven- |
||||
ким уровнем витамина D в сыворотке крови у девочек |
|
tion of cancer and fractures: an updated meta-analysis for |
||||
и ранним менархе. Известно, что ранний возраст начала |
|
the U. S. Preventive Services Task Force. Ann Intern Med. |
||||
менструации (до 12 лет) является одним из основных фак- |
|
2011;155(12):827–38. |
||||
торов риска развития заболеваний молочной железы (дис- |
6. |
Westerdahl J., Ingvar C., Masback A., Jonsson N., Olsson H. |
||||
плазии и рака молочной железы) [10–12]. |
|
|
|
Risk of cutaneous malignant melanoma in relation to use |
||
Таким образом, фундаментальные и клинико-эпиде- |
|
of sunbeds: further evidence for UV-A carcinogenicity. Br J |
||||
миологические данные свидетельствуют о необходимости |
|
Cancer. 2000;82(9):1593–1599. |
||||
просветительской работы среди населения о важной роли |
7. |
Zheng Y., Zhu J., Zhou M., Cui L., Yao W., Liu Y. Meta- |
||||
витамина D в профилактике и лечении онкологических |
|
analysis of long-term vitamin D supplementation on overall |
||||
заболеваний. С этой целью витамин D следует прини- |
|
mortality. PLoS One. 2013;8(12): e8210. |
||||
мать в дозах никак не менее 800 МЕ, лучше в интервале |
8. |
Kemmis C., Welsh J. E. Mammary epithelial cell transfor- |
||||
1000–2000 МЕ/сут в течение достаточно длительных пери- |
|
mation is associated with deregulation of the vitamin D |
||||
одов времени (не менее 3 лет); особенно важен регулярный |
|
pathway. J Cell Biochem. 2008;105:980–988. |
||||
ежедневный прием витамина D (2000 МЕ/сут) в период |
9. |
Shao T., Klein P., Grossbard M. L. Vitamin D and breast |
||||
с октября по май. |
|
|
|
|
cancer. Oncologist. 2012;17(1):36–45. |
|
|
|
|
|
|
10. Rogers D. A., Lobe T. E., Rao B. N., et al. Breast malignancy |
|
|
|
|
|
|
|
in children. J Pediatr Surg. 1994;29(1):48–51. |
ЛИТЕРАТУРА |
|
|
|
|
11. Neinstein L. S. Breast disease in adolescent and young |
|
1. Громова О. А., Торшин И. Ю. Витамин D — смена пара- |
|
women. Pediatr Clin North Am. 1999;46(3):607–629. |
||||
дигмы. Под ред. акад. РАН Е. И. Гусева, проф. И. Н. Заха- |
12. Харченко В. П., Рожкова Н. И. Маммология: националь- |
|||||
ровой. М.: ГЭОТАР-Мед. 2017. С. 386–389. |
|
|
|
ное руководство. М.: ГЭОТАР-Медиа, 2009. 328 с. |
||
2. Gilad L. A., |
Bresler T. Regulation |
of vitamin |
D |
receptor |
|
|
expression |
via estrogen-induced |
activation |
of |
the ERK |
|
|
1/2 signaling pathway in colon and breast cancer cells. J Endocrinol. 2005;185(3):577–592.
3. Gilad L. A., Schwartz B. Association of estrogen receptor beta with plasma-membrane caveola components: implication in control of vitamin D receptor. J Mol Endocrinol. 2007;38(6):603.
|
инсулинорезистентностью [3], неблагоприятным влиянием |
уровни которого связаны с ожирением и диабетом. Курсовой |
|
|
на секрецию инсулина [4], а также с глюкозотолерантностью |
прием витамина (3000 МЕ/сут в течение 12 месяцев) досто- |
|
|
и повышенным риском сахарного диабета 2-го типа (СД2) |
верно увеличивал уровни адипонектина (p < 0,02) [14]. |
|
|
[5]. Экспериментальные и клинические исследования под- |
Все эти эффекты витамина D осуществляются посред- |
|
|
тверждают, что адекватная обеспеченность витамином D |
ством специфичного связывания активных форм витамина |
|
|
снижает заболеваемость СД2, улучшает метаболический |
с рецептором VDR, который в свою очередь оказывает ком- |
|
|
контроль при наличии диабета (в т. ч. гестационного, стиму- |
плексное воздействие на процессы транскрипции генома. |
|
|
лирующего формирование пороков развития и макросомии |
Биоинформационный анализ [15] указал на существование |
|
|
у новорожденного) [6–9]. |
по крайней мере 100 генов, транскрипция которых может |
|
|
Ожирение является многофакторным заболеванием, |
регулироваться витамином D, а нарушения активности |
|
|
в генезе которого играют роль как наследственные, так и мно- |
соответствующих генам белков ассоциированы с факторами |
|
|
гочисленные внешнесредовые стимулы. В последние годы |
патофизиологии диабета. Некоторые из этих генов и белков, |
|
|
в литературе широко обсуждаются плейотропные эффекты |
которые участвуют в регуляции углеводного и жирово- |
|
|
витамина D, в частности его влияние на накопление и обмен |
го метаболизма, активации адренергических сигнальных |
|
|
жировой ткани. При этом причинно-следственные взаимоотно- |
путей, апоптоза/выживания клеток и в иммуномодуляции, |
|
|
шения дефицита витамина D и ожирения понятны не до конца. |
перечислены в табл. 4.11. |
|
|
С одной стороны, обсуждается негативное влияние избытка |
Одним из механизмов этиопатогенетического воздей- |
|
|
жира на повышение катаболизма и образование неактивных |
ствия витамина D на метаболический синдром и диабет |
|
|
форм витамина D, избыточное депонирование его в жировой |
является, несомненно, нормализация процессов воспаления. |
|
|
ткани, снижение активности -гидроксилаз в инфильтриро- |
В культуре клеток поджелудочной железы 1,25(ОН)2D тор- |
|
|
ванной жиром печени. С другой стороны, широкая пред- |
мозил экспрессию провоспалительных хемокинов и цито- |
|
|
ставленность и возможности экспрессии рецепторов витами- |
кинов в панкреатических островках [16]. Сравнение моно- |
|
|
на D в жировой ткани, участвующих в липогенезе, липолизе |
цитов у пациентов с СД2 с моноцитами здоровых и больных |
|
|
и адипогенезе, повышение содержания ПТГ, отмечаемое при |
СД1 показало, что моноциты пациентов с СД2 имели значи- |
|
|
дефиците витамина D и активирующее липогенез, позволяют |
тельно более высокие уровни экспрессии провоспалитель- |
|
|
рассматривать витамин D в качестве самостоятельного факто- |
ных интерлейкинов TNF , IL6, IL1, IL8, фермента цикло- |
|
|
ра риска накопления жировой ткани [10–13]. |
оксигеназа-2, белков-маркеров воспаления (ICAM-1, B7-1) |
|
46 |
|||
В настоящее время накоплено достаточно убедительных |
по сравнению с контрольной группой и группой больных |
||
|
|||
|
данных, подтверждающих роль жировой ткани как самосто- |
СД1. Снижению экспрессии вышеназванных провоспали- |
|
|
ятельного эндокринного органа, способного секретировать |
тельных интерлейкинов способствовал 1,25(ОН)2D [17]. |
|
|
и депонировать биологически активные вещества — адипо- |
Метаанализ 28 исследований (n = 99 745) показал |
|
|
цитокины, имеющие ауто-, пара- и эндокринную направлен- |
(рис. 4.17), что среди участников в квартиле с самыми |
|
|
ность действия. Так, к числу наиболее изученных можно |
высокими уровнями 25(OH)D в сыворотке крови отме- |
|
|
отнести лептин — полифункциональный адипокин, играю- |
чено снижение риска кардиометаболических расстройств |
|
|
щий ключевую роль в процессах сигналинга «периферия, |
(СД2 и метаболического синдрома) на 43% (ОР 0,57; 95% |
|
|
жировая ткань — центр, анализаторы центральной нервной |
ДИ 0,48–0,68) [18]. |
|
|
системы», посредством которого происходят регулирование |
Сравнение 170 детей (5–16 лет), больных СД1, с кон- |
|
|
количества жировой ткани, активация системы гонадо- |
трольной группой из 170 здоровых детей указало на зна- |
|
|
стата, управление пищевым поведением и т. д. Нарушение |
чительное снижение уровней витамина D в плазме крови |
|
|
лиганд-рецепторных взаимодействий в отношении лептина |
у пациентов с СД1 (р = 0,009) [19]. Метаанализ данных |
|
|
ведет к серьезным нарушениям, касающимся, в первую оче- |
5 исследований типа случай-контроль показал, что риск |
|
|
редь, жирового обмена. Роль лептина продолжает изучаться. |
СД1 был значительно ниже у грудных детей, которые полу- |
|
|
По мнению некоторых исследователей, избыточное коли- |
чали добавки с витамином D, по сравнению с теми деть- |
|
|
чество лептина вследствие ожирения способно негативно |
ми, которые не получали витамина D (ОР 0,71; 95% ДИ |
|
|
влиять на функциональные эффекты витамина D, снижая |
0,60–0,84). В исследовании наблюдался отчетливый дозоза- |
|
|
активность фермента альфа-гидроксилазы, катализирую- |
висимый эффект витамина D [20]. Полученные результаты |
|
|
щей реакции образования активного метаболита витами- |
были подтверждены в последующих 8 метаанализах [21]. |
|
|
на D кальцитриола. Другим адипоцитокином, обладающим |
Прием витамина D3 (2000 МЕ/сут в течение 12 недель) |
|
|
уникальной антидиабетической, антиатерогенной и про- |
в группе подростков с ожирением приводил к досто- |
|
|
тивовоспалительной активностью, является адипонектин. |
верному повышению 25(OH)D в сыворотке на 6 нг/мл |
|
|
Снижение уровня адипонектина сыворотки крови выяв- |
(p < 0,001 по сравнению с плацебо) [22]. Курсовой прием |
|
|
ляется у людей, страдающих ожирением, СД2, артериаль- |
(3000 МЕ/сут, 12 месяцев) в группе детей с ожирением |
|
|
ной гипертонией, дислипидемией и ишемической болезнью |
и дефицитом витамина D (< 15 нг/мл) достоверно увеличи- |
|
|
сердца. Более того, во взрослой популяции низкий уровень |
вал уровни адипонектина (p < 0,02) [23]. Назначение добавок |
|
|
адипонектина (менее 4,0 мкг/мл) является независимым |
витамина D3 (25 000 МЕ/нед, 9 недель, т. е. ~4000 МЕ/сут) |
|
|
фактором риска развития СД2 и дислипидемий. В некото- |
в группе детей 8–18 лет, страдающих ожирением (n = 109) |
|
|
рых исследованиях показано снижение уровня адипонек- |
и имеющих дефицит витамина D (< 50 нмоль/л), приводило |
|
|
тина при прогрессировании пубертата, нарастании уровня |
к тому, что после 9 недель дефицит витамина был установ- |
|
|
тестостерона. Взаимоотношения как лептина, так и адипо- |
лен только у 25% пациентов, при этом терапия не имела |
|
|
нектина с уровнем 25(ОН)D при разной степени накопле- |
никаких побочных эффектов [24]. |
|
|
ния жировой ткани являются недостаточно изученными. |
В пилотном исследовании [25, 26], выполненном |
|
|
Протеомный подход к анализу биомаркеров крови уста- |
в Северо-Западном регионе России (Санкт-Петербург и |
|
|
новил, что у детей с ожирением и дефицитом витамина D |
Ленинградская область), изучены обеспеченность вита- |
|
|
снижены уровни адипонектина. Группа детей с ожирением |
мином D и параметры метаболического статуса у детей |
|
|
была разделена на две подгруппы — с выраженным дефи- |
школьного возраста (7–17 лет) с ожирением. Основные |
|
|
цитом витамина [n = 18; 25(OH)D < 15 нг/мл] и нормой |
ассоциации были установлены между сниженным уров- |
|
|
[n = 24; 25(OH)D > 30 нг/мл]. Анализ протеома плазмы кро- |
нем витамина D и возрастанием инсулинорезистентности, |
|
|
ви указал на 53 белка, которые достоверно отличались между |
гипертриглицериемией, дислипидемией с увеличением ате- |
|
|
подгруппами: среди этих белков был адипонектин, низкие |
рогенных фракций липидов. |
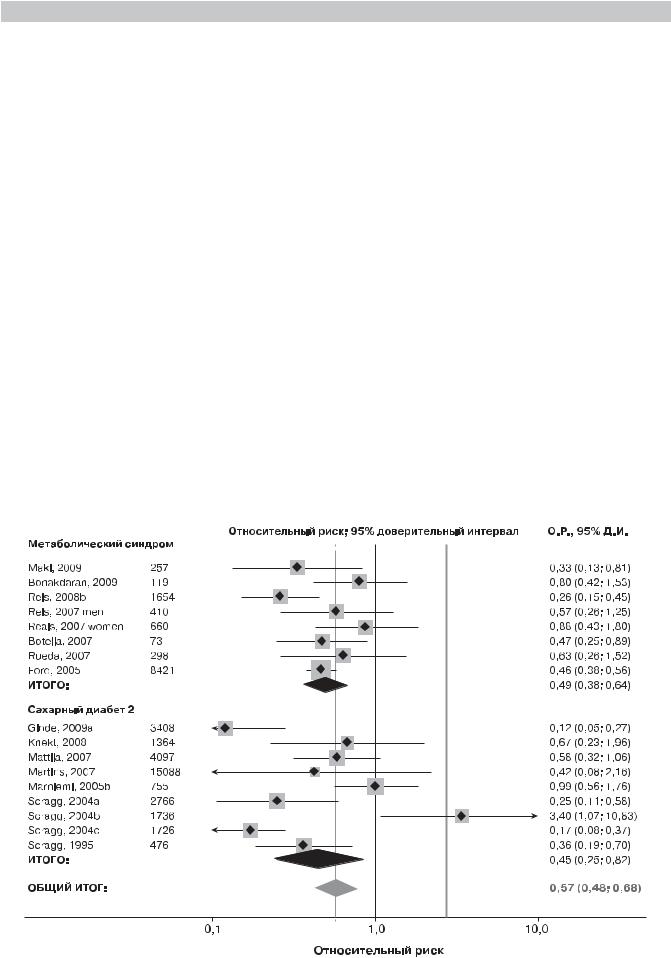
Таблица 4.11. Примеры активируемых рецептором витамина D генов, изменение уровня активности которых способствует развитию диабета
Ген |
Белок |
Функция |
|
|
|
|
|
|
|
|
|
|
Регуляция углеводного и жирового метаболизма |
|
|
||
|
|
|
|
|
|
|
|
Опосредует внутриклеточные эффекты инсулина. Дефекты |
|
|
|
IRS1 |
Cубстрат рецептора инсулина 1 |
гена нарушают транспорт и метаболизм глюкозы, приводя |
|
|
|
|
|
к инсулинонезависимому диабету (ОМИМ 125853) |
|
|
|
|
|
|
|
|
|
IGFBP3 |
Связывающие белки |
Пролонгируют время жизни инсулиноподобного фактора роста, |
|
|
|
IGFBP5 |
модулируют секрецию инсулина и выживание/апоптоз клеток |
|
|
||
инсулиноподобного фактора роста |
|
|
|||
IGFBP6 |
поджелудочной железы |
|
|
||
|
|
|
|||
|
|
|
|
|
|
PPP1R3A |
Регуляторная субъединица |
Регуляция метаболизма гликогена, дефекты гена приводят |
|
|
|
3А протеинфосфатазы |
к инсулинонезависимому диабету (ОМИМ 125853) |
|
|
||
|
|
|
|||
|
|
|
|
|
|
PPARD |
Фактор дельта пролиферации |
Регулятор бета-окисления липидов, дефекты гена способствуют |
|
|
|
пероксисом |
развитию атеросклероза и накоплению избыточной жировой ткани |
|
|
||
|
|
|
|||
|
|
|
|
|
|
|
|
Магнийзависимый белок, поддерживает стабильность геномной |
|
|
|
WRN |
Синдром Вернера |
ДНК. Дефекты гена приводят к синдрому Вернера (ОМИМ 277700) |
|
|
|
|
|
и нарушению углеводного метаболизма |
|
|
|
|
|
|
|
|
|
|
Активация адренергических сигнальных путей |
|
|
||
|
|
|
|
|
|
ADCY5 |
Аденилатциклаза 5 |
Магнийзависимый белок опосредует эффекты адренергических |
|
|
|
рецепторов |
|
|
|||
|
|
|
|
||
|
|
|
|
|
|
ADCYAP1 |
Аденилатциклазаактивирующий белок |
Активирует аденилатциклазу гипофиза |
|
|
|
|
|
|
|
|
|
ADRB3 |
Адренергический рецептор бета-3 |
Адренергическая регуляция липолиза и термогенеза |
|
|
|
|
|
|
|
|
|
ATF3 |
цАМФ-зависимый транскрипционный |
Связывает сигнальные ДНК типа CRE, модулируя эффекты белка |
|
|
|
47 |
|||||
фактор 3 |
CREB, эффекты адренергических рецепторов |
|
|||
|
|
||||
|
|
|
|
|
|
|
Иммуномодуляция и апоптоз/выживание клеток |
|
|
||
|
|
|
|
|
|
CEBPB |
ССААТ/энхансер бета-белок |
Иммуномодуляция острой фазы и воспаления |
|
|
|
|
|
|
|
|
|
NR3C1 |
Глюкокортикоидный рецептор |
Характеризуется широким спектром эффектов, включая поддержку |
|
|
|
минерального баланса и иммуномодуляцию |
|
|
|||
|
|
|
|
||
|
|
|
|
|
|
Рис. 4.17. Метаанализ ассоциации уровней витамина D в плазме крови и риска метаболических нарушений (сахарного диабета 2-го типа и метаболического синдрома) [18]

В группе детей с ожирением было проведено лечение: витамин D в дозе 1500 МЕ/сут в течение 3 месяцев, затем в дозе 2000 МЕ/сут в последующие 3 месяца (общий курс составил 6 месяцев). До лечения 100% детей имели уровень 25(ОН)D < 30 нг/мл, при этом дефицит был диагностирован у 74% из них. Через 3 месяца лечения уровень витамина D [25(ОН)D > 30 нг/мл)] восстановился у 53% детей. У остальных (47%) была констатирована недостаточность витамина D, при этом дефицит витамина D отсутствовал. Спустя 6 месяцев после лечения уровень 25(ОН)D > 30 нг/мл отмечался у всех (100%) наблюдаемых детей. Что касается метаболических нарушений, то при восстановлении уровня 25(ОН)D у 29% детей нормализовался индекс инсулинорезистентности HOMA (Homeostasis Model Assessment). Гипертриглицеридемия, наблюдаемая до терапии у 26% детей, через 3 месяца терапии сохранялась лишь у 5%, а через 6 месяцев отсутствовала у 100% обследуемых. Если до приема витамина D снижение липопротеинов высокой плотности было у 37% детей, то через 6 месяцев — лишь у 15%; повышение липопротеинов низкой плотности наблюдалось у 5% пациентов, а через 3 и 6 месяцев их уровень у всех детей был нормальным. Следует отметить, что на протяжении всего периода применения витамина D уровни ионизированного кальция и ПТГ в плазме крови оставались в референсном диапазоне.
При количественной оценке уровня лептина полу-
48чены данные, свидетельствующие о значительном повышении его в группе детей и подростков с ожирением по сравнению с группой детей с нормальной массой тела. Сывороточная концентрация адипонектина в группе детей с нормальной массой тела была выше, чем в группе с ожирением. Установлены существенные различия в метаболическом статусе, концентрации адипоцитокинов в зависимости от факта наличия и степени тяжести ожирения, стадии пубертата, степени недостаточности витамина D. Так, индекс массы тела негативно коррелировал с уровнем витамина D и позитивно — с уровнем лептина, который, в свою очередь, имеет сильную позитивную связь с индексом массы жира, что в целом подтвердило опосредованные обратные взаимоотношения уровня лептина, всегда возрастающего параллельно степени ожирения, и витамина D, снижающегося в ответ на увеличение жировой массы. Снижение витамина D, в свою очередь, вело к повышению уровня ПТГ с активацией процессов липогенеза, дальнейшим нарастанием степени ожирения, увеличением лептина и таким образом поддержанием порочного круга прогрессирования метаболических расстройств. Несмотря на то, что высокий уровень лептина является типичным при ожирении, установлены количественные различия, заключающиеся в значимом нарастании лептина при более низком уровне витамина D, что позволило отнести послед-
ний к независимым предикторам прогрессирования накопления жира. Изучаемые параметры оказывали значимое влияние на процессы липидного и углеводного обмена. Так, у детей с ожирением установлены качественные различия роли адипоцитокинов, заключающиеся в прямой корреляции лептина с атерогенными (триглицериды), а адипонектина — с неатерогенными (липопротеиды высокой плотности) фракциями липидного спектра. При этом уровень 25(ОН)D при ожирении, подобно лептину, был сильно ассоциирован с дислипидемией за счет снижения неатерогенных фракций. Более того, возрастание уровня лептина происходило сонаправленно росту инсулинорезистентности, причем данные ассоциации выявлены только у детей, вступивших в период пубертата. Что касается адипонектина, то уровень его снижался у пациентов с ожирением по сравнению с нормальной массой тела, также имелась сильная обратная корреляция сывороточного уровня адипонектина с уровнем гликированного гемо-
глобина, свидетельствующая о снижении протективного в отношении сахарного диабета эффекта адипонектина
упациентов с ожирением и более низким уровнем последнего. Взаимосвязи адипонектина с уровнем витамина D носили разнонаправленный характер.
Проведенное исследование подтвердило безопасность применения суточной дозы витамина D до 2000 МЕ/сут
удетей с ожирением [25, 26].
Взаключение следует отметить, что место каждого из исследованных параметров требует дальнейшего изучения, однако понятны тесные взаимодействия между ними, приводящие в конечном итоге к формированию самоподдерживающейся патологической системы, для размыкания которой необходима нормализация составляющих ее компонентов, к которым в первую очередь следует отнести витамин D и адипоцитокины жировой ткани.
Таким образом, недостаточная обеспеченность витамином D при ожирении повышает метаболические риски, ассоциированные с нарушениями липидного обмена и СД2, при этом восстановление статуса витамина D оказывает позитивное влияние на вышеназванные нарушения. В соответствии с большинством международных рекомендаций, при ожирении доза витамина D, необходимая для восстановления концентрации 25(ОН)D в референсном диапазоне, должна быть в 2–3 раза выше рекомендуемой для возраста (4000–6000 МЕ/сут).
ЛИТЕРАТУРА
1. Snijder M.B., van Dam R.M., et al. Adiposity in relation to vitamin D status and parathyroid hormone levels: a population-based study in older men and women. J Clin Endocrinol Metab. 2005,90:4119–23.
2.Bodnar L.M., Catov J.M., et al. Prepregnancy obesity predicts poor vitamin D status in mothers and their neonates. J Nutr. 2007;137:2437–42.
3.Ford E.S., Ajani U.A., et al. Concentrations of serum vitamin D and the metabolic syndrome among U.S. adults. Diabetes Care. 2005;28:1228–1230.
4.Norman A., Frankel J. Vitamin D deficiency inhibits pancreatic insulin secretion. Science. 1980;109:823–825.
5.Forouhi N.G., Luan J., et al. Baseline serum 25-hydroxy vitamin D is predictive of future glycemic status and insulin resistance: The Medical Research Council Ely Prospective Study 1990–2000. Diabetes. 2008;57:2619–25.
6.Mathieu C., Waer M., Laureys J., Rutgeerts O., Bouillon R. Prevention of autoimmune diabetes in NOD mice by 1,25 dihydroxyvitamin D3. Diabetologia. 1994;37(6):552–558.
7.Clifton-Bligh R.J., McElduff P., McElduff A. Maternal vitamin D deficiency, ethnicity and gestational diabetes. Diabet Med. 2008;25(6):678–684.
8.Farrant H.J., Krishnaveni G.V., Hill J.C., et al. Vitamin D insufficiency is common in Indian mothers but is not associated with gestational diabetes or variation in newborn size. Eur J Clin Nutr. 2009;63(5):646–52.
9.Zhang C., Qiu C., Hu F.B., David R.M., van Dam R.M., Bralley A., Williams M.A. Maternal plasma 25-hydroxyvi- tamin D concentrations and the risk for gestational diabetes
mellitus. PLoS One. 2008;3(11):e3753.
10.Каронова Т.Л., Гринева Е.Н., Михеева Е.П., Беляева О.Д., Красильникова Е.И., Никитина И.Л. Уровень витамина D и его взаимосвязь с количеством жировой ткани и содержанием адипоцитокинов у женщин репродуктивного возраста. Проблемы эндокринологии. 2012;6:19–23.
11.Blum M., Dolnikowski G., Seyoum E, Susan S.H. Vitamin D(3) in fat tissue. Endocr Rev. 2008;33:90–94.
12.Kull M., Kallikorm R., Lember M. Body mass index determines sunbathing habits: implications on vitamin D levels. Intern Med J. 2009;39:256–258.

13.De Paula F.J.A., Rosen C.J. Vitamin D and fat in Vitamin D. существенный вклад в повышение риска сердечно-сосуди- Eds D. Feldman, J.W. Pike, J.S. Adams. Academic Press. стой патологии.
2011. P. 769–776.
14.Walker G.E., Ricotti R., Roccio M., Moia S., Bellone S., Prodam F., Bona G. Pediatric obesity and vitamin D deficiency: a proteomic approach identifies multimeric adiponectin as a key link between these conditions. PLoS One. 2014 Jan 3;9(1):e83685.
15.Торшин И.Ю., Громова О.А. Экспертный анализ данных в молекулярной фармакологии. М.: МЦНМО, 2012. 768 с.
16.Gysemans C.A., Cardozo A.K., Callewaert H., Giulietti A., Hulshagen L., Bouillon R., Eizirik D.L., Mathieu C. 1,25-Dihydroxyvitamin D3 modulates expression of chemokines and cytokines in pancreatic islets: implications for prevention of diabetes in nonobese diabetic mice. Endocrinology. 2005;146(4):1956–64.
17.Giulietti A., van Etten E., Overbergh L., Stoffels K., Bouillon R., Mathieu C. Monocytes from type 2 diabetic patients have a pro-inflammatory profile. 1,25-Dihydroxy- vitamin D(3) works as anti-inflammatory. Diabetes Res Clin Pract. 2007;77(1):47–57.
18.Parker J., Hashmi O., Dutton D., Mavrodaris A. Levels of vitamin D and cardiometabolic disorders: systematic review and meta-analysis. Maturitas. 2010;65(3):225–36.
19.Bener A., Al-Ali M., Hoffmann G.F. High prevalence of vitamin D deficiency in young children in a highly sunny humid country: a global health problem. Minerva Pediatr. 2009 Feb;61(1):15–22.
20.Zipitis C.S., Akobeng A.K. Vitamin D supplementation in early childhood and risk of type 1 diabetes: a systematic review and meta-analysis. Arch Dis Child. 2008;93(6):512–7.
21.Dong J.Y., Zhang W.G., Chen J.J., Zhang Z.L., Han S.F., Qin L.Q. Vitamin D intake and risk of type 1 diabetes: a meta-analysis of observational studies. Nutrients. 2013;5(9):3551–62.
22.Nader N.S., Aguirre Castaneda R., Wallace J. Effect of Vitamin D3 Supplementation on Serum 25(OH)D, Lipids and Markers of Insulin Resistance in Obese Adolescents: A Prospective, Randomized, Placebo-Controlled Pilot Trial. Horm Res Paediatr. 2014 Jul;16:107–112.
23.Walker J.P., Hiramoto J.S. Vitamin D deficiency is associated with mortality and adverse vascular access outcomes in patients with end-stage renal disease. J Vasc Surg. 2014 Jul; 60(1):176–83.
24.Radhakishun N.N., van Vliet M. Efficacy and Tolerability of a High Loading Dose (25,000 IU Weekly) Vitamin D3 Supplementation in Obese Children with Vitamin D Insufficiency/Deficiency. Horm Res Paediatr. 2014 Jul; 19:103–106.
25.Тодиева А.М., Никитина И.Л., Каронова Т.Л., Васильева Е.Ю., Буданова М.В. Витамин D и метаболический статус у детей и подростков с ожирением. Вопросы детской диетологии. 2013;11(3):15–22.
26.Никитина И.Л., Тодиева А.М., Каронова Т.Л., Гринева Е.Н. К вопросу о метаболических нарушениях у детей со сниженным уровнем витамина Д и ожирением. Лечащий врач. 2014;3:10–17.
4.2.8. Дефицит витамина D
и сердечно-сосудистые заболевания
Кальцитриол [1,25(OH)2D] активно экспрессируется в тканях сердечно-сосудистой системы, в том числе кардиомиоцитах, эндотелиальных и гладкомышечных клетках сосудов [1, 2]. Как было показано выше, недостаточная обеспеченность витамином D способствует формированию инсулинорезистентности, глюкозотолерантности, ожирения и диабета. Все эти патофизиологические факторы вносят
В развитии болезней, связанных с дефицитом витамина D, имеет значение полиморфизм генов его рецептора [3]. Гетерозиготные мутации гена рецептора витамина D VDR: 283 A>G [Bsml] и VDR: 2 A>G (Lys2Arg) [FokI] приводят к повышенному риску развития колоректального рака [4], гестационного сахарного диабета [5], связаны с ускоренным разрежением костной ткани при ревматоидном артрите [6]. Полиморфизмы Bsml и ApaI связаны с долгожительством: существует значительное различие в частоте Bsml- генотипов (р = 0,037), ApaI-генотипов (р = 0,022) и ApaI- аллелей (р = 0,050) у столетних долгожителей по сравнению с 70-летними. При данных полиморфизмах у долгожителей также отмечаются нормальные показатели холестерина, артериального давления, индекса массы тела и психического здоровья [7].
Инфаркт миокарда, ишемическая болезнь сердца, инсульт являются наиболее распространенными заболеваниями и основными причинами смертности во всем мире [8, 9]. Дефицит витамина D совсем недавно был обозначен в качестве самостоятельного фактора риска сердечно-сосуди- стых заболеваний и общей смертности в общей популяции [10, 11]. Сезонные колебания смертности от сердечно-сосу- дистых заболеваний уменьшаются летом [12]. Это подчеркивает важность уточнения роли витамина D в структуре сер-
дечно-сосудистых заболеваний. Низкий уровень 25(ОН)D 49 в плазме крови является риском неблагоприятных прогнозов у больных с острым инфарктом миокарда и в кардиохирургии [13], связан с учащением частоты сердечных сокращений, повышением систолического артериального давления, что приводит к увеличению работы сердца [14].
По данным крупномасштабного исследования NHANES (2001–2004 гг.), в когорте из 4666 подростков в возрасте 12–19 лет уровень витамина D в крови был ниже у детей
свысоким систолическим артериальным давлением, низким уровнем липопротеинов высокой плотности и метаболическим синдромом [15]. УФ-излучение спектра В, стимулирующее синтез витамина D в коже, способствует снижению уровня как систолического, так и диастолического давления у пациентов с артериальной гипертензией в сочетании
сповышением уровня 25(ОН)D в сыворотке крови [16].
Вмногочисленных клинических исследованиях низкая обеспеченность витамином D была ассоциирована с нарушенным липидным профилем. Например, испанское исследование с участием 149 детей в возрасте 8–13 лет показало, что более низкие уровни 25(OH)D в сыворотке крови соответствовали более высоким уровням триглицеридов (r = -0,857; р = 0,01), причем эффект оставался статистически достоверным после поправок на возраст, пол, индекс массы тела и физическую активность [17]. Обследование здоровых добровольцев показало, что уровень витамина D выше 40 нг/мл оказывал положительное влияние на соотношение уровней холестерина и липопротеинов высокой плотности [18].
Низкая концентрация 25(OH)D в сыворотке крови ассоциируется с гипертрофией желудочков, эндотелиальной дисфункцией, повышенной жесткостью артерий и активацией ренин-ангиотензиновой системы [19, 20]. Витамин D способствует снижению активности транскрипции ренина — основного медиатора ренин-ангиотензиновой систе-
мы регуляции артериального давления [21]. 1,25(OH)2D подавляет экспрессию генов ренина, а в случае мутации гена VDR происходят повышенное производство ренина, гипертрофия сердца и повышение артериального давления. Установлена достоверная отрицательная связь между уров-
нем циркулирующего 1,25(OH)2D и активностью ренина плазмы у пациентов с гипертонической болезнью [22, 23]. Метаанализ рандомизированных контролируемых исследо-