Материал: Л5 Лекция по токсикологии и нормированию ЗВ (развернуто)
101
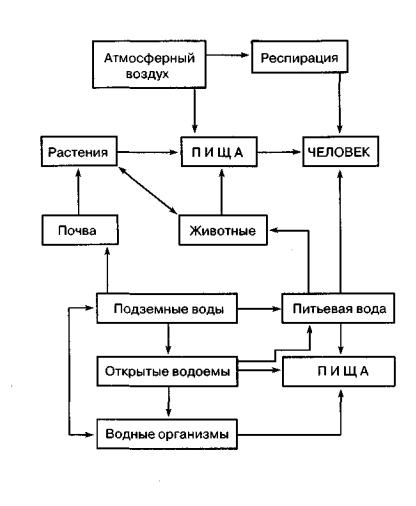
Рисунок 5 - Пути миграции загрязнителей
загрязнителей (мг/сутки) в составе пищевого рациона. Зная ДСД, ПДК и средний набор пищевых продуктов в суточном рационе, рассчитывают ПДК ксенобиотика в тех продуктах, в которых он может находиться.
Учеными [18] установлено[18], что в большинстве случаев, особенно при воздействии малых доз загрязнителей, наблюдается суммирование токсического эффекта. Это позволяет рассчитать суммарный (аддитивный)
эффект двух и более факторов, выражая каждый из них в долях предельно допустимой концентрации. Например, если в воздухе концентрация фтора составляет 0,001 мг/ м3 (ПДК 0,005), бензола - 0,16 мг/м3 (ПДК 0,8), то в сумме меньше 1 ПДК (фтора -1/5 ПДК и бензола 1/5 ПДК) и суммарное действие этих концентраций химических веществ безопасно.
102
Принцип суммирования часто применяют при расчете комплексного влияния различных загрязнителей. Например, если вещество поступает в организм человека с атмосферным воздухом, водой и пищей, то производят расчет по следующей формуле [18]:
сатм / пдкатм + своды / пдкводы + спрод./пдкпрод. < 1, (1)
где Сатм, Своды, Спрод - концентрация данного вещества в атмосфере, воде, продуктах питания;
Токсическое действие загрязнителей различных групп отличается по
критериям риска: тяжести, частоте встречаемости и времени наступления поражения. С точки зрения токсичности различают несколько групп
веществ.
.Загрязнения токсичными металлами
По одной из точек зрения, все металлы периодической системы делят на
3 группы:
металлы как незаменимые факторы питания (эссенциальные макро- и
микроэлементы),
неэссенциальные или необязательные для жизнедеятельности металлы;
токсичные металлы.
По другой точки зрения все металлы необходимы для
жизнедеятельности, но в определенных количествах.
Разработана классификация по воздействию микроэлементов на организм
человека: |
|
|
|
|
1) |
микроэлементы, имеющие значение в питании |
человека и |
||
животных (Со, Сг, Се, F, Fe, I, Mn, Mo, Ni, Se, Si, V, Zn); |
|
|||
2) |
микроэлементы, |
имеющие |
токсикологическое |
значение |
(As, Be, Cd.Co, Cr, F, Hg, Mn, Mo, Ni, Pb, Pd, Se, Sn, Ti, V, Zn). |
|
|||
Следует отметить, что 10 из перечисленных элементов отнесены в обе группы. [93]
103
Биологически эссенциальные металлы имеют пределы доз, определяющих их дефицит, оптимальный уровень и уровень токсического действия.
Токсические металлы на этой же шкале в низких дозах не оказывают вредного действия и не несут биологических функций. Однако, в высоких дозах они оказывают токсическое действие. Таким образом, не всегда возможно ус-
тановить различие между жизненно необходимыми и токсичными металлами.
Все металлы могут проявить токсичность, если они потребляются в избыточном количестве. Кроме того, токсичность металлов проявляется в их взаимодействии друг с другом. Например, физиологическое воздействие кадмия на организм, в
том числе его токсичность, зависят от количества присутствующего цинка, а
функции железа в клетках определяются присутствием меди, кобальта и в некоторой степени молибдена и цинка. Тем не менее, существуют металлы,
которые проявляют сильно выраженные токсикологические свойства при самых низких концентрациях и не выполняют какой либо полезной функции. К таким токсичным металлам относят ртуть, кадмий, свинец, мышьяк.
Они не являются ни жизненно необходимыми, ни благотворными, но в даже малых дозах приводят к нарушению нормальных метаболических функций организма.
Отравления соединениями тяжелых металлов и мышьяком
В данную группу ядов входит более 40 элементов с большой атомной массой: ртуть, свинец, медь, мышьяк, золото, железо, кадмий и другие.
Органические и неорганические соединения этих элементов могут попадать в организм человека при добыче и обработке руды в промышленнсти и про применении соединений в сельском хозяйстве
(инсектициды, гербициды). Многие тяжелые элементы (медь, ртуть, висмут)
могут входить в состав лекарств; растворы сулемы (ртуть) используют в качестве антисептиков. Свинец и многие другие его соединения используют в промышленности для приготовления сплавов (латунь), аккумуляторов,
104
кислотных аккумуляторов, в производстве хрусталя, красок (свинцовые белила), глазури (для гончарных изделий).
Ртуть получают путем обжига минерала киновари. Ртуть – жидкий металл, испаряется даже при t=0oC, превращается при этом в бесцветный пар без запаха. Опасность ртутных отравлений может возникать при добыче ртути на рудниках, выплавке её из руд, на электростанциях, при изготовлении радиовакуумных приборов, рентгеновских трубок, ртутных насосов. (ПДК ртути в воздухе – 0.01 мг/м3).
Ртуть (Hg) человек знает в течение многих веков. Легко извлекается из руд. Ртуть - металл, в нормальных условиях жидкость, из-за этого свойства ртуть была названа "жидким серебром". Раньше ртуть ценилась в основном своими медицинскими свойствами, также использовалась для серебрения зеркал в смеси с другими металлами. В последнее столетие доказано, что ртуть участвует как катализатор во многих химических реакциях. Благодаря своим свойствам широко применяется в промышленности. Ртуть ис-
пользуют:
-для производства электродов,
-при производстве красок,
-для производства ртутных приборов (термометры),
-в агрохимии,
-при получении детонаторов и катализаторов,
-в производстве бумаги,
-фармацевтике и косметике,
-в военных целях.
Промышленное значение имеют высокотоксичные неорганические соединения ртути - сулема, из которой получают другие ртутные соединения. Сулему применяют, при травлении стали. Вызывает смертельные отравления в количестве 0.2-0.3 г при приеме внутрь. При
105
обработке зерна применяли органические соединения ртути в качестве фунгицидов. Во многих странах мира с тех пор, как стало известно об опасности таких соединений, их использование было запрещено.
Ежегодно 10 тыс. тонн металла выделяется в окружающую среду при сгорании угля, нефти и газа, добыче пустой породы и других индустриальных разработках [77]. Естественным образом ежегодно от 30
тыс. до 150 тыс. тонн ртути выделяется при дегазации земной коры и океанов.
Ртуть относится к числу рассеянных в природе микроэлементов. По распространению в земной коре она занимает 62-е место, средняя концентрация составляет 0,5 мг/кг. В природе присутствует атомарная
(металлическая) ртуть и окисленная (со степенью окисления +1 и +2). Свойства ртути в различных степенях окисления определяются окислительно-восстанови-
тельным потенциалом раствора и присутствием комплексных соединений. Ион
Hg2+ может образовывать стабильные комплексы с биологическими соединениями, особенно через сульфгидрильные группы. Хорошо взаимодействует с хлором.
В пищевых продуктах может присутствовать атомарная ртуть, окисленная ртуть Hg2+ и алкилртуть.
Случаи загрязнения пищевых продуктов металлической ртутью являются очень редкими. Ртуть плохо адсорбируется на продуктах и легко удаляется с поверхности пищи. С токсикологической точки зрения ртуть Наибольшую опасность ртуть представляет, присоединяясь к углеродному атому метиловой,
этиловой или пропиловой группы - это алкильные соединения с короткой цепью. Процесс метилирования ртути является ключевым звеном биокумуляции по пищевым цепям водных экосистем.
Ртуть аккумулируют планктонные организмы (например, водоросли),
которыми питаются ракообразные. Ракообразных поедают рыбы, а рыб птицы.
Концевыми звеньями пищевых цепей нередко бывают чайки и орланы. Человек