Материал: Концентрация растворов
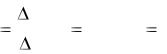
Т = t0C + 273 = 25 + 273 = 298K,
G0х.р. = − 71,0 − 298·(−0,021) = −64,7 кДж.
Ответ: Так как G0х.р. < 0, реакция протекает в прямом направлении.
Пример 4. При какой температуре наступит равновесие в системе:
2CH4(г) = C2H2(г) + 3H2(г)?
Решение:
В прил. 1 находим значения энтальпий образования для веществ, участвующих в реакции:
H0(CH4) = −74,9 кДж/моль;
H0(C2H2) = 226,8 кДж/моль;
H0(H2) = 0 кДж/моль (простое вещество). По следствию из закона Гесса
H0х.р. = H0(C2H2) + 3 H0(H2) − 2 H0(CH4),
H0х.р. = 226,8 + 3·0 − 2(−74,9) = 376,6 кДж.
Аналогично находим изменение энтропии, используя стандартные значения из прил. 1:
S0(CH4) = 186,2 Дж/моль · К;
S0(C2H2) = 200,8 Дж/моль · К; S0(H2) = 130,5 Дж/моль · К,
S0х.р. = S0(C2H2) + 3S0(H2) − 2S0(CH4),
S0х.р. = 200,8 + 3·130,5 − 2·186,2 = 219,9 Дж/К = 0,2199 кДж/К.
Теперь можно рассчитать температуру, при которой достигается равновесие:
T |
H |
х0. р. |
|
376,6 |
|
1712К . |
S |
0 |
0,2199 |
||||
|
х. р. |
|
||||
|
|
|
|
|
|
|
Ответ: Травн = 1712 К.
21
Пример 5. Рассчитайте значение стандартной энтальпии реакции образования одного моля оксида железа (III) из простых веществ по следующим термохимическим уравнениям:
2Fe(т) + О2(г) = 2FeO(т); |
H0х.р. = −532 кДж, |
|
4FeO(т) + О2(г) = 2Fe2O3(т); |
H0х.р. = −584 кДж. |
|
Решение: |
|
|
Получить оксид железа (III) из простых веществ можно либо |
||
сразу по реакции |
|
|
2Fe + 3/2 О2 = Fe2O3; |
H0х.р.(1), |
|
либо в два этапа, сначала получив оксид железа (II): |
||
2Fe + O2 = 2FeO; |
H0х.р.(2) |
|
2FeO + ½ O2 = Fe2O3; |
H0х.р.(3) |
|
Согласно закону Гесса, тепловой эффект химической реакции зависит только от природы и состояния исходных веществ и продуктов реакции, но не зависит от пути перехода системы из начального в конечное состояние. То есть
H0х.р.(1) = H0х.р.(2) + H0х.р.(3)
Очевидно, что H0х.р.(2) равен тепловому эффекту первой из указанных в задании реакций:
H0х.р.(2) = −532 кДж.
В то же время H0х.р.(3) равен половине теплового эффекта второй из указанных в задании реакций:
H0х.р.(3) = −584/2 = −292 кДж.
Значит, тепловой эффект реакции получения одного моля оксида железа (III) из простых веществ H0х.р.(1) можно рассчитать:
H0х.р.(1) = −532 + (−292) = −824 кДж. Ответ: H0х.р.(1) = −824 кДж.
22

3. Растворы неэлектролитов и электролитов
Некоторые свойства растворов зависят только от количества частиц растворенного вещества и не зависят от его природы. К таким свойствам относятся, в первую очередь, осмотическое давление и изменение температур замерзания и кипения растворов по сравнению с соответствующими температурами чистого растворителя.
3.1. Замерзание и кипение растворов
Все растворители имеют определенные температуры замерзания (кристаллизации) и кипения. Присутствие в них растворенного вещества понижает температуру замерзания и повышает температуру кипения на некоторую величину t. Для разбавленных растворов неэлектролитов эту величину можно рассчитать по следствию из закона Рауля:
tзам = Ккр · Сm ; Δtкип = Кэб · Сm ,
где Ккр – криоскопическая постоянная; Кэб – эбуллиоскопическая постоянная;
Сm – моляльная концентрация.
Криоскопическая и эбуллиоскопическая постоянные – константы, зависящие только от природы растворителя. Значения этих констант приводятся в справочниках. Например, для воды Ккр = 1,86;
Кэб = 0,52.
Моляльная концентрация, или моляльность, показывает, сколько молей растворенного вещества приходится на 1000 граммов растворителя.
Моляльность может быть рассчитана по формуле:
Cm = |
m(вещества) 1000 |
, |
|
M (вещества) m( растворителя) |
|||
|
|
где m(вещества) – масса растворенного вещества, г; m(растворителя) – масса растворителя, г;
M(вещества) – молярная масса растворенного вещества, г/моль.
23
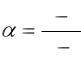
В растворах электролитов при равной молярной концентрации количество частиц больше, чем в растворах неэлектролитов. Это связано с диссоциацией молекул на ионы. Увеличение числа частиц за счет диссоциации молекул учитывают с помощью изотонического коэффициента (i). Этот коэффициент зависит от степени диссоциации (α) и от числа ионов (n), на которые диссоциирует одна молекула. Например:
HCl  H+ + Cl− (два иона, n = 2); MgCl2
H+ + Cl− (два иона, n = 2); MgCl2  Mg2+ + 2Cl− (три иона, n = 3);
Mg2+ + 2Cl− (три иона, n = 3);
Al2(SO4)3  2Al3+ + 3SO42- (пять ионов, n = 5).
2Al3+ + 3SO42- (пять ионов, n = 5).
Зависимость изотонического коэффициента от числа ионов и степени диссоциации имеет вид:
i 1 n 1 .
Формулы для расчета изменения температур замерзания и кипения для электролитов можно записать в виде:
tзам = i · Ккр · Сm ;
Δtкип = i · Кэб · Сm .
3.2. Осмотическое давление
Осмосом называется процесс односторонней диффузии молекул растворителя в раствор через полупроницаемую перегородку. Мерой интенсивности этого процесса является осмотическое давление.
Осмотическое давление растворов неэлектролитов зависит от концентрации раствора и температуры. Эта зависимость имеет вид:
Росм = СМ · R · T,
где R – универсальная газовая постоянная, R = 8,31 Дж/моль · К; Т – абсолютная температура; СМ – молярная концентрация раствора.
24

Молярная концентрация (или молярность) показывает, сколько молей растворенного вещества содержится в одном литре раствора. Она может быть рассчитана по формуле:
CM = |
m(вещества) |
. |
|
M (вещества) V ( раствора) |
|||
|
|
Для растворов электролитов при расчете осмотического давления также следует использовать изотонический коэффициент:
Росм = i · СМ · R · T.
3.3. Водородный показатель (рН)
Важнейшей характеристикой растворов электролитов является водородный показатель (рН), который определяет реакцию среды в растворе.
Водородный показатель определяется концентрацией ионов водорода в растворе:
рН = − lg[H+],
где [H+] – концентрация ионов водорода. Эту же зависимость можно записать:
[H+] = 10 pH .
Вода – слабый электролит, диссоциирующий на ионы водорода
и гидроксильные ионы: |
|
Н2О |
Н+ + ОН− |
В чистой воде концентрации ионов водорода и гидроксидионов одинаковы. При 250С концентрация этих ионов составляет 10 – 7 моль/л.
Произведение концентраций этих ионов – величина постоянная:
[H+]·[OH −] = 10–14.
Эта зависимость называется ионным произведением воды.
В нейтральных водных растворах, как и в чистой воде, [H+] = [OH −] = 10−7 моль/л. Значит, в нейтральной среде
рН = - lg(10−7) = 7.
Вкислой среде [H+] > [OH −]. Значит, рН < 7.
Вщелочной среде [H+] < [OH −] и рН > 7.
25