Материал: Концентрация растворов

Пример 7. К 100 мл 27%-ного раствора NaOH с плотностью 1,3 г/мл прибавили 260 мл воды. Вычислите нормальность полученного раствора, если его плотность 1,1 г/мл.
В этой задаче речь идет о двух растворах: исходном и полученном. Поэтому при записи условия и в процессе решения задачи следует четко обозначать, к какому именно раствору относятся используемые величины. Для этого можно использовать цифры 1(исходный раствор) и 2 (полученный раствор).
Дано:
V1(р-ра) = 100 мл
ω1(NaOH) = 27%
ρ1 = 1,3 г/мл V(H2O) = 260 мл
ρ2 = 1,1 г/мл
СН(2) = ?
Решение:
Для расчета нормальной концентрации полученного раствора по формуле
m (NaOH)
CН(2) = M 2 V
Э (NaOH) 2( раствора)
надо знать массу NaOH в полученном растворе, объем этого раствора и молярную массу эквивалента NaOH.
1. Найдем массу NaOH.
При добавлении воды к исходному раствору масса растворенного вещества не изменяется. Значит, достаточно найти массу NaOH в исходном растворе.
Определим массу исходного раствора:
m1(р-ра) = V1(р-ра) · ρ1(р-ра) = 100 . 1,3 = 130 г.
Из формулы для расчета массовой доли
ω = m(вещества) ·100% m( раствора)
найдем массу растворенного вещества (NaOH):
m(NaOH ) |
m( р ра) |
130 27 |
35,1г, |
||
100 |
|
100 |
|||
|
|
||||
то есть m2(NaOH) = m1(NaOH) = 35,1 г.
11
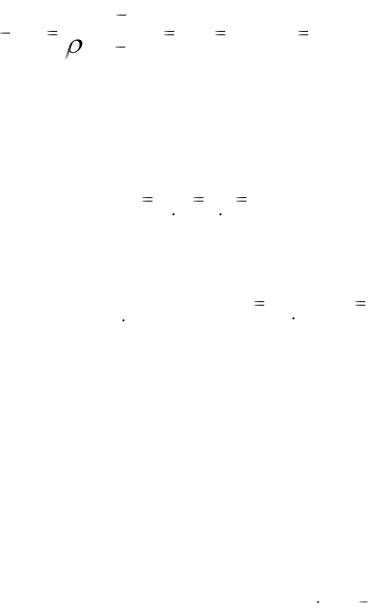
2. Найдем объем полученного раствора.
Масса полученного раствора складывается из массы исходного раствора (130 г) и массы добавленной воды. Так как плотность воды равна 1 г/мл, то
m(H2O) = V(H2O) . ρ(H2O) = 260 . 1 = 260 г.
Значит,
m2(р-ра) = m1(р-ра) + m(H2O) = 130 + 260 = 390 г.
Тогда
|
|
m ( р ра) |
390 |
|
||
V |
( р ра) |
2 |
|
|
|
354,5мл 0,3545л . |
|
|
|
|
|||
2 |
|
2 ( р ра) |
1,1 |
|
|
|
|
|
|
|
|||
3. Определим молярную массу эквивалента NaOH.
Ее можно рассчитать по формуле эквивалента сложного вещества:
MЭ (NaOH) |
M |
40 |
|
40 г/моль |
|
|
|
|
|
||
n z |
1 1 |
||||
4. Подставим полученные значения в исходную формулу:
|
m (NaOH) |
35,1 |
|
|
||
CН(2) = |
2 |
|
|
|
2,48н . |
|
MЭ (NaOH) V2( раствора) |
40 0,3545 |
|||||
|
|
|||||
|
|
|
|
|
||
Ответ: CН(2) = 2,48н.
Пример 8. Какой объем 1,2M раствора нитрата калия потребуется для приготовления 2 литров 5%-ного раствора этого вещества, если плотность полученного раствора 1,05 г/мл?
Дано: |
Решение: |
|
|
|
СМ(1) = 1,2М |
Объем исходного раствора можно найти из |
|||
V2(р-ра) = 2 л = 2000 мл |
формулы для расчета молярной концентрации: |
|||
ω2(KNO3) = 5% |
|
m1(KNO3 ) |
|
|
ρ = 1,05 г/мл |
CM(1) = |
|
. |
|
|
|
|||
2 |
|
M (KNO3 ) V1( р |
ра) |
|
|
|
|||
V1(р-ра) = ? |
Для нахождения объема надо знать моляр- |
|||
ную концентрацию исходного |
|
раствора |
||
|
|
|||
|
(СМ(1)=1,2М), молярную массу нитрата калия |
|||
|
||||
12

(M(KNO3) = 101 г/моль) и массу растворенного вещества.
При разбавлении раствора масса растворенного вещества не изменяется, то есть масса нитрата калия в исходном и в полученном растворе одинакова.
Для того чтобы найти массу растворенного вещества в полученном растворе, надо знать массу этого раствора:
m2(р-ра) = V2(р-ра) . ρ2(р-ра) = 2000 . 1,05 = 2100 г.
Теперь из формулы для расчета массовой доли можно найти массу нитрата калия:
|
|
m ( р ра) |
2 |
(KNO3 ) |
2100 5 |
|
|
|
m |
(KNO3 ) |
2 |
|
|
|
105 |
г. |
|
100% |
|
|
100 |
|||||
2 |
|
|
|
|
|
|||
Выразим из исходной формулы объем и подставим все известные величины:
V1( р ра) |
m(KNO3 ) |
|
105 |
|
0,866 л 866 мл |
|
CМ (1) M (KNO3 ) |
1,2 101 |
|||||
|
|
|||||
|
|
|
|
|
||
Ответ: V1(р-ра) = 866 мл.
Пример 9. Для нейтрализации 50 мл серной кислоты потребовалось 25 мл 0,2н раствора щелочи. Определите нормальность раствора кислоты.
Дано: |
|
Решение: |
|
|
|
|
|
|
|
|
V (к-ты) = 50 мл |
|
Используем закон эквивалентов для раство- |
||||||||
V(щ) = 25 мл |
|
ров |
|
|
|
|
|
|
|
|
СН(щ) = 0,2н |
|
|
СН(к-ты) |
. |
V(к-ты) = CH(щ) |
. |
V(щ) |
|||
СН(к-ты) = ? |
|
|
|
|
||||||
|
Тогда |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|||
|
СН(к-ты) = |
СН (щ) V (щ) |
|
|
0,2 25 |
0,1н . |
|
|
||
|
V (к ты) |
|
|
50 |
|
|
|
|||
|
|
|
|
|
|
|
|
|||
Ответ: СН(к-ты) = 0,1н.
13

Пример 10. Сколько граммов цинка можно растворить в 100 мл
2н соляной кислоты? |
|
|
Дано: |
Решение: |
|
V (к-ты) = 100 мл = 0,1 л |
Для решения этой задачи используем |
|
закон эквивалентов: |
||
СН(к-ты) = 2н |
||
|
||
m(Zn) = ? |
nЭ(к-ты) = nЭ(Zn). |
|
|
||
|
|
Так как кислота взята в виде раствора, то число эквивалентов кислоты
nЭ(к-ты) = СН(к-ты) . V(к-ты).
Цинк участвует в реакции в виде чистого вещества. Тогда число эквивалентов цинка
m(Zn) nэ (Zn) M Э (Zn) .
Подставив это выражение в исходную формулу, получим закон эквивалентов в виде:
m(Zn)
CН (к ты) V (к ты) M Э (Zn) .
Молярная масса эквивалента цинка может быть рассчитана, как молярная масса эквивалента простого вещества:
MЭ |
(Zn) |
A |
65 |
32,5 . |
||
|
|
|
||||
z |
2 |
|||||
|
|
|
||||
Тогда массу цинка можно выразить из закона эквивалентов и рассчи-
тать
m(Zn) CН (к ты)  V (к ты)
V (к ты)  M Э (Zn) 2
M Э (Zn) 2  0,1
0,1 32,5 6,5 г .
32,5 6,5 г .
Ответ: m(Zn) = 6,5 г.
14

2. Химическая термодинамика
Химическая термодинамика – раздел химии, изучающий взаимопревращения различных видов энергии при протекании химических процессов.
2.1. Энтальпия. Тепловой эффект химической реакции
Протекание химических реакций сопровождается выделением или поглощением энергии в виде тепла. Энергия системы, которая может быть превращена в тепло при постоянном давлении, называется энтальпией и обозначается «Н». Абсолютное значение энтальпии измерить невозможно, но можно измерить ее изменение (ΔН).
Количество теплоты, выделяющееся или поглощающееся при протекании химической реакции, называется тепловым эффектом реакции.
Тепловой эффект химической реакции, протекающей при постоянном давлении и температуре, равен изменению энтальпии системы (ΔНх.р.).
Реакции, протекающие с выделением теплоты, называются экзотермическими. В этих реакциях запас энергии уменьшается, поэтому Нх.р.< 0.
Реакции, протекающие с поглощением теплоты, называются эндотермическими. В этих реакциях запас энергии системы увеличивается, поэтому Нх.р.> 0.
В основе термохимических расчетов лежит закон Гесса:
Тепловой эффект химической реакции зависит только от природы и состояния исходных веществ и продуктов реакции, но не зависит от пути перехода системы из начального в конечное состояние.
Часто в термохимических расчетах используют следствие из закона Гесса:
Тепловой эффект химической реакции равен сумме энтальпий образования продуктов реакции за вычетом энтальпий образования исходных веществ с учетом коэффициентов перед формулами этих веществ в уравнении реакции.
15