Материал: Концентрация растворов
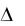
То есть
Нх.р. = ∑ΔНпрод. - ∑ΔНисх.
Энтальпией образования вещества называется тепловой эффект реакции образования одного моля этого вещества при стандартных условиях из простых веществ, взятых в устойчивом состоянии.
Стандартными условиями считаются температура 250С (298К) и давление 1атм.
Стандартные энтальпии образования многих сложных веществ приведены в справочниках. Для решения задач можно использовать приложение 1.
Энтальпии образования простых веществ в устойчивом состоянии принимаются равными нулю.
Энтальпию образования вещества иногда называют теплотой образования.
Тепловой эффект реакции, протекающей при стандартных условиях, обозначается H х0. р. .
2.2. Энтропия. Энергия Гиббса. Направление протекания реакции
Любые процессы самопроизвольно могут протекать только в направлении уменьшения запаса энергии в системе. Однако при этом следует принимать во внимание не только тепловую энергию (энтальпию), но и вероятностный фактор. Этот фактор характеризуется термодинамической величиной, которая называется энтропия (S).
Энтропия системы отражает хаотичность движения и взаимного расположения частиц вещества и является мерой неупорядоченности системы. Частицы вещества (ионы, атомы, молекулы) непрерывно совершают разные виды движения (поступательное, вращательное, колебательное), переходя из одного микросостояния в другое. Чем больше число возможных микросостояний, тем больше неупорядоченность системы, тем больше энтропия.
Термодинамические системы, которые не обмениваются с внешней средой ни веществом, ни тепловой энергией, называются изолированными. Запас тепловой энергии в такой системе не изменяется, то есть
16

Н = 0. Поэтому направление протекания процесса определяется только вероятностным фактором.
В изолированной системе самопроизвольно могут протекать только такие процессы, которые сопровождаются увеличением энтропии (возрастанием неупорядоченности).
Энтропия вещества резко возрастает при переходе из твердого
состояния в |
жидкое |
и |
далее – в |
газообразное. Поэтому |
об изменении |
энтропии |
в |
химической |
реакции можно судить |
по количеству газообразного вещества до и после реакции.
Изменение энтропии при протекании химической реакции можно точно рассчитать по следствию из закона Гесса, используя стандартные энтропии веществ, приведенные в справочниках (см. прил. 1):
Sх.р. = ∑Sпрод. - ∑Sисх.
При этом, в отличие от энтальпии образования, энтропия простого вещества не равна нулю.
Критерием направленности процессов в неизолированной системе является изменение энергии Гиббса (ΔG), которая учитывает как энтальпийный (тепловой), так и энтропийный (вероятностный) фактор.
Энергия Гиббса связана с энтальпией и энтропией соотношением:
G = H – TΔS,
где T – абсолютная температура.
Самопроизвольно возможно протекание только таких процессов, в которых энергия Гиббса уменьшается (ΔG < 0).
Протекание экзотермических химических реакций (ΔH < 0), сопровождающихся возрастанием энтропии (ΔS > 0), возможно, так как в этом случае G < 0.
Эндотермические реакции (Δ H > 0), сопровождающиеся уменьшением энтропии (ΔS < 0), самопроизвольно в прямом направлении протекать не могут, так как в этом случае G > 0. Реакция может протекать только в обратном направлении.
Если же H < 0 и ΔS < 0, а также если H > 0 и ΔS > 0, термодинамическая возможность протекания реакции определяется кон-
17
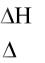
куренцией энтальпийного и энтропийного факторов, в которую вмешивается температура.
Например, если H < 0 и ΔS < 0, то при низкой температуре преобладает энтальпийный фактор (ΔH), G < 0 и реакция протекает в прямом направлении. Повышение температуры усиливает влияние энтропийного фактора. G становится больше нуля. Поэтому при высокой температуре та же реакция может протекать только в обратном направлении.
То есть при повышении температуры происходит изменение знака G и направления протекания реакции. Значит, при какой-то температуре G = 0 и система находится в равновесии.
В этом случае температуру равновесия можно рассчитать:
Травн = |
|
. |
|
S |
|||
|
|
2.3. Примеры решения задач по теме «Химическая термодинамика»
Пример 1. Рассчитайте тепловой эффект реакции
3Fe(к) + 4H2O(г) = 4H2(г) + Fe3O4(к),
протекающей при стандартных условиях.
Экзоили эндотермической является эта реакция?
Решение:
По следствию из закона Гесса
H0х.р. = 4 Н0(H2) + H0(Fe3O4) − 3ΔH0(Fe) − 4ΔH0(H2O).
В прил. 1 находим значения энтальпий образования для Fe3O4 и
H2O:
H0(Fe3O4) = − 1117,1 кДж/моль; H0(H2O)= − 241,8 кДж/моль.
Энтальпии образования простых веществ равны нулю. Поэтому
Н0(H2) = 0; H0(Fe) = 0.
18
Подставим в формулу численные значения энтальпий образования веществ:
H0х.р. = 4·0 + (− 1117,1) − 3·0 − 4(− 241,8) = − 149,9 кДж.
Так как H0х.р. < 0, реакция экзотермическая.
Ответ: H0х.р. = − 149,9 кДж. Реакция экзотермическая.
Пример 2. Реакция горения пропана выражается термохимическим уравнением:
C3H8(г) + 5O2(г) = 3СО2(г) + 4Н2О(г); H0х.р. = –2043,8 кДж.
Вычислите энтальпию образования пропана.
Решение:
По следствию из закона Гесса
H0х.р. = 4 H0(H2O) + 3 H0(CO2) − 5 H0(O2) − H0(C3H8).
Следовательно,
H0(C3H8) = 4ΔH0(H2O) + 3ΔH0(CO2) − 5ΔH0(O2) − H0х.р.
В прил. 1 находим значения энтальпий образования для CO2 и
H2O:
H0(CO2) = − 393,5 кДж/моль;
H0(H2O) = − 241, 8 кДж/моль.
Энтальпии образования простых веществ равны нулю. Поэтому
H0(O2) = 0.
Подставим в формулу численные значения энтальпий образования веществ:
H0(C3H8) = 4 · (− 241, 8) + 3 . (− 393,5) − 5 · 0 − (− 2043,8) = −103,9 кДж/моль.
Ответ: H0(C3H8) = –103,9 кДж/моль.
19
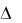
Пример 3. Пользуясь значениями H 0 и S0, определите направление протекания реакции при 250С:
SO2(г) + NO2(г) = SO3(г) + NO(г).
Решение:
Направление протекания реакции можно определить по знаку G0х.р. Изменение энергии Гиббса связано с энтальпией и энтропией
соотношением:
G0х.р. = H0х.р. – T S0х.р.
По следствию из закона Гесса
H0х.р. = H0(SO3) + H0(NO) − H0(SO2) − H0(NO2).
В прил. 1 находим значения энтальпий образования для веществ, участвующих в реакции:
H0(SO3) = − 395,2 кДж/моль; H0(NO) = 90,3 кДж/моль; H0(SO2) = − 296,9 кДж/моль; H0(NO2) = 33,0 кДж/моль.
Тогда
H0х.р. = − 395,2 + 90,3 − (− 296,9) − 33,0 = − 71,0 кДж.
Аналогично находим изменение энтропии, используя стандартные значения из прил. 1.
S0х.р. = S0(SO3) + S0(NO) − S0(SO2) − S0(NO2),
S0(SO3) = 256,7 Дж/моль · К;
S0(NO) = 210,6 Дж/моль · К;
S0(SO2) = 248,1 Дж/моль · К;
S0(NO2) = 240,2 Дж/моль · К,
S0х.р. = 256,7 + 210,6 − 248,1 − 240,2 = −21 Дж/К = −0,021 кДж/К.
Используя полученные значения, можно рассчитать изменение энергии Гиббса:
G0х.р. = H0х.р. − T · S0х.р.,
20