Материал: Концентрация растворов
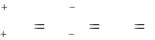
Степень диссоциации кислоты составляет 1%. Это значит, что из 100 молекул кислоты в диссоциированном состоянии находится только одна. То есть
[H+] = CM(к-ты)· α = 0,1 · 0,01 = 0,001 = 10−3 моль/л.
Определим рН раствора:
рН = − lg[H+] = − lg(10−3) = 3.
Ответ: рН раствора равен 3.
Пример 8. Вычислите, во сколько раз нужно увеличить или уменьшить концентрацию ионов водорода в растворе, чтобы величина рН увеличилась на две единицы.
Решение:
Возьмем любое исходное значение рН, например 5.
Тогда при увеличении исходного значения на две единицы получим новое значение рН, равное 7.
Рассчитаем концентрацию ионов водорода в исходном и в полученном растворах.
[H+]1 = 10−pH = 10−5 моль/л. [H+]2 = 10−pH = 10−7 моль/л.
Тогда
[H ]1 |
10 |
5 |
10 |
2 |
100 |
|
|
|
|
|
|
||
[H ] |
10 7 |
|
||||
|
|
|
||||
2 |
|
|
|
|
|
|
То есть концентрация ионов водорода в исходном растворе в 100 раз больше, чем в полученном.
Ответ: концентрацию ионов водорода надо уменьшить в 100 раз.
31
4. Электрохимия
Этот раздел курса химии изучает химические процессы, либо протекающие под действием электрического тока (электролиз), либо сопровождающиеся возникновением тока (гальванический элемент, коррозия).
Все электрохимические процессы – это окислительно-восстано- вительные реакции, то есть реакции, сопровождающиеся изменением степени окисления элементов. Процесс отдачи электронов называется окислением. Степень окисления элемента при этом увеличивается. Процесс присоединения электронов называется восстановлением. При этом степень окисления элемента уменьшается. Процессы окисления и восстановления взаимосвязаны и не могут протекать один без другого.
Электрохимические процессы отличаются от обычных окисли- тельно-восстановительных реакций тем, что они протекают не во всем объеме раствора, а только на поверхности электродов. Электроды обычно изготовляются из различных металлов. Часто в качестве материала электрода используется графит. При этом процессы окисления и восстановления разделены в пространстве, а передача электронов от восстановителя к окислителю осуществляется через внешнюю цепь.
В зависимости от характера протекающего процесса электрод называют анодом или катодом.
Анодом называется электрод, на котором протекает процесс
окисления.
Катодом называется электрод, на котором протекает процесс
восстановления.
Важнейшей характеристикой электрода, определяющей его активность, является его потенциал.
4.1. Электродный потенциал
При погружении металла в раствор электролита на границе раздела металл–раствор возникает разность потенциалов или электродный потенциал. Абсолютную величину этого потенциала измерить нельзя. Можно измерить лишь разность потенциалов между
32

двумя электродами. Второй электрод в этой системе называется электродом сравнения. В качестве электродов сравнения могут использоваться различные электроды, обладающие постоянным потенциалом. Но исторически принято сравнивать потенциалы с потенциалом стандартного водородного электрода, который принимается равным нулю.
Потенциал металла, погруженного в раствор, содержащий ионы этого металла, концентрация которых составляет 1 моль/литр, называется стандартным потенциалом. Значения стандартных потенциалов для различных металлов приводятся в справочниках (см. прил. 2 )
Изменение концентрации ионов металла в растворе приводит к изменению величины электродного потенциала. Зависимость потенциала от концентрации раствора выражается уравнением Нернста:
E = E0 + RTzF lnC,
где E – равновесный электродный потенциал, В; E0 – стандартный электродный потенциал, В;
R – универсальная газовая постоянная (8,31 |
Дж |
); |
|
моль K |
|||
|
|
||
Т – абсолютная температура, К; |
|
|
z – абсолютная величина заряда иона металла; F – число Фарадея (96500 Кл);
С – концентрация ионов металла в растворе, моль/л.
Если в уравнении Нернста заменить величины R и F их численными значениями, а натуральный логарифм – десятичным, то для температуры 250С или 298К (стандартное значение) оно примет вид:
E = E0 + |
0,059 |
lgC. |
|
z |
|||
|
|
Так как изменение концентрации ионов металла в растворе приводит к относительно небольшому изменению потенциала, при
33

определении характера протекающей на поверхности электрода реакции в первом приближении можно использовать стандартные значения потенциала.
Электродный потенциал является важной характеристикой металла, определяющей его поведение в различных электрохимических системах. Чем меньше потенциал металла, тем более активным является этот металл, то есть тем легче протекает процесс
Me0 - zē Mez+.
Чем больше потенциал, тем легче протекает обратный процесс
Mez+ + zē Me0,
то есть тем легче выделить металл из раствора.
4.2. Гальванический элемент
Гальванический элемент представляет собой устройство, предназначенное для получения электрического тока за счет протекания химической окислительно-восстановительной реакции. При этом ток возникает при движении электронов от восстановителя к окислителю через внешнюю цепь. Гальванический элемент состоит из двух электродов, то есть двух металлов, погруженных в растворы электролитов. Электролитами обычно являются растворы солей этих металлов. Электролиты разделяются пористой перегородкой, которая не позволяет электролитам перемешиваться, но не препятствует протеканию электрического тока.
При схематическом изображении гальванического элемента граница раздела между металлом и раствором обозначается вертикальной чертой, граница раздела между растворами – двойной вертикальной чертой. Например, схема гальванического элемента, состоящего из цинкового и медного электродов, имеет вид:
Zn| ZnSO4 || CuSO4 |Cu
При замыкании внешней цепи в гальваническом элементе электроны будут двигаться от электрода с меньшим значением потенциала к электроду с более высоким потенциалом.
34
В приведенном примере
Е0(Zn2+/Zn0) = -0,76В (см. прил. 2),
E0(Cu2+/Cu0) = +0,34В.
Значит цинк отдает электроны. На электроде протекает процесс окисления. Электрод является анодом. Можно записать:
Анод: Zn0 – 2ē = Zn2+
Медь принимает электроны. На электроде протекает процесс восстановления. Электрод является катодом. Можно записать:
Катод: Cu2+ + 2ē = Cu0
Так как потенциал цинка меньше потенциала меди, в этом гальваническом элементе цинковый электрод имеет знак «минус», медный – «плюс».
Таким образом, в гальваническом элементе электрод
с меньшим значением потенциала (более активный металл) является анодом и имеет знак «минус».
4.3. Коррозия
Коррозия – это процесс разрушения металла под действием окружающей среды. Чаще всего протекающие при этом процессы имеют электрохимический характер. При электрохимической коррозии на поверхности металла образуются гальванические микроэлементы. Причины их образования многообразны. Это и примеси других металлов, и поры в оксидных пленках, и неоднородность поверхности металла.
Анодным процессом при коррозии всегда является процесс окисления (разрушения) металла:
Анод: Ме0 – zē = MeZ+
Катодный процесс при коррозии в первую очередь зависит от того, в каких условиях протекает коррозия.
При коррозии в атмосферных условиях или в нейтральных растворах окислителем обычно является кислород воздуха. В этом
35