Материал: Изучение закономерностей формирования наночастиц кобальта в структуре полимерных матриц на основе модифицированного тетрафторэтилена
2. Экспериментальная часть
.1 Использованные реактивы и растворы
В работе использовались следующие реактивы: 6-водный хлорид кобальта, хлорид натрия, боргидрид натрия, азотная кислота, перекись водорода, дистиллированная вода, модифицированные перфторированные мембраны марки МФ-4СК.
Все используемые реактивы имели квалификацию "химически чистый", 6-водный хлорид кобальта дополнительно перекристаллизован.
Их данных реактивов были приготовлены следующие растворы:
исходный раствор хлорида кобальта концентрацией 0,1 моль/л в дистиллированной воде;
исходный раствор хлорида натрия концентрацией 0,1 моль/л в дистиллированной воде;
раствор хлорида натрия концентрацией 1,5 моль/л;
раствор боргидрида натрия концентрацией 2 моль/л в дистиллированной воде.
Примечание - раствор боргидрида натрия каждый раз использовали свежеприготовленным.
.2 Определение концентрации ионов Co2+ в растворе
.2.1 Комплексонометрическое титрование исходного раствора хлорида кобальта
С целью подтверждения концентрации приготовленного раствора хлорида кобальта
провели его комплексонометрическое титрование. Из раствора хлорида кобальта
концентрацией 0,1М отобрали аликвоту объемом 3 мл; добавили в нее 3 капли
индикатора (ксиленол оранжевый); добавили 1 каплю конц. HCl; добавляем постепенно 25-й раствор
уротропина до появления розовой окраски. Теперь полученный раствор с помощью
микробюретки титруем раствором ЭДТА до изменения окраски. Титрование повторили
3 раза, объем раствора ЭДТА ушедший на титрование во всех трех случаях занесен
в таблицу 2.
Таблица 2 - Объем раствора ЭДТА, ушедший на титрование
|
№ п/п |
Объем ЭДТА, мл |
|
1 |
6,02 |
|
2 |
6,02 |
|
3 |
6,04 |
Концентрацию ионов Co2+ определяли по формуле
 , (17)
, (17)
где
![]() - объем ЭДТА, ушедший на титрование, л;
- объем ЭДТА, ушедший на титрование, л;
![]() -
концентрация раствора ЭДТА, моль/л;
-
концентрация раствора ЭДТА, моль/л;
![]() - объем
аликвоты раствора хлорида кобальта, л.
- объем
аликвоты раствора хлорида кобальта, л.
Полученная концентрация кобальта с учетом среднеквадратической погрешности оказалась равной (0,100 ± 0,002) моль/л. Такой результат показывает, что полученный нами раствор кобальта обладает достаточной химической чистотой, а его концентрация получена достаточно точно.
.2.2 Спектрофотометрическое определение концентрации ионов Co2+
Концентрацию ионов кобальта до и после вымачивания мембран определяли спектрофотометрически по калибровочному графику, который показан на рисунке 13
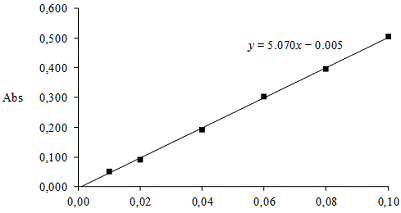
Рисунок 13 - Калибровачный график, полученный при спектрофотометрическом
исследовании исходных растворов известной концентрации
Калибровочный
график строили по интенсивности максимума полосы поглощения иона Co2+ (![]() нм) в
растворах приготовленных из исходного раствора хлорида кобальта известной
концентрации (0,1М) определенной методом комплексонометрического титрования,
описанного в пункте 2.2.1. Спетктрофотометрическое исследование проводили на
спектрофотометре Hitach U-2900 в диапазоне длин волн от
190 до 1 000 нм, при скорости сканирования 400 нм/мин. Уровень шума ± 0,00015Abs
(на длине волны 500 нм).
нм) в
растворах приготовленных из исходного раствора хлорида кобальта известной
концентрации (0,1М) определенной методом комплексонометрического титрования,
описанного в пункте 2.2.1. Спетктрофотометрическое исследование проводили на
спектрофотометре Hitach U-2900 в диапазоне длин волн от
190 до 1 000 нм, при скорости сканирования 400 нм/мин. Уровень шума ± 0,00015Abs
(на длине волны 500 нм).
Спектры
поглощения растворов хлорида кобальта до вымачивания полимерной матрицы
приведены на рисунке 14.
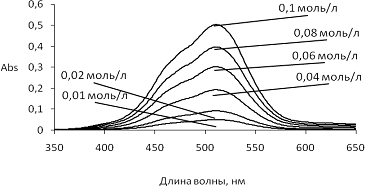
Рисунок 14 - Спектры поглощения растворов хлорида кобальта полученные на спектрофотометре до вымачивания полимера
Калибровочный график линейно аппроксимировали методом наименьших
квадратов. Уравнение прямой имеет вид
![]() . (18)
. (18)
Коэффициенты a и b определяли по формулам (19) и (20)
соответственно.
![]() , (19)
, (19)
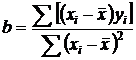 , (20)
, (20)
Полученное с помощью формулы (2) уравнение прямой имеет вид
![]() . (21)
. (21)
Таблица 3 - Результаты спектрофотометрического исследования. Концентрации растворов до и после вымачивания.
|
№ образца |
Вычисленная концентрация растворов |
|||
|
|
Abs до вымачивания |
Abs после вымачивания |
Концентрация Co2+ до вымачивания мембран, моль/л |
Концентрация Co2+ после вымачивания мембран, моль/л |
|
1 |
0,026 |
- |
0,005 |
- |
|
2 |
0,051 |
0,023 |
0,010 |
0,006 |
|
3 |
0,092 |
0,059 |
0,020 |
0,013 |
|
4 |
0,146 |
0,094 |
0,030 |
0,020 |
|
5 |
0,193 |
0,139 |
0,040 |
0,028 |
|
6 |
0,314 |
0,236 |
0,060 |
0,048 |
|
7 |
0,397 |
0,327 |
0,080 |
0,066 |
|
8 |
0,444 |
0,365 |
0,090 |
0,073 |
|
9 |
0,504 |
0,472 |
0,100 |
0,085 |
2.3 Определение константы ионного обмена полимерного материала
По вычисленным концентрациям растворов хлорида кобальта до и после
вымачивания полимеров определили количество вещества, которое может быть
имплантировано в полимер при данной концентрации. Количество вещества в
миллимолях, содержащееся в единице массы мембраны.
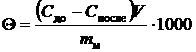 (22)
(22)
где
![]() - концентрация раствора до вымачивания полимера,
моль/л;
- концентрация раствора до вымачивания полимера,
моль/л;
![]() -
концентрация раствора после вымачивания полимера, моль/л;
-
концентрация раствора после вымачивания полимера, моль/л;
![]() - объем
раствора для вымачивания, л;
- объем
раствора для вымачивания, л; ![]() - масса
полимера, г.
- масса
полимера, г.
Рассчитанное по формуле (22) количество ионов кобальта, приходящееся на
единицу массы полимера после имплантации, приведены в таблице 4.
Таблица 4 - Количество вещества, приходящееся на единицу массы полимера после имплантации.
|
№ п/п |
Концентрация Co2+ до вымачивания мембран, моль/л |
Количество вещества в единице массы полимера, ммоль/г |
|
|
1 |
0,005 |
- |
0,005 |
|
2 |
0,010 |
0,006 |
0,010 |
|
3 |
0,020 |
0,013 |
0,020 |
|
4 |
0,030 |
0,020 |
0,030 |
|
5 |
0,040 |
0,028 |
0,040 |
|
6 |
0,060 |
0,048 |
0,060 |
|
7 |
0,080 |
0,066 |
0,080 |
|
8 |
0,090 |
0,073 |
0,090 |
|
9 |
0,100 |
0,085 |
0,100 |
2.4 Получение образцов нанокомпозитных полимерных материалов
В качестве полимерной матрицы, используемой модификации наночастицами кобальта, были выбраны ионообменные мембраны МФ-4СК предствляют собой листы толщиной около 300 мкм.
.4.1 Подготовка полимера
Для подготовки мембран их последовательно кипятили:
в 5%-м растворе азотной кислоты;
в 10%-м растворе перекиси водорода;
в дистиллированной воде;
в течение 1,5 часов в каждом.
Таким образом получали набухшие мембраны в H-форме. Для того чтобы перевести мембрану в Na-форму, полученные мембраны промывали в водном растворе хлорида натрия концентрацией 1,5 моль/л несколько раз.
.4.2 Имплантация ионов кобальта в структуру политетрафторэтилена
Введение ионов кобальта в ионообменную мембрану проводили путем
вымачивания образцов полимерного материла в водном растворе хлорида кобальта
различных концентраций. Мембраны массой 250 мг в набухшем состоянии помещали на
24 часа в смешанный раствор хлорида кобальта и хлорида натрия общим объемом 5
мл. Концентрации компонентов смешанных растворов, приготовленных для вымачивания,
приведены в таблице 5.
Таблица 5 - Концентрация компонентов раствора при вымачивании мембран
|
№ п/п |
Концентрация CoCl2·6H2O, моль/л |
Концентрация NaCl, моль/л |
|
1 |
0,005 |
0.095 |
|
2 |
0,010 |
0,090 |
|
3 |
0,020 |
0,080 |
|
4 |
0,030 |
0,070 |
|
5 |
0,040 |
0,060 |
|
6 |
0,060 |
0,040 |
|
7 |
0,080 |
0,020 |
|
8 |
0,090 |
0,010 |
|
9 |
0,100 |
0,000 |
Перед вымачиванием концентрации растворов определялись
спектрофотометрически по процедуре, описанной в пункте 2.2.2. Используемые
ионообменные мембраны были модифицированы сульфитной группой, к которой в
процессе подготовки мембран, описанной в пункте 2.4.1, присоединялись ионы Na+, поэтому во время вымачивания мембран ионы Na+, закрепленные на сульфогруппах, замещались на ионы Co2+ из раствора по реакции:
![]() (23)
(23)
.4.3 Восстановление имплантированных в политетрафторэтилен ионов кобальта
Мембраны после вымачивания в водном растворе CoCl2·6H2O готовы к восстановлению. Для
восстановления от исходных мембран массой 250 мг отрезали часть прямоугольной
формы и размером 1 см на 0,5 см. В качестве восстановителя использовался
боргидрид натрия NaBH4. Согласно данным [35] уравнение
реакции выглядит следующим образом
![]() . (24)
. (24)
Борид кобальта далее взаимодействует с кислородом, и в ходе реакции
образуется металлический кобальт
![]() . (25)
. (25)
Непосредственно перед проведением реакции готовили свежий раствор боргидрида натрия концентрацией 2 моль/л.
Мембраны после вымачивания перемещали в свежеприготовленный раствор восстановителя (приготовленный не более двух минут назад). Объем восстановителя для каждой мембраны специально не поддерживался постоянным и составлял от 20 до 30 мл. После помещения мембраны в восстановитель она сразу же меняла цвет с розового на черный, что свидетельствует об образовании металлического кобальта. Также во время реакции наблюдалось обильное выделение газа водорода с поверхности мембраны, при этом следили, чтобы выделяющийся газ не приводил к плаванию мембраны на поверхности раствора.
В этом случае мембрану специально утапливали стеклянной палочкой. Продолжительность проведения реакции всегда выдерживали 30 минут. После этого раствор NaBH4 сливали, и промывали мембраны дистиллированной водой до полного прекращения реакции на их поверхности. Затем мембраны помещали под пресс между двумя листами фильтровальной бумаги. Пресс нужен, для того чтобы не допустить сворачивания мембраны в процессе высушивания.
2.5 Исследование структурных и магнитных характеристик нанокомпохитных полимерных материалов
.5.1 Исследование структуры нанокомпозитных полимерных материалов методами РЭМ
Структурную упорядоченность полученных нанокомпозитных полимерных материалов изучали методами растровой электронной микроскопии (РЭМ). Для этого изоготовляли торцевой срез полимера. Для изготовления торцевого среза полимер вначале замораживали в жидком азоте, а потом аккуратно отламывали ножом необходимую часть. Исследование проводили на растровом электронном микроскопе JEOL JSM-7500F в режиме отраженных электронов (COMPO). Для каждого образца получали изображения торцевого среза с различным увеличением от 1 000 до 50 000 раз. На рисунке 15 приведено изображение образца нанокомпозитного материала в небольшом увеличении, который вымачивался в растворе хлорида кобальта концентрацией 0,1 моль/л.
На рисунке 16 показано изображение торцевого среза этого же образца при более высоком увеличении показаны на рисунке 2.4
Изображения торцевого среза других образцов, полученные на растровом
электронном микроскоепе, приведены в приложении А. По РЭМ изображениям
торцевого среза с большим увеличением можно определить распределение размеров
полученных наночастиц и представить их в виде гистограммы. К примеру,
полученное распределение наночастиц образца нанокомпозитного материала,
изображение торцевого среза которого представлено на рисунке 15, показано на
рисунке 17.

Рисунок 15 - Увеличенное в 1 000 раз изображение торцевого среза
полученного нанокомпозитного материала, который вымачивался в растворе
концентрацией 0,1 моль/л

Рисунок 16 - Увеличенное в 10 000 (а) и 30 000 раз изображение торцевого
среза полученного нанокомпозитного материала, который вымачивался в растворе
концентрацией 0,1 моль/л
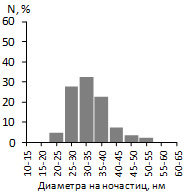
Рисунок 17 - Гистограмма распределения наночастиц по размерам в образце
нанокомпозитного полимерного материала, который вымачивался в растворе хлорида
кобальта концентрацией 0,1 моль/л
Определение глубины проникновения наночастиц проводили, используя РЭМ изображения образцов, измеряя расстояние между краем мембраны и границы, на которой перестают наблюдаться наночастицы. Измерения проводили в пяти различных точках и затем вычисляли среднее значение.
Так, например, на РЭМ изображении образца, который вымачивался в растворе
хлорида кобальта концентрацией 0,1 моль/л, показанном на рисунке 15, глубина
проникновения наночастиц измеренная в пяти различных точках равна 42,7 мкм.
Глубина проникновения, полученная таким способом для всех образцов полученных
нанокомпозитных полимеров представлена в таблице 6.