Материал: Иродов. т5 Квантовая физика Основные законы. 2014, 256с
160 |
Глава 6 |
|
|
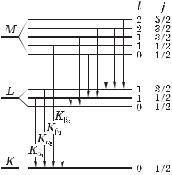
Тонкая структура рентгеновских спектров. Более детальный анализ характеристических спектров привел к уточнению структуры рентгеновских термов (рис. 6.9). K-терм остается одиночным. L-терм оказался тройным, М-терм — пятикратным.
Поясним причину расщепления.
Прежде всего отметим, что мы встречаемся здесь со случаем jj-связи, которая осуществляется в глубинных слоях тяжелых атомов.
УK-оболочки n 1, значит каждый электрон имеет l 0, s 1/2 и j 1/2 (это единственное значение).
УL-оболочки n 2, каждый электрон имеет l 0 или 1. При l 0 j 1/2, а при l 1 согласно (6.30) j 1/2 и 3/2. Итак, мы
имеем здесь три подуровня в точном соответствии с кратностью L-края полосы поглощения. А именно, при n 2 (L-оболочка)
l |
0 |
1 |
|
|
|
j |
1/2 |
1/2, 3/2 |
|
|
|
Аналогично для М-оболочки и т. д. (см. рис. 6.9).
Кроме того, необходимо учесть, что возможны только те переходы между термами, которые подчиняются правилу отбора:
l 11, j 0, 11. |
(6.44) |
Теперь должны быть понятными изображенные на рис. 6.9
переходы: только они удовлетво-
ряют этим правилам отбора. Мы
видим, что линии K-серии имеют
дублетную структуру. Компоненты дублетов обозначают индексами 1, 2; 71, 72 и т. д. Например,
K -линия представляет собой дуб-
лет K 1 и K 2.
Серия L и другие имеют более
сложную мультиплетную структуру.
Рис. 6.9

Квантование атомов |
161 |
|
|
Задачи
6.1.Атом водорода. Электрон атома водорода находится в стационарном состоянии, описываемом волновой функцией /(r) Ae– r, где А и — некоторые постоянные. Найти энергию E электрона и постоянную .
Р е ш е н и е. В данном случае уравнение Шредингера (6.4) будет иметь вид
2 / |
|
2 / |
|
2m |
( E U )/ 0. |
(1) |
||
r 2 |
r |
r |
2 |
|||||
|
|
|
|
|||||
Вычислив первую и вторую производные /-функции по r, подставим их выражения в (1) и сгруппируем следующим образом:
|
|
|
2mE |
|
2me2 |
|
1 |
|
|
||
|
2 |
|
|
|
|
|
|
|
|
0. |
(2) |
|
|
|
|
||||||||
|
|
|
2 |
|
|
2 |
|
|
|
|
|
|
|
|
|
|
r |
|
|
||||
Из этого соотношения видно, что равенство его нулю при любых значениях r возможно лишь в том случае, когда обе скобки по отдельности равны нулю. Отсюда
E |
2 |
2 |
|
me |
2 |
|
|
, |
|
|
. |
||
|
2 |
|
||||
|
2m |
|
|
|
||
|
|
|
|
|
||
6.2.Найти средний электростатический потенциал 0, создаваемый электроном в центре атома водорода, если электрон находится в основном состоянии, описываемом нормированной /-функцией
/(r) Aexp(–r/r1), где A 1/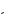
 r13 , r1 — первый боровский радиус.
r13 , r1 — первый боровский радиус.
Р е ш е н и е. Заряд электрона в 1s-состоянии — это заряд сфери- чески-симметричного электронного облака, плотность которого ( –e 2 r). Выделим мысленно тонкий сферический слой с радиусами r и r dr. Полный заряд этого слоя dq ( Δr2dr создает в центре атома потенциал d dq/r. Проинтегрировав это выражение по r от 0 до , найдем:
(
0 d 0 r 4 r 2 dr.
Приведя последний интеграл к табличному виду, получим
|
|
e |
|
e |
|
|
0 |
|
e x x dx |
. |
|||
|
|
|||||
|
r |
0 |
r |
|||
|
1 |
1 |
|
|||
162 |
Глава 6 |
|
|
Этот интеграл берется по частям или прямо из таблиц, он равен единице.
6.3.Найти наиболее вероятное расстояние электрона от ядра атома водорода в состоянии 2p.
Р е ш е н и е. В этом состоянии электронное облако не является сферически-симметричным. Согласно формуле (6.12)
/ R(r) Y( , ).
Найдем сначала вероятность местонахождения электрона в элементе объема dV вблизи некоторой точки пространства r, , :
dP /2dV AR2(r)Y2( , )r2drd , |
(1) |
где объем dV dS dr (рис. 6.10). Поскольку d dS/r2, то dV r2d dr.
Теперь найдем вероятность пребывания элект-
рона в сферическом слое с радиусами r и r dr. Для этого надо проинтегрировать (1) по телесно-
му углу d :
Рис. 6.10
dP AR2(r)r2dr Y ( , )d . |
(2) |
Интеграл в (2) не зависит от r, это некоторое число. Значит, можно записать, что
dP BR2(r)r2dr |
(3) |
и плотность вероятности в расчете на единицу толщины слоя:
dP/dr Br2R2(r), |
(4) |
где В — некоторая постоянная. Теперь введем вместо r новую переменную ( r/r1 и согласно табл. 6.1 перепишем R(() в явном виде. В результате (4) примет вид
dP/dr T (2R2(() (4e–(. |
(5) |
Функция f(() (4e–( имеет максимум. Найдем значение ( при котором он будет наблюдаться. Для этого продифференцируем f(() по ( и полученный результат приравняем к нулю. В результате получим
(вер 4.
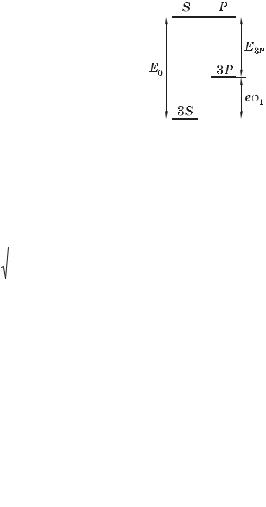
Квантование атомов |
163 |
|
|
Так как ( — это расстояние r в единицах r1, то найденное значение (вер соответствует второму боровскому радиусу согласно (2.23).
6.4.Атомы щелочных металлов. Найти ридберговскую поправку 3P-терма атома Na, первый потенциал возбуждения которого
1 2,10 В, а энергия связи валентного электрона в основном 3S-состоянии E0 5,14 эВ.
Р е ш е н и е. Воспользуемся формулой (6.19), которая содержит интересующую нас поправку. В этой формуле левую часть (энергию 3P-состояния) можно представить согласно рис. 6.11 как
E3P – (E0 – e 1) – (5,14 – 2,10) эВ
(имея в виду, что энергия уровня равна с об- |
Рис. 6.11 |
|||||||||
ратным знаком энергии связи на этом уров- |
||||||||||
|
||||||||||
не). Таким образом, формула (6.19) примет вид |
|
|||||||||
E0 |
– e 1 |
|
|
|
|
R |
, |
|
||
|
|
|
#p )2 |
|
||||||
|
|
|
(3 |
|
|
|||||
откуда |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
#p |
R |
|
|
|
3 0,88 . |
|
||||
|
|
|
|
|
||||||
|
|
E0 e 1 |
|
|
|
|||||
6.5.Найти энергию связи валентного электрона в основном состоянии атома лития, если известно, что длины волн головной линии резкой серии и ее коротковолновой границы равны соответственно1 813 нм и K 350 нм.
Р е ш е н и е. Согласно (6.19) энергия связи электрона в 2s-состоя- нии равна
Eсв |
|
E2 s |
|
|
R |
|
|
|
|
|
. |
(1) |
|||
|
|
(2 # )2 |
|||||
|
|
|
|||||
|
|
|
|
|
s |
|
|
Задача сводится к нахождению поправки #s. Воспользовавшись рис. 6.3 и формулой (6.19), запишем разность энергий
|
K |
|
|
1 |
R |
|
|
|
|
(3 # )2 . |
(2) |
||||
|
|
|
|
|
s |
|
|

164 |
|
|
|
|
|
|
|
|
|
|
Глава 6 |
|
|||||||||||
Имея в виду, что 2 c/ , перепишем (2) так: |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
#s |
|
|
R 1 K |
|
3. |
(3) |
|||
|
|
|
2 c( 1 K ) |
|
|||||||
|
|
|
|
|
|
|
|
|
|||
Остается подставить (3) в (1), и мы получим: |
|||||||||||
Eжв |
|
|
|
|
|
R |
|
|
5,3 |
эВ, |
|
|
|
|
|
|
|
1 2 |
|||||
|
R |
K |
/2 c |
|
|||||||
|
|
1 |
|
|
|
|
|
|
|||
где 1 – K .
6.6.Момент импульса. Найти максимально возможный полный механический момент и соответствующий спектральный символ терма атома в состоянии с электронной конфигурацией 1s2 2p 3d.
Р е ш е н и е. Максимальный момент будет складываться из максимальных орбитального и спинового моментов. Это относится и к соответствующим квантовым числам:
Lмакс 1 2 3, Sмакс 1/2 1/2 1.
В результате получим:
J |
макс |
3 1 4, M |
макс |
|
20 |
, |
3F . |
|
|
|
|
|
4 |
6.7.Определить спектральный символ терма атома, мультиплетность которого равна пяти, кратность вырождения по квантовому числу J — семи и значение орбитального квантового числа равно максимально возможному в этих условиях.
Р е ш е н и е. Из мультиплетности 2S 1 находим S 2, а из
кратности вырождения (2J 1) имеем J 3. Далее, мы знаем, что вообще говоря, если известны L и S, то квантовое число J в формуле (6.38) может принимать значения (через единицу) от L S до |L – S|. Отсюда видно, что значениям J 3 , S 2 и требованию, чтобы L было максимальным, отвечает условие
J L – S, откуда L J S 5.
Спектральный символ этого состояния 5H3.
6.8.Написать спектральный символ терма, кратность вырождения которого по J равна семи, и квантовые числа L и S связаны соотношением L 3S.