Материал: Иродов. т5 Квантовая физика Основные законы. 2014, 256с

Квантование атомов |
155 |
|
|
Правила Хунда. Это полуэмпирические правила, относящиеся к системе эквивалентных электронов (у них n и l одинаковы), т. е. для электронов, находящихся в одной подоболочке. Этих правил два:
1.Минимальной энергией данной электронной конфигурации обладает терм с наибольшим возможным значением спина S и с наибольшим возможным при таком S значении L.
2.При этом квантовое число
4 |
|
L S |
|
, если подоболочка заполнена менее, чем наполовину, |
|
|
|||
J 5 |
|
|
|
в остальных случаях. |
|
|
|
||
6 L S |
|
|||
Применим эти правила к p-оболочке. В ней всего могут находиться 2(2l 1) 6 электронов. Возьмем, например, атом кислорода O (у него электронная конфигурация, как видно из табл. 6.7, имеет вид 1s22s2p4), т. е. р-подоболочка заполнена не полностью. Изобразим состояние с различными значениями ml. Для р-подоболочки это будут 1/2, 0 и –1/2, т. е. три ячейки:
ml |
1/2 |
0 |
–1/2 |
|
|
|
|
ms |
ΒΧ |
Β |
Β |
Затем будем заполнять эти состояния (ячейки) электронами. У каждого электрона ms 1/2 или –1/2. Ддя наглядности эти значения ms будем, как и раньше, изображать стрелками Β и Χ соответственно.
Начнем с заполнения ячеек спинами Β (таких в каждой ячейке может быть не более одного согласно принципу Паули). Оставшийся четвертый электрон со спином Χ надо поместить в такую ячейку, ml которой максимально. Этим самым мы обеспечиваем максимальные значения mS и mL:
mS : ms 1, mL : ml 1.
Но максимальные значения mS и mL равны S и L, т. е. S 1 и L = 1.
В данном случае подоболочка заполнена более, чем наполовину, поэтому согласно второму правилу Хунда
J L S 2.
156 Глава 6
Таким образом, основной терм данной конфигурации это 3P2. Вернемся к атому бора В. У него в незаполненной р-подобо-
лочке только один электрон. Легко сообразить, что в этом случае максимальные значения mS 1/2 и mL 1, а значит, L = 1 и S 1/2. Подоболочка заполнена менее, чем наполовину, поэтому J |L – S| 1/2. И мы приходим к тому, что основным термом является 2P1/2.
Полезно убедиться самостоятельно (с помощью правил Хунда) в справедливости распределения р-электронов по ячейкам ml для конфигураций р2, р3 и р5, приведенных в нижеследующих табличках, и соответствующего каждому из них основного терма:
1) p2 |
ml |
+1 |
0 |
–1 |
3P0; |
2) p3 |
ml |
+1 |
0 |
–1 |
4 S1 2 ; |
3) p5 |
ml |
+1 |
0 |
–1 |
2 P3 2 ; |
ms |
Β |
Β |
|
ms |
Β |
Β |
Β |
ms |
ΒΧ |
ΒΧ |
Β |
||||||
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рассмотрим в качестве примера обратную задачу.
Пример. Найдем с помощью правил Хунда число электронов в единственной незаполненной подоболочке атома, основной терм которого 3F2.
Символ F означает, что L 3. Спиновое число находим из мультиплетности: 3 2S 1, откуда S 1. Поскольку J 2, то оно может быть представлено только как J L – S, а это значит, согласно второму правилу Хунда, что подоболочка d (ей отвечает L 3) заполнена менее, чем наполовину, и только таким способом:
ml 2 1 0 –1 –2
ms Β Β
Ей соответствует электронная конфигурация d2. Например, атом титана Ti (1s22s2p63s2p6d24s).
§ 6.7. Характеристические рентгеновские спектры
Рентгеновские спектры, возникающие при бомбардировке электронами антикатода рентгеновской трубки, бывают двух видов: сплошные и линейчатые. Сплошные спектры возникают при торможении быстрых электронов в веществе антикатода и явля-
Квантование атомов |
157 |
|
|
ются обычным тормозным излучением электронов (см. § 1.2). Вид этих спектров не зависит от материала антикатода.
При повышении напряжения на трубке наряду со сплошным спектром появляется линейчатый. Он состоит из отдельных линий и зависит от материала антикатода. Каждый элемент обладает своим, характерным для него линейчатым спектром. Поэтому такие спектры называют характеристическими.
С увеличением напряжения на рентгеновской трубке коротковолновая граница сплошного спектра смещается (см. § 1.2), линии же характеристического спектра становятся лишь более интенсивными, не меняя своего расположения.
Особенности характеристических спектров.
1.В отличие от оптических линейчатых спектров с их сложностью и разнообразием, рентгеновские характеристические спектры различных элементов отличаются простотой и однообразием. С ростом атомного номера Z элемента они монотонно смещаются в коротковолновую сторону.
2.Характеристические спектры разных элементов имеют сходный характер (однотипны) и не меняются, если интересующий нас элемент находится в соединении с другими. Это можно объяснить лишь тем, что характеристические спектры возникают при переходах электронов во внутренних частях атома, частях, имеющих сходное строение.
3. Характеристические спект- |
|
|
|
|
|
|
|
|
|
|
||||
ры состоят из нескольких серий: |
|
|
|
|
|
|
|
|
|
|
||||
K, L, М, ... Каждая серия — из |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|||||
небольшого числа линий: K , K , |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|||||
K , ... L , L , L , ... и т. д. в по- |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|||||
рядке убывания длины волны . |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|||||
Анализ |
характеристических |
|
|
|
|
|
|
|
|
|
|
|||
спектров |
привел к пониманию, |
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
что атомам присуща система |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|||
рентгеновских термов K, L, М, ... |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
||||
(рис. 6.7). На этом же рисунке по- |
|
|
|
|
|
|
|
|
|
|
||||
казана схема возникновения ха- |
|
|
|
|
|
|
|
|
|
|
||||
рактеристических спектров. Воз- |
|
|
|
|
|
|
|
|
|
|
||||
буждение |
атома возникает при |
|
|
|
Рис. 6.7 |
|
||||||||

158 |
Глава 6 |
|
|
удалении одного из внутренних электронов (под действием электронов или фотонов достаточно большой энергии). Если вырывается один из двух электронов K-уровня (n 1), то освободившееся место может быть занято электроном из какого-либо более высокого уровня: L, М, N, и т. д. В результате возникает K-серия. Подобным же образом возникают и другие серии: L, М, ...
Серия K, как видно из рис. 6.7, непременно сопровождается появлением и остальных серий, поскольку при испускании ее линий освобождаются электроны на уровнях L, М и др., которые в свою очередь будут заполняться электронами с более высоких уровней.
Закон Мозли. Мозли (1913) экспериментально установил закон, согласно которому частота K -линий зависит от атомного номера Z элемента как
|
3 |
R(Z #)2 , |
(6.43) |
K |
4 |
|
|
где R — постоянная Ридберга (2,07 1016 с–1), # — постоянная, практически равная единице (# % 1) для легких элементов. Этот закон сыграл в свое время важную роль при уточнении расположения элементов в периодической системе.
Пример. Вычислим разность E энергий связи K- и L-электронов ванадия (Z 23).
Достаточно обратиться к рис. 6.7, и мы увидим, что искомая разность энергий связи равна просто энергии перехода между L- и K-уровнями, которая связана с частотой K -линии, т. е. с законом Мозли. Таким образом,
E K 34 R( Z 1)2 5 кэВ.
Закон Мозли достаточно точно выполняется для легких элементов. Для тяжелых же элементов поправка # значительно отличается от единицы; например, для олова (0,29), цезия (0,00) и вольфрама (–2,1).
С одной стороны ясно, что частоты, фигурирующие в законе Mозли, обусловлены переходами между соответствующими рентгеновскими термами. С другой стороны, попытки представить значение как разность термов вида Т R(Z – #)2/n2 следует признать неудачными: уж очень сильно отличаются поправки

Квантование атомов |
159 |
|
|
# для разных термов. В чем здесь дело — это предстоит еще выяснить, но сконструировать закон Мозли (6.43) с помощью такого вида термов не удается.
Особенности спектра поглощения. Коэффициент поглощения вещества при прохождении через него рентгеновского излучения вообще возрастает с увели- 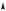
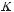
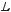 чением длины волны. Однако при
чением длины волны. Однако при 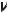
 некотором значении K он резко па-
некотором значении K он резко па- 
дает, а затем начинает снова плавно возрастать (рис. 6.8, где показаны и
линии испускания). Такая особенность поглощения
веществом рентгеновского излучения объясняется довольно просто.
Пусть длина волны рентгеновского излучения настолько мала, что возбуждается K-уровень, а значит и все остальные. За счет этого интенсивность проходящего через вещество пучка будет уменьшаться. При увеличении длины волны, начиная с некоторого значения K, энергии рентгеновского кванта становится уже недостаточно, чтобы возбудить K-уровень. В результате поглощение резко уменьшается. Появляется так называемый K-край полосы поглощения. При дальнейшем увеличении длины волны на кривой поглощения появляется новый, L-край поглощения, состоящий из трех «зубцов»: LI, LII, LIII (см. рис. 6.8). Дальнейшее увеличение длины волны сопровождается появлением М-края полосы поглощения, состоящего из пяти зубцов, и т. д. Заметим, что для легких элементов зубцы расположены очень тесно, и при расчетах часто их характеризуют одной длиной волны L или M.
Итак, например, K-край полосы поглощения ( K) связан с прекращением возбуждения K-уровня. Это значит, что длина
волны K характеризует энергию |
связи |
K-электрона (EK): |
||||
EK K |
|
2 c |
|
1,24 |
|
кэВ. |
|
|
|
||||
|
|
K |
K (нм) |
|||
Значения длин волн, соответствующих K- и L-краям поглощения для разных элементов, определены экспериментально и представлены в виде специальных таблиц.