Материал: Иродов. т5 Квантовая физика Основные законы. 2014, 256с
Квантование атомов |
145 |
|
|
Итак, каждый ряд уровней, кроме S-ряда, имеет дублетную структуру. Уровни (термы) принято обозначать символом, определяющим значения квантовых чисел l, s и j, т. е. по существу полностью «структуру» углового момента электрона. Символически это записывают так:
n (L) j , |
(6.31) |
где L — символ состояния, определяемого квантовым числом l — в соответствии с (6.10), только большими латинскими буквами: S, P, D и т. д.; n — так называемая мультиплетность, она связана со спином: n 2s 1.
Выпишем несколько первых рядов термов атома щелочных металлов:
2S1/2; 2P1/2,2P3/2; 2D3/2,2D5/2; ... |
(6.32) |
Для атомов щелочных металлов дублетное расщепление очень мало (по сравнению с расстояниями между «основными» уровнями).
Величина тонкого расщепления уровней для легких атомов не более 10–5 эВ. Для тяжелых же может достигать десятых долей эВ (это уже трудно назвать тонким расщеплением). Для сравнения приведем разность между двумя уровнями на рис. 6.3, которая равна 2 эВ.
Правила отбора для j. Для квантового числа j действует правило отбора, согласно которому возможны только те переходы между уровнями, при которых
j 0, 1 1. |
(6.33) |
|
|
Тонкая структура спектральных линий была обнаружена экспериментально и у атома водорода. Но расщепление уровней атома водорода оказалось слишком мало. и поэтому чаще всего им просто пренебрегают (за исключением очень тонких исследований).
Закономерности тонкой структуры. Поясним происхождение тонкой структуры спектральных линий, например, лития, в трех случаях.
146 |
Глава 6 |
|
|
|
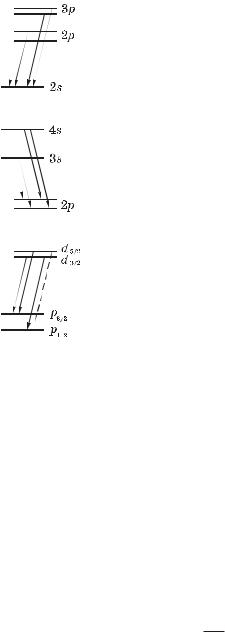
Главная серия. В результате переходов с близко |
|
отстоящих друг от друга подуровней p-термов на |
|
один и тот же уровень 2s возникают две близко |
|
расположенные линии, т. е. дублет (рис. 6.4). Рас- |
|
щепление различных p-термов различно, отсюда и |
|
наблюдаемое различие расщепления соответствую- |
Рис. 6.4 |
щих дублетов. |
|
Резкая серия. Переходы с s-уровней на 2p-уро- |
|
вень (рис. 6.5) приводит к одному и тому же рас- |
|
щеплению линий этой серии, поскольку у всех ли- |
|
ний оно обусловлено расщеплением одного и того |
|
же уровня 2p. |
|
Диффузная серия. Вследствие переходов с |
Рис. 6.5 |
d-уровней на 2p-уровень (рис. 6.6) — спектральные |
|
линии оказываются триплетами, так как перехо- |
|
ды, в которых квантовое число j меняется на 2, за- |
|
прещено правилом отбора (6.33). Таковым являет- |
|
ся переход d5/2 – 2p1/2, изображенный пунктиром. |
|
Расщепление d-уровней значительно меньше рас- |
|
щепления 2p-уровня. Поэтому компоненты трипле- |
|
та не всегда разрешаются, а сами линии получают- |
Рис. 6.6 |
ся размытыми (отсюда и название серии). |
|
Таким образом, тонкая структура уровней и спектральных линий атомов щелочных металлов обусловлены спином электрона, или, что то же, спин-орбитальным взаимодействием.
В заключение рассмотрим пример, с решением которого нередко возникают затруднения.
Пример. У атомов некоторого щелочного металла головная линия резкой серии с длиной волны представляет собой дублет, разность длин волн которого . Найдем величину расщепления в частотах следующих линий этой серии.
Поскольку все линии резкой серии обусловлены переходом с синглетных s-уровней на один и тот же расщепленный нижний p-уровень, то разность энергий переходов будет одинакова в каждом дублете. Значит одинаковым будет и расщепление . В нашем случае I , поэтому, учитывая связь
2 c/ , можно записать:
2 c .2

Квантование атомов |
147 |
|
|
§ 6.4. Механический момент многоэлектронного атома
Сложение угловых моментов. Как показывает расчет (который мы опускаем), суммарный орбитальный момент системы определяется выражением
ML |
|
, |
|
L (L 1) |
(6.34) |
||
|
|
|
|
где L — орбитальное квантовое число результирующего момента. В случае системы из двух частиц с орбитальными моментами l1 и l2 квантовое число L — целое, положительное — может иметь следующие значения:
L (l1 l2), (l1 l2 – 1), …, |l1 – l2| . |
(6.35) |
Отсюда следует, что L (а значит и результирующий момент) может иметь 2l1 1 или 2l2 1 различных значений (нужно взять меньшее из двух значений l). Это легко проверить; например, для l1 2 l2 3 получаем 2 2 1 5 разных значений L: 5, 4, 3, 2, 1.
Если система состоит не из двух, а из многих частиц, то квантовое число L, определяющее результирующий орбитальный момент, находится путем последовательного применения правила (6.35), но мы не будем на этом останавливаться, поскольку в дальнейшем это не понадобится.
Проекция результирующего орбитального момента на неко-
торое направление Z определяется аналогично |
(6.28): |
|
Mz m L , m L 0, 1 1, 1 2, ..., 1 |
L. |
(6.36) |
Подобным же образом определяется и суммарный спиновый
момент системы: |
|
MS S (S 1) , |
(6.37) |
где квантовое число S результирующего спинового момента может быть целым или полуцелым — в зависимости от числа частиц — четного или нечетного. Если число N частиц четное, то S Ns, Ns – 1, ..., 0, где s 1/2, т. е. в этом случае S — целые числа. Например, при N 4 число S может быть равно 2, 1, 0.
148 |
Глава 6 |
|
|
Если же число N частиц нечетное, то S принимает все полуцелые значения от Ns до s, где s 1/2. Например, при N 5 возможные значения S равны 5/2, 3/2 и 1/2.
Типы связи. В многоэлектронном атоме каждый электрон можно характеризовать орбитальным и спиновым моментами. Возникает естественный вопрос: чему равен полный механический момент атома? Ответ на этот вопрос зависит от того, какие моменты взаимодействуют друг с другом сильнее: орбитальные, спиновые или спин-орбитальные.
Оказывается, наиболее важной и распространенной является так называемая нормальная связь, или связь Рессель-Саун- дерса. Эта связь заключается в том, что орбитальные моменты электронов взаимодействуют между собой сильнее, чем со спиновыми моментами. Аналогично ведут себя и спиновые моменты. Вследствие этого все орбитальные моменты складываются в результирующий орбитальный момент ML, а спиновые — в результирующий спиновый момент MS. А затем взаимодействие ML и MS определяет суммарный момент MJ атома:
MJ |
|
, |
|
J(J 1) |
(6.38) |
где квантовое число J полного момента может иметь одно из следующих значений:
J L S, L S – 1, …, |L – S| .
Значит, J будет целым, если S целое ( т. е. при четном числе электронов) или полуцелым, если S полуцелое (при нечетном числе электронов). Так например,
LS Возможные значения J
2 |
1 |
3, 2, 1 |
23/2 7/2, 5/2, 3/2, 1/2
Такой вид связи, как правило, присущ легким и не слишком тяжелым атомам.
Однако нормальная связь является не единственно возможной. Это только один из крайних случаев связи. Другой край-
Квантование атомов |
149 |
|
|
ний случай — так называемая j–j связь, когда спин-орбиталь- ное взаимодействие у каждого электрона оказывается основным. В этом случае суммарный момент атома MJ :Mj , т. е. равен сумме отдельных спин-орбитальных моментов Mj.
Такая связь встречается у тяжелых атомов, но достаточно редко. В основном же осуществляются более сложные промежуточные виды связи. Но мы их затрагивать не будем, ограничившись в основном только нормальной связью, наиболее важной и чаще встречающейся.
Спектральные обозначения. В случае нормальной связи термы принято обозначать символами, подобными (6.31):
n (L) J , |
(6.39) |
где n 2S 1 — мультиплетность, J — квантовое число полного момента. Отличие с обозначением (6.31) лишь в том, что малые буквы s и j заменены на соответствующие большие S и J.
Приведем примеры термов систем с двумя электронами. Здесь возможны два случая: S 0 (спины электронов противоположны) и S 1 (спины сонаправлены).
В первом случае J L и 2S 1 1, т. е. все термы — синглеты. Во втором случае 2S 1 3, т. е. все три терма — триплеты. Причем во втором случае возможны три значения J: L 1, L и |L – 1|. Сказанное сведено для наглядности в таблицы 6.4 и 6.5.
Таблица 6.4 |
Таблица 6.5 |
S |
L |
J |
Синглеты |
|
|
|
|
0 |
0 |
0 |
1S0 |
0 |
1 |
1 |
1P |
|
|
|
1 |
0 |
2 |
2 |
1D |
|
|
|
2 |
|
|
|
|
S |
L |
J |
Триплеты |
||
|
|
|
|
|
|
1 |
0 |
1, 0 |
3S |
3S |
0 |
|
|
|
1 |
||
1 |
1 |
2, 1, 0 |
3P |
3P |
3P |
|
|
|
2 |
1 |
0 |
1 |
2 |
3, 2, 1 |
3D |
3D |
3D |
|
|
|
3 |
2 |
1 |
|
|
|
|
|
|
Следует отметить, что мультиплетность n дает количество подуровней только в случае S < L (в случае же S > L, число подуровней равно 2L 1).
Правила отбора. При рассмотрении внешнего электрона в атомаx щелочных металлов было отмечено, что не все переходы