Материал: Иродов. т5 Квантовая физика Основные законы. 2014, 256с
140 |
Глава 6 |
|
|
E электрона не только от n, но и от l. Иными словами, в данном случае вырождение по l снимается.
Исследование спектров ионов щелочных металлов показало, что момент импульса атомного остова (т. е. ядра и Z – 1 электронов) равен нулю. Следовательно, орбитальный момент атома щелочного металла оказывается равным моменту его внешнего электрона и определяется квантовым числом l (что и показано на рис. 6.3).
Правило отбора. Излучение (и поглощение) происходит в результате перехода внешнего электрона с одного уровня на другой. Однако не все переходы возможны. Возможны лишь те, при которых орбитальное квантовое число l внешнего электрона меняется на единицу:
l 11. |
(6.21) |
|
|
Это означает, что разрешенными являются переходы лишь между s- и p-состояниями, между p- и d-состояниями и т. д. (см. рис. 6.3). Заметим еще, что главное квантовое число n может изменяться на любое целое число.
Пример. Определим, сколько спектральных линий будет испускать источник, состоящий из атомов лития, которые постоянно возбуждают на уровень 4s.
Согласно правилу отбора (6.21) таких переходов будет шесть (см. рис. 6.3), это:
4s&3 p, 4s&2 p, 3 p&3s, 3 p&2s, 3s&2 p, 2 p&2s.
С точки зрения квантовой теории правила отбора связаны с вероятностью перехода из одного квантового состояния в другое. Оказывается, вероятность переходов, не разрешенных правилами отбора, практически равна нулю.
Спектральные серии. С учетом правила отбора (6.21) легко понять, что в спектрах атомов лития наблюдаются следующие серии:
главная: |
2s np, |
n 2, 3, 4, … |
|
резкая: |
2 p ns, |
n 3, 4, 5, … |
(6.22) |
диффузная: |
2 p nd, |
n 3, 4, 5, … |
|

Квантование атомов |
141 |
|
|
Здесь — частота испускаемой линии. Спектральная линия главной серии, соответствующая переходу 2s – 2p, является самой интенсивной. Эту линию называют резонансной.
Серии (6.22) записаны в символической форме. В явном виде их записывают как разности, двух соответствующих термов. Например, для главной серии лития:
|
R |
|
R |
, n 2, 3, 4, … |
(6.23) |
(2 #s )2 |
(n #p )2 |
Аналогично и для других серий. Заметим, что ридберговские поправки в пределах каждой серии практически постоянные, но меняются от серии к серии.
Тонкая структура спектральных линий. Исследование спектральных линий атомов щелочных металлов приборами с большой разрешающей способностью обнаружило, что эти линии являются двойными (дублетами), т. е. образуют тонкую структуру.
Спектральные линии, состоящие из нескольких компонент, называют мультиплетами. Число компонент в мультиплете различных атомов может быть равно двум (дублеты), трем (триплеты), четырем (квартеты) и т. д. В частности, спектральные линии могут быть и одиночными (синглеты).
Тонкая структура, т. е. расщепление спектральных линий, очевидно, вызвана расщеплением самих энергетических уровней (термов). Вместе с тем, это никак не следует из решения уравнения Шредингера. В чем же причина такого загадочного расщепления? Ответ на этот вопрос — в следующем параграфе.
§ 6.3. Спин электрона
Гипотеза спина. Тонкая структура спектральных линий, т. е. их расщепление, как было сказано в конце предыдущего параграфа, является следствием расщепления самих энергетических уровней. Это был первый экспериментальный факт, побудивший Гаудсмита и Уленбека (1925) выдвинуть гипотезу о наличии у электрона собственного момента, названного спином. В дальнейшем эта гипотеза была подтверждена и рядом других весьма убедительных экспериментальных фактов.

142 |
Глава 6 |
|
|
Гипотеза спина сразу открыла возможность простого объяснения большого числа экспериментальных фактов, некоторые из которых мы рассмотрим далее.
Спин — существенно квантовая величина, не имеющая классического аналога. Он ничего общего не имеет с представлением о вращающейся частице, как первоначально предполагали (отсюда и название).
Спин характеризует внутреннее свойство электрона подобно массе и заряду. Выяснилось, что спин является свойством одновременно квантовым и релятивистским*. В отличие от орбитального момента, спин всегда сохраняется (как внутреннее свойство).
Спин электрона определяется по общим законам квантовой теории. Аналогично орбитальному моменту, определенные значения в одном и том же состоянии могут иметь квадрат спина M 2s (а значит и модуль спина Ms) и одна из его проекций Msz на произвольно выбранную ось Z:
Ms |
s (s 1) |
, s 1/2, |
(6.24) |
где s — спиновое квантовое число, и |
|
||
Msz hms, ms 1s 1/2 и –1/2. |
(6.25) |
||
Значение s 1/2 получено из следующих соображений. Аналогично орбитальному моменту число возможных значений проекции ms, соответствующих данному значению s, равно 2s 1. Экспериментально было установлено, что это число для электрона равно двум, т. е. 2s 1 2, откуда s 1/2.
Отметим, что спином обладает подавляющее большинство частиц. Например, у протона и нейтрона s 1/2, а у фотона s 1.
Поскольку спин электрона s 1/2, а его проекции ms равны 1/2 и –1/2, то становится понятным, почему кратность вырождения n-го энергетического уровня атома водорода равна не n2, а 2n2. Впрочем, это скорее кратность вырождения не n-го уровня, а суммарная кратность вырождения двух подуровней, соответствующих квантовому числу n.
*Дирак (1928) показал, что спин электрона автоматически содержится в его теории электрона, основанной на релятивистском волновом уравнении.

Квантование атомов |
143 |
|
|
Полный момент импульса электрона. С механическими моментами (орбитальным и спиновым) связаны магнитные моменты. В результате их взаимодействия происходит сложение моментов — возникает полный момент импульса электрона. Символически это записывают так: Mj Ml Ms, где j — квантовое число полного момента.
Правила сложения угловых моментов в квантовой теории не зависят от того, являются ли моменты орбитальными или спиновыми. Поэтому полный момент электрона Mj определяется формулой, аналогичной формулам для орбитального и спинового моментов, а именно
Mj |
j (j 1) |
, j l s l 1 1 2. |
(6.26) |
Таким образом, квантовое число j является полуцелым, поскольку l — целое, причем, если l 0, то j s = 1/2. Кроме того, j всегда положительно.
В связи со знаками 1 перед спином s в (6.26) условно принято говорить, что спиновый момент либо «сонаправлен» с орбитальным моментом (знак ), либо они взаимно противоположны «по направлению» (знак –).
Возможные проекции момента (6.26) на ось Z определяются как
Mjz hmj, mj j, j – 1, j – 2, …, –j, |
(6.27) |
т. е. при данном j возможны 2j 1 квантовых состояний, отличающихся значениями mj. Например, при l 1
j1 1 1/2 3/2, |
mj 3/2, |
1/2, –1/2, –3/2, |
j2 1 – 1/2 1/2, |
mj 1/2, |
–1/2. |
Если же l 0, то весь момент импульса чисто спиновый.
Общие результаты. Выпишем собственные значения угловых моментов (орбитального, спинового и полного) и их проекций на ось Z в одной таблице (табл. 6.3), чтобы обратить внимание на их однотипность и облегчить запоминание.

144 |
Глава 6 |
|
|
|
|
|
|
|
|
|
|
Таблица 6.3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
l 0, 1, 2, . . . |
M l |
l (l 1), |
|||||||
M lz ml , |
ml 0, 1 1, 1 2, . . . , 1 l. |
|||||||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
s 1 2 , |
|
M s |
|
s( s 1), |
||||||
M sz ms , |
ms 1 2, 1 2. |
|||||||
|
|
|
|
|||||
|
|
|
|
|
|
j l 1 s l 1 1 2, |
||
M j |
j( j 1), |
|||||||
M jz mj , |
mj j, j 1, . . . , j. |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(6.28)
(6.29)
(6.30)
В дальнейшем на эти формулы мы будем неоднократно ссылаться.
Тонкая структура. Рассмотрим на примере атома лития, как с помощью спина можно объяснить дублетную структуру линий спектра. Вследствие того, что момент атомного остова равен нулю (см. стр. 140), момент атома лития равен моменту внешнего (валентного) электрона. Момент же этого электрона равен сумме орбитального момента и спинового. Полный момент данного электрона согласно (6.30) определяется квантовым числом j:
j l 1 1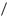 2,
2,
где l и 1/2 — орбитальное и спиновое квантовые числа. Причем, в случае l 0 квантовое число j имеет только одно значение: j 1/2.
Мы уже знаем, что моменты Ml и Ms взаимодействуют друг с другом. Энергия этого взаимодействия зависит от взаимной «ориентации» орбитального и спинового моментов, что и приводит к расщеплению энергетических уровней.
Таким образом, каждый уровень (терм) ряда P (l 1) расщепляется на два подуровня с j 1/2 и 3/2, каждый уровень ряда D (l 2) — на подуровни с j 3/2 и 5/2 и т. д. Исключение составляют уровни ряда S (l 0), которым соответствует только одно значение j 1/2; поэтому уровни этого ряда не расщепляются (остаются синглетными).