Материал: Иродов. т5 Квантовая физика Основные законы. 2014, 256с

130 |
Глава 5 |
|
|
делению максимального вращательного квантового числа r уровня с энергией . Учитывая (5.33), запишем
2 r (r 1) , 2I
откуда
r2 r – 2 I/h 0.
Решение этого уравнения дает rмакс:
rОаЊж |
|
1 |
1 4(2 I / ) |
|
% 2 I 33. |
|
|
|
|||
|
2 |
|
|
||
Следовательно, чисто вращательный спектр данной молекулы содержит около 30 линий.
5.10.Колебательно-вращательная полоса. В середине колебательно-вра- щательной полосы спектра испускания молекул HCl, где отсутст-
вует «нулевая» линия, запрещенная правилом отбора, интервал между соседними линиями равен 0. Найти расстояние между ядрами молекулы НСl.
Р е ш е н и е. Сначала найдем интервал Е между соседними вращательными энергетическими уровнями. Согласно (5.34),
2
E (r 1).
I
Соответствующая ему частота перехода
r E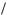 (r 1)
(r 1)  I.
I.
При переходе к соседней линии r меняется на единицу, согласно правилу отбора (5.35), и интервал между соседними линиями
( r) h I h/I,
где r 1. Остается учесть, что в середине колебательно-враща- тельной полосы этот интервал будет вдвое больше, а также выра-
жение (5.37) для момента инерции молекулы. В результате получим 0 2 2h/ d2, откуда
d 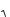
 2
2  0 ,
0 ,
где — приведенная масса молекулы, m1m2/(m1 m2).

Глава 6
Квантование атомов
§ 6.1. Квантование атома водорода
Рассмотрим простейшую систему, состоящую из электрона e, который движется в кулоновском поле ядра с зарядом Zе. Такую систему называют водородоподобной. При Z 1 это атом водорода, при Z 2 — однократно ионизированный атом гелия — ион Не+, при Z 3 — двукратно ионизированный атом лития — ион Li++ и т. д.
Потенциальная энергия взаимодействия электрона с ядром в такой системе равна
U(r) |
Ze |
2 |
, |
(6.1) |
|
|
|||
|
|
r
где r — расстояние между электроном и ядром, которое в первом приближении будем считать точечным (здесь и далее).
Уравнение Шредингера в этом случае имеет вид
|
2 |
|
|
|
|
Ze |
2 |
|
|
|
|
2m |
|
|
|
|
|||
. |
|
/ |
|
|
E |
|
|
/ 0. |
(6.2) |
|
|
|
|
|
|||||
|
|
|
2 |
|
|
r |
|
|
|
|
|
|
|
|
|
|
|
|
|
Поле (6.1), в котором движется электрон, является централь- но-симметричным, т. е. зависит только от r. Поэтому решение уравнения (6.2) наиболее целесообразно проводить в сферической системе координат r, , , где оператор Лапласа . 2 имеет следующий вид:
|
2 |
|
2 |
2 |
|
|
1 |
|
|
|
|
|
1 |
|
2 |
||||||
. |
|
|
|
|
|
|
|
|
|
|
|
|
sin |
|
|
|
|
|
|
. (6.3) |
|
|
|
r r |
r 2 |
|
|
|
r 2 |
|
|
||||||||||||
|
|
|
r 2 |
|
sin |
|
|
sin2 2 |
|||||||||||||
Мы не будем воспроизводить здесь этапы решения уравнения (6.2), поскольку оно слишком громоздко (об этом красноречиво свидетельствует уже сам вид оператора Лапласа). Остановимся лишь на сути процесса решения и на анализе окончательных результатов.

132 |
Глава 6 |
|
|
Решение уравнения (6.2) проводят методом разделения переменных с учетом естественных требований, налагаемых на /-функцию: она должна быть однозначной, конечной, непрерывной и гладкой. В процессе решения обнаруживается, что этим требованиям можно удовлетворить при любых положительных значениях энергии E, но в области отрицательных значений E — только при дискретных значениях E, а именно, если
En |
|
me 2 |
|
Z |
2 |
, |
n 1, 2, 3, ... |
(6.4) |
2 2 |
|
|
|
|||||
|
|
|
n 2 |
|
|
|||
Этот случай (E < 0) для нас представляет особый интерес, поскольку он соответствует связанным состояниям электрона (электрону в атоме).
Таким образом, последовательное решение уравнения Шредингера приводит в случае E < 0 к формуле (6.4) для энергетических уровней — без использования каких-либо дополнительных постулатов (в отличие от первоначальной теории Бора). Кроме того, совпадение с формулой (2.25) означает, что мы пришли к той же самой системе энергетических уровней (см. рис. 2.7). Это же относится и к частотам излучения при переходах между уровнями. Поэтому повторять нет необходимости.
Различие в интерпретации относится только к состояниям электрона: в теории Бора это движение по стационарным орбитам, здесь же орбиты теряют физический смысл, их место за- нимают /-функции.
Собственные функции уравнения (6.2), т. е. /-функции, содержат, как выяснилось, три целочисленных параметра — n, l, m:
/ /nlm(r, , ), |
(6.5) |
где n называют главным квантовым числом (это то же n, что и в выражении для Еn). Параметры же l и m — это орбитальное и магнитное квантовые числа, определяющие по формулам (5.25) и (5.26) модуль момента импульса М и его проекцию Мz.
В процессе решения выясняется, что решения, удовлетворяющие естественным условиям, получаются лишь при значениях l, не превышающих n – 1. Таким образом, при данном n квантовое число l может принимать n значений:
l 0, 1, 2, ... , n – 1. |
(6.6) |
Квантование атомов |
133 |
|
|
В свою очередь, при данном l квантовое число m согласно (5.26) может принимать 2l 1 различных значений:
m 0, 1 1, 1 2, ..., 1 l. (6.7)
Энергия Еn электрона (6.4) зависит только от главного квантового числа n. Отсюда следует, что каждому собственному значению En (кроме случая n 1) соответствует несколько собственных функций /nlm, отличающихся значениями квантовых чисел l и m. Это означает, что электрон может иметь одно и то же значение энергии, находясь в нескольких различных состояниях. Например, энергией E2 (n 2) обладают четыре состоя-
ния: /200, /21–1, /210, /21+1.
Кратность вырождения. Состояния с одинаковой энергией называют вырожденными, а число различных состояний с определенным значением энергии En — кратностью вырождения данного энергетического уровня.
Кратность вырождения n-го уровня водородоподобной системы можно определить, учитывая число возможных значений l и m. Каждому из n значений квантового числа l соответствует 2l 1 значений m. Поэтому полное число N различных состояний для данного n равно
n 1 |
|
N :(2l 1) 1 3 5 … (2n – 1) n2. |
(6.8) |
l 0
Следовательно, кратность вырождения n-го энергетического уровня водородоподобных систем равна n2.
В действительности, как будет показано в дальнейшем (§ 6.3), это число надо удвоить из-за наличия собственного момента (спина) у электрона. Таким образом, кратность вырождения n-го энергетического уровня
N 2n2. |
(6.9) |
Символы состояний. Различные состояния электрона в атоме принято обозначать малыми буквами латинского алфавита в зависимости от значения орбитального квантового числа l:
Квантовое число l |
0 |
1 |
2 |
3 |
4 |
5 |
(6.10) |
|
|
|
|
|
|
|
|
Символ состояния |
|
|
|
|
|
|
|
s |
p |
d |
f |
g |
h |
||
|
|
|
|
|
|
|
|
134 |
Глава 6 |
|
|
Принято говорить о s-состояниях (или s-электронах), p-состоя- ниях (или p-электронах) и т. д.
Значение главного квантового числа n указывают перед символом состояния с данным l. Например, электрон, имеющий главное квантовое число n 3 и l 2, обозначают символом 3d и т. д. Выпишем последовательно несколько состояний электрона:
1s; 2s, 2p; 3s, 3p, 3d; … (6.11)
Собственные функции уравнения (6.2) представляют собой произведение двух функций, одна из которых зависит только
от r, а другая — только от углов и : |
|
/nlm(r, , ) Rnl(r) Ylm( , ), |
(6.12) |
где первый сомножитель зависит от квантовых чисел n и l, второй же — от l и m.
Функция Ylm( , ) является собственной функцией операто-
|
2 |
. Для s-состояний (l 0) эта |
ра квадрата момента импульса M |
|
функция является константой, так что /-функция вида /n00 зависит только от r. Вообще же
Y |
lm |
( , ) > |
( ) eim . |
(6.13) |
|
|
l|m| |
|
В таблицах (6.1) и (6.2) приведен в качестве примера вид наиболее простых функций Rnl(r) и >l|m|( ) с точностью до нормировочных множителей.
|
|
|
Таблица 6.1 |
|
|
|
|
|
|
Состояние |
n, l |
R(( |
|
|
|
|
|
|
|
1s |
1, 0 |
e–( |
|
|
2s |
2, |
0 |
(2–()e–(/2 |
|
2p |
2, |
1 |
(e–(2 |
|
|
|
|
|
|
Таблица 6.2
Состояние |
l, m ? |
>l |m ( ) |
||
s |
0, 0 |
1 |
||
p |
1, |
0 |
cos |
|
1, |
1 |
sin |
||
|
||||
|
|
|
|
|
|
|
|
|
|
Здесь ( r/r1, r1 — боровский радиус (2.24).
В соответствии с формулами (6.12) и (6.13) и этими таблицами представим, как выглядит, например, функция /211:
/ |
Are r /2 r1 sin e i , |
211 |
|
где А — нормировочный коэффициент.