Материал: Иродов. т5 Квантовая физика Основные законы. 2014, 256с
Квантование атомов |
135 |
|
|
Распределение плотности вероятности. В квантовой теории нельзя говорить о траекториях электрона в атоме. Имеет смысл лишь состояние (/-функция) и вероятность местонахождения электрона в том или ином месте в поле ядра. Для наглядности вводят представление об электронном облаке, плотность распределения которого в каждой точке пропорциональна плотности вероятности dP/dV местонахождения электрона в этой точке.
Плотность вероятности местонахождения электрона дается квадратом модуля волновой функции |/|2 или //*. Ограничимся для простоты рассмотрением основного состояния электрона 1s атома водорода, которое является сферически-симметрич- ным, т. е. его /-функция зависит только от r:
/1s T e– r, |
(6.14) |
где 1/r1, r1 — боровский радиус.
Вероятность нахождения электрона в объеме dV, как мы знаем, равна |/|2dV. Возьмем в качестве элементарного объема dV сферический слой толщиной dr и радиусом r: dV 4 r2dr. Тогда вероятность dP нахождения 1s-электрона в этом слое
dP Ar2/2dr, |
(6.15) |
где А — нормировочный коэффициент. Отсюда плотность вероятности dP/dr, т. е. вероятность местонахождения электрона в сферическом слое единичной толщины вблизи радиуса r есть
dP/dr Ar2e–2 r T r2e–2 r. |
(6.16) |
Эту плотность вероятности не следует смешивать с плотностью вероятности dP/dV, отнесенной к единице объема вблизи точки с радиусом-вектором r и равной |/|2.
Видно, что (6.16) обращается в нуль при r & 0 и при r & . Найдем значение r, при котором (6.16) достигает максимума. Для этого продифференцируем (6.16) по r и приравняем нулю полученное выражение (после сокращения на экспоненту). В результате получим наиболее вероятное расстояние электрона от ядра:
rm 1/ r1. |
(6.17) |
136 Глава 6
Мы видим, что rm в точности совпадает с радиусом первой боровской орбиты электрона в атоме водорода (2.24).
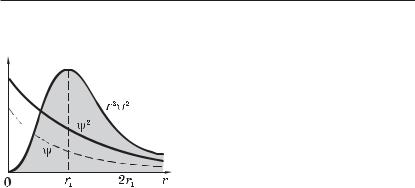
На рис. 6.1 показаны графики
зависимостей /(r), /2(r) и dP/dr T r2/=. Следует обратить внимание на то, что пространственное рас-
пределение в электронном облаке
атома можно характеризовать
либо квадратом модуля пси-функ-
ции |/(r)|2, либо величиной r2|/(r)|2. Первое выражение определяет вероятность местонахождения электрона в единице объема,
второе — в сферическом слое единичной толщины. Их графики существенно отличаются друг от друга, как видно из рисунка.
Заметим, что /1s(r) не является гладкой в точке r 0. Это есть следствие того, что потенциальная энергия электрона при r & 0 обращается в бесконечность (в предположении, что ядро является точечным). Учет конечных размеров ядра устраняет этот дефект /-функции.
Состояние движения электрона в атоме не всегда имеет даже какой-то приближенный аналог. Например, во всех s-состояни- ях орбитальный момент электрона равен нулю (l 0). С классической точки зрения это соответствует движению электрона вдоль радиуса, т. е. электрон при своем движении должен был бы пересекать область, занятую ядром. Это в классике невозможно. В квантовой же теории состояние с нулевым орбитальным моментом существует — это s-состояния электрона, в которых распределение «плотности» электронного облака сфери- чески-симметрично. Итак, в основном 1s-состоянии угловой момент электрона, в отличие от теории Бора, равен нулю.
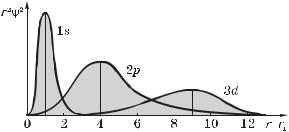
В заключение несколько слов о распределении электронного облака в других состояниях (p, d, …). Здесь оно уже не сфериче- ски-симметрично и в сильной степени зависит от угла . Вместе с тем, выяснилось, что при усреднении по углу остается зави- симость /-функции только от r, и максимумы распределения в состояниях с l n – 1 ( т. е. наиболее вероятные расстояния электрона от ядра) приходятся на соответствующие боровские
Квантование атомов |
137 |
|
|
орбиты. Это показано для трех состояний на рис. 6.2, где на оси абсцисс длинными вертикальными отрезками отмечены радиусы соответствующих орбит в боровской теории атома водорода. Аналогия с теорией Бора на этом скромном (но любопытном) факте и исчерпывается.
Рис. 6.2
§ 6.2. Уровни и спектры щелочных металлов
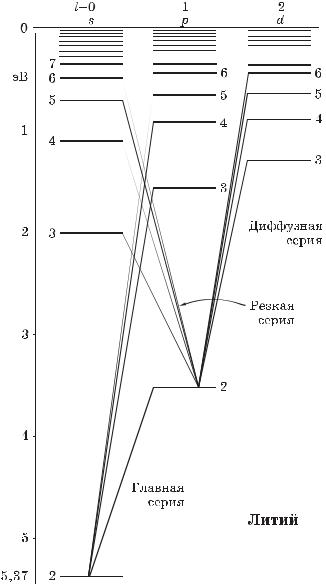
Спектры щелочных металлов. Спектры испускания атомов щелочных металлов, как и спектр атома водорода, состоят из множества спектральных линий. Кропотливая систематика этих спектральных линий позволила сгруппировать их в серии, каждая из которых связана с переходом возбужденного атома на какой-то определенный уровень. Для атомов лития это показано на рис. 6.3.
Схема уровней других щелочных металлов имеет аналогичную структуру.
Анализ полученных результатов позволил сопоставить их с весьма характерной структурой электронной оболочки атомов щелочных металлов. Если атом щелочного металла имеет всего Z электронов, то можно считать, что Z – 1 электронов вместе с ядром образуют сравнительно прочный остов, в электрическом поле которого движется внешний (валентный) электрон, довольно слабо связанный с остовом атома.
В некотором смысле атомы щелочных металлов являются водородоподобными, однако не полностью. Дело в том, что внешний электрон несколько деформирует электронный остов и тем самым искажает поле, в котором движется. В первом приближении поле остова можно рассматривать как суперпозицию поля точечного заряда e и поля точечного диполя, распо-
138 |
|
|
|
Глава 6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 6.3

Квантование атомов |
139 |
|
|
ложенных в центре остова. При этом ось диполя направлена все время к внешнему электрону. Поэтому движение последнего происходит так, как если бы поле остова, несмотря на искажение, сохранялось сферически-симметричным.
Это позволяет представить потенциальную энергию внешнего электрона в поле такого остова как
U(r) |
e 2 |
C |
e |
2 |
, |
(6.18) |
|
r |
r |
2 |
|||||
|
|
|
|
где C — некоторая постоянная.
Решение уравнения Шредингера для электрона с потенциальной энергией (6.18) приводит к тому, что теперь дозволенные значения энергии Е в области Е < 0 (для связанных состояний внешнего электрона) будут зависеть не только от главного квантового числа n (как в случае атома водорода), но и от орбитального квантового числа l:
Enl |
R |
, |
(6.19) |
|
(n #l )2 |
||||
|
|
|
где #l — ридберговская поправка (или квантовый дефект), зависящая от l. Заметим, что у лития (см. рис. 6.3) основным состоянием является 2s, поскольку состояние с n 1 уже занято двумя электронами, входящими в состав остова.
Энергетическому уровню (6.19) соответствует терм, имеющий согласно (2.30) вид
Tnl |
R |
. |
(6.20) |
|
(n #l )2 |
||||
|
|
|
Зависимость энергии электрона от орбитального квантового числа l является принципиальным отличием уровней энергии атомов щелочных металлов от уровней энергии атома водорода. Эта зависимость означает, что в данном случае снимается вырождение по l. Физически это связано с тем, что в атомах щелочных металлов внешний электрон находится в электрическом поле атомного остова. Заряд последнего не точечный, и распределение его несколько отличается от сферически-сим- метричного. Электрическое поле остова уже не кулоновское (не T 1/r2). Благодаря этому и получается зависимость энергии