Материал: Д6868 Цветков ОБ Методы расчета свойств переноса раб веществ хол техн

Для линейных молекул cv,вр = R, тогда, согласно (2.4),
Рекомендуемое значение λ = 3110·10–5 Вт/(м·К) [3].
3. ВЯЗКОСТЬ ГАЗОВЫХ СМЕСЕЙ
Для расчета вязкости бинарных неполярных газовых смесей молекулярно-кинетическая теория предлагает следующую зависимость [1]:
Значения 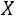 ,
, 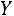 , и
, и 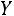 определяют из соотношений
определяют из соотношений
где A12* – функция приведенной температуры T12* = T(ε12/k)–1, определяемая по формуле
26

(3.5)
В расчетах пользуются величиной вязкости гипотетического газа, молекулы которого имеют молекулярную массу, равную 2M1M2/(M1+M2), и взаимодействуют по потенциальной кривой, определяемой параметрами взаимодействия ζ12 и ε12,
Параметры потенциальной функции ζ12 и ε12 определяют из комбинационных правил, приведенных выше.
Молекулярно-кинетическая теория позволяет также рассчитать вязкость многокомпонентных газовых смесей, однако вычисления становятся существенно более сложными и громоздкими. Точность уравнений строгой молекулярно-кинетической теории по сравнению с экспериментальными данными о вязкости газовых смесей во многих случаях невелика. Одной из основных причин этого положения является недостаточное знание особенностей межмолекулярного взаимодействия. Модели потенциалов, с определенными ограничениями «работающие» для индивидуальных газов, в то же время для смесей, состоящих из большего числа различных газов, мало обоснованы [6]. Теоретические уравнения обрастают эмпирическими коэффициентами и формулами, сложными и недостаточно строгими. Это ограничивает возможность применения теоретических формул к практическим задачам, заставляет искать более рациональные методы расчета, основанные на обобщенных закономерностях, справедливых и для составляющих смесь компонентов, и для смеси. С этой точки зрения наиболее приемлемым можно считать метод, предложенный И.Ф. Голубевым и Н.Е. Гнездиловым [7].
Общее уравнение, включающее все возможные по составу варианты газовых смесей, имеет вид [7]
х |
(3.7) |
|
27 |

|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
где |
|
|
|
, |
(3.8) |
|||||||||
, |
|
|
(3.9) |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
При η ≤ 1 до Tсм = 1000–1200 К
Для смесей, содержащих одновременно полярный газ и кислород, являющийся по сравнению с другими газами сильным парамагнитным веществом, показатель степени
Особый класс смесей – смеси, содержащие гелий. В этом случае расчетное уравнение имеет вид
28

где
При расчетах определяющие смесь параметры вычисляются в соответствии с законом аддитивности:
Для всех неуглеводородов принимается n = 1, а для полярных молекул, не содержащих атомы водорода, μ = 0. Уравнения (3.7)– (3.14) позволяют вычислять вязкость смесей: неполярных газов, неполярных и полярных газов, полярных газов, а также смесей, содержащих кислород и гелий. Для расчета необходимо знать молекулярные массы компонентов, критические температуры, давления и дипольные моменты индивидуальных газов, составляющих смесь.
29

Примеры расчета
3.1. Определить вязкость смеси следующего мольного состава:
60,22 % H2 и 39,78 % CH4 при T = 473,15 К.
Расчет. Параметры потенциала (6-12) Леннарда-Джонса возьмем из табл. 1.4. Обозначим индексом 1 параметры водорода и ин-
дексом 2 параметры метана. Имеем: ε1/k = 38 К; ζ1 |
= 2,915·10–10 м; |
ε2/k = 163,6 К; ζ2 = 3,697·10–10 м. |
|
Определяем значения приведенных температур: |
|
; |
. |
Параметры потенциала для смеси находим с помощью комбинационных правил
Определяем
.
Из табл. 1.2 найдем: для |
; для |
; |
для |

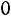
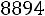 .
.
По формуле (1.7) вычисляем вязкость:
–водорода
–метана
30