Материал: Д6868 Цветков ОБ Методы расчета свойств переноса раб веществ хол техн

Расшифровка входящих в уравнения (1.1)–(1.3) величин для модели газа, состоящего из твердых сфер, позволяет уточнить приведенные выше зависимости для коэффициентов переноса [1]
Из уравнений (1.4)–(1.6) видно, что коэффициент диффузии изменяется пропорционально абсолютной температуре в степени 3/2 и обратно пропорционально давлению. Вязкость и теплопроводность независимы от давления и возрастают с повышением температуры как квадратные корни из Т. Все свойства переноса обратно пропорциональны квадрату диаметра молекул.
Соотношения (1.4)–(1.6) справедливы для молекул, являющихся твердыми сферами. Для молекул реальных газов их использование ограничено. Вместе с тем из соотношений (1.4)–(1.6) вытекает целый ряд практически полезных выводов. Здесь представляет интерес, в частности, рассмотрение безразмерных комплексов: критериев Прандтля 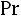

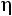
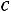
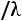 и Шмидта
и Шмидта 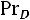

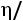
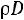
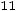 .
.
Поскольку отношение удельных теплоемкостей 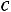
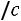 для одноатомных газов (а именно для этих газов наиболее близка к действительности модель твердых сфер) теоретически постоянно и равно 5/3, значение критерия Прандтля должно быть постоянно и равно 0,67, а критерий Шмидта (часто его называют также диффузионным критерием Прандтля) должен иметь значение 0,83. Экспериментальные значения этих комплексов при t = 0 °С и р = 0,101 МПа приведены в табл. 1.1 [1].
для одноатомных газов (а именно для этих газов наиболее близка к действительности модель твердых сфер) теоретически постоянно и равно 5/3, значение критерия Прандтля должно быть постоянно и равно 0,67, а критерий Шмидта (часто его называют также диффузионным критерием Прандтля) должен иметь значение 0,83. Экспериментальные значения этих комплексов при t = 0 °С и р = 0,101 МПа приведены в табл. 1.1 [1].
6
Таблица 1.1
Значения критериев Прандтля и Шмидта
|
|
|
|
Газ |
|
|
|
|
Критерий |
|
|
|
|
|
|
|
|
Ne |
Ar |
N2 |
CH4 |
O2 |
CO2 |
H2 |
||
|
||||||||
|
|
|
|
|
|
|
|
|
Pr |
0,66 |
0,67 |
0,71 |
0,74 |
0,72 |
0,75 |
0,71 |
|
|
|
|
|
|
|
|
|
|
PrD |
0,73 |
0,75 |
0,74 |
0,70 |
0,74 |
0,71 |
0,73 |
|
|
|
|
|
|
|
|
|
Уравнения для расчета свойств переноса, выведенные из представлений элементарной кинетической теории газов, не являются строгими. При описании свойств реальных газов необходимо учитывать сложный характер межмолекулярного взаимодействия, поскольку реальные молекулы притягиваются друг к другу на больших расстояниях и отталкиваются друг от друга, когда межмолекулярное расстояние становится очень малым (порядка 10–10 м).
Межмолекулярные силы бывают двух типов: коротко- и дальнодействующие. Короткодействующие силы чаще называют валентными или химическими силами. Короткодействующие силы возникают тогда, когда молекулы настолько сближаются друг с другом, что их электронные облака перекрываются.
Среди дальнодействующих сил можно выделить три составляющие: электростатическую, индуцированную и дисперсионную.
Электростатическая составляющая межмолекулярных сил проявляется как воздействие электрических сил, если взаимодействующие молекулы обладают дипольными моментами. Диполи притягиваются друг к другу, происходит взаимная ориентация молекул. Это дает основание в ряде работ называть электростатическую составляющую ориентационным межмолекулярным взаимодействием.
Каждая молекула обладает поляризуемостью. Индуцированная составляющая характеризует, таким образом, взаимодействие индуцированных диполей, вызванных воздействием на молекулу внешних сил, например, электрического поля.
Более сложным является дисперсионное взаимодействие, которое для неполярных молекул является главной составляющей сил,
7
действующих на больших расстояниях (нередко ее называют силой Ван-дер-Ваальса). Дело в том, что, хотя в среднем дипольный момент неполярной молекулы равен нулю, в отдельные мгновения он отличен от нуля, и поэтому взаимодействие неполярных молекул возможно. Предложенная здесь картина взаимодействия, естественно, упрощена, и строгий расчет дисперсионного взаимодействия возможен лишь в рамках квантово-механических представлений.
За исключением случаев взаимодействия простейших молекул, строгий расчет сил межмолекулярного взаимодействия выходит за рамки современных вычислительных возможностей, поэтому конструируют различные модельные потенциалы, описывающие основные свойства межмолекулярного взаимодействия и включающие в себя небольшое число (два-четыре) свободных параметров, значения которых подбирают, исходя из экспериментальных данных, в частности, о свойствах переноса.
На рис. 1.1 схематически изображены различные модельные потенциалы межмолекулярного взаимодействия, которые оказались достаточно полезными и часто применяются. Рассмотрим некоторые качественные и количественные аспекты этих потенциалов [1].
Потенциал твердой сферы
Это простейшая, так называемая однопараметрическая модель (рис. 1.1, а). Она содержит только один параметр – диаметр сферы 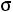 . Модель наглядна, но далека от реальности, поскольку на малых расстояниях потенциал взаимодействия θ(r) растет слишком круто, а на больших расстояниях модель совершенно не учитывает межмолекулярного взаимодействия
. Модель наглядна, но далека от реальности, поскольку на малых расстояниях потенциал взаимодействия θ(r) растет слишком круто, а на больших расстояниях модель совершенно не учитывает межмолекулярного взаимодействия
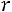
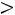
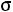 .
.
Эту модель использовали в элементарной кинетической теории газа, о чем упоминалось ранее.
8
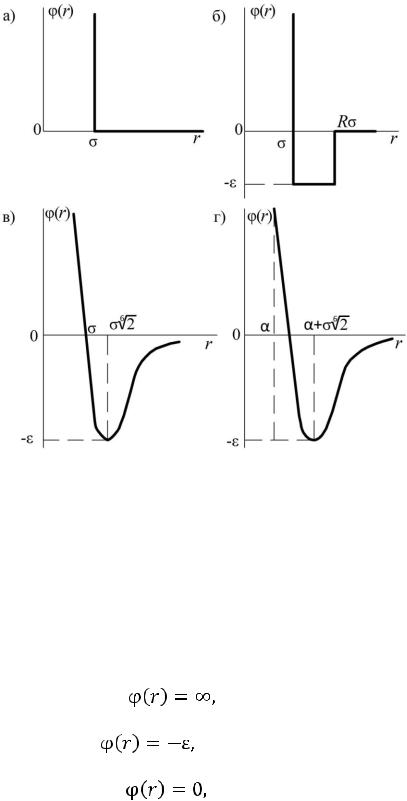
Рис. 1.1. Графическое представление модельных потенциалов:
а – модель твердой сферы; б – модель прямоугольной ямы; в – потенциал Леннарда–Джонса; г – потенциал Кихары
Модель прямоугольной потенциальной ямы
Эта модель принимает в расчет как силы отталкивания, так и силы притяжения (рис. 1.1, б). Она имеет вид
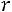
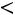
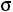 ;
;
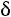
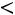
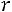
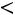
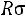 ;
;
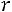
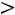
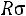 .
.
9

Модель содержит три произвольных параметра: ζ, ε, Rζ (Rζ – численный коэффициент). Потенциал прямоугольной ямы удобен в расчетах и в ряде случаев позволяет получить хорошие результаты.
Потенциал Леннарда-Джонса
Модель Леннарда-Джонса (рис.1.1, в) имеет достаточно широкое применение и описывается уравнением вида
.
Первый член уравнения описывает энергию отталкивания, второй – энергии притяжения. Это уравнение обычно записывают как
и называют потенциалом (6-12) Леннарда-Джонса. Параметры ε и ζ являются постоянными, характеризующими химическую разновидность взаимодействующих молекул. Параметр ζ определяет значение расстояния r между молекулами, при котором потенциал взаимодействия θ(r) = 0. Величина ε – максимальное значение энергии притяжения (глубина потенциальной ямы), которое соответствует r = 21/6ζ.
Потенциал Леннарда-Джонса имеет достаточно близкую к реальной картине межмолекулярного взаимодействия форму, однако выбор значений показателей степени 6 и 12 не является единственно возможным. В ряде работ предложены другие, более подходящие, значения параметров потенциала δ и γ, например, δ = 18.
Потенциал Кихары
Потенциал Кихары (рис. 1.1, г) имеет вид
где ρ = r – a.
10