Материал: Бодунов Физика учебник

Например, электрону, прошедшему ускоряющую разность потенциалов U = 10 В, соответствует длина волны де Бройля 0,388 нм.
Гипотеза де Бройля явилась мощным революционным толчком к развитию новых представлений о природе материальных объектов и привела к созданию квантовой механики.
Опыты по дифракции частиц. Первое экспериментальное подтверждение гипотезы де Бройля было получено в 1927 г. К. Девиссоном и Л. Джермером. Они обнаружили, что пучок электронов, рассеиваясь на кристалле никеля, дает дифракционную картину, совпадающую с картиной рассеяния на кристалле коротковолнового рентгеновского излучения. Кристалл никеля в этих экспериментах играл роль дифракционной решетки. По положению дифракционных максимумов была определена длина волны электронов, которая соответствовала ее длине, вычисленной по формуле де Бройля.
Впоследствии дифракционные явления были обнаружены также для нейтронов, протонов, атомных и молекулярных пучков.
Экспериментальное доказательство существования волновых свойств микрочастиц привело к выводу, что это – универсальное свойство материи. Таким образом, волновыми свойствами должны обладать и макроскопические тела. Однако вследствие большой массы макроскопических тел их волновые свойства не могут быть обнаружены экспериментально. Например, пылинка массой 10–9 г, движущаяся со скоростью 0,5 м/с, имеет длину волны де Бройля порядка 10–21 м, что на одиннадцать порядков меньше размеров атомов. Такая длина волны лежит в области, не доступной для наблюдения. Следовательно, макроскопические тела могут проявлять только корпускулярные свойства.
2.6. Волновая функция. Уравнение Шредингера
Волновая функция. Результаты интерференционных опытов с микрочастицами показывают, что поведение данных частиц носит случайный характер, и, следовательно, их состояние может быть описано с помощью вероятностных методов. В этом заключается важнейшая особенность квантовой механики– раздела физики, в котором изучаются свойства микромира.
Вквантовой механике каждому микрообъекту (например, электрону
ватоме) ставится в соответствие функция координат и времени Ψ(x, y, z, t), которая характеризует состояние микрочастицы, т. е. ее положение, импульс, энергию и т. д. Эту функцию принято называть Ψ-функцией. Она обладает свойствамиклассическихволн, поэтомуназываетсятакжеволновой функцией.
Физический смысл волновой функции заключается в следующем: квад-
рат ее модуля (x, y, z,t) 2 определяет вероятность dW того, что микроча-
60

стица может быть обнаружена в момент времени t в пределах объема dV с координатами x, y и z:
dW (x, y, z,t) 2 dV.
Из этого выражения видно, что 2 dW / dV (т. е. квадрат модуля
волновой функции) есть плотность вероятности (отношение вероятности dW к объему dV) нахождения частицы в данном месте пространства.
Из физического смысла волновой функции следует, что квантовая механика не позволяет определить положение частицы или ее траекторию, но может предсказать, с какой вероятностью частица может быть обнаружена в разных точках пространства.
С помощью волновой функции можно найти средние значения физических величин, характеризующих состояние микрочастицы, – координаты, импульса, энергии и т. д.:
Xср(t) X (x, y, z, t 2 dxdydz,
где X – физическая величина. Так, например, среднее значение радиуса орбиты электрона rср в атоме водорода
rср r 2 dr.
Уравнение Шредингера. Выражение волновой функции находят из уравнения Шредингера (1926 г., Э. Шредингер) – основного уравнения квантовой механики.
В стационарном случае, т. е. когда волновая функция не зависит от времени (Ψ = Ψ(x, y, z)), уравнение Шредингера записывают следующим образом:
2m 2x2 2y2 2z2 U (x, y, z) E ,
где m – масса частицы; U и E – ее потенциальная и полная энергия. Выражение в скобках часто обозначают символом
x22 y22 z22 ,
называемым оператором Лапласа, с помощью которого уравнение Шредингера принимает вид
61

U (x, y, z,t) E . 2m
Таким образом, решив это уравнение, можно найти волновую функцию и с ее помощью определить вероятность нахождения частицы в разных точках пространства, а также средние значения характеризующих ее физических величин.
Квантование энергии. Из уравнения Шредингера и условий, налагаемых на волновую функцию, вытекает важный вывод, что энергия частицы квантуется, т. е. принимает строго определенные значения (собственные значения), совокупность которых (E1, E2,…, En,…) называется спектром энергий. Соответствующие этим значениям энергии волновые функции (Ψ1, Ψ2,…,
Ψn,…) называются собственными функциями.
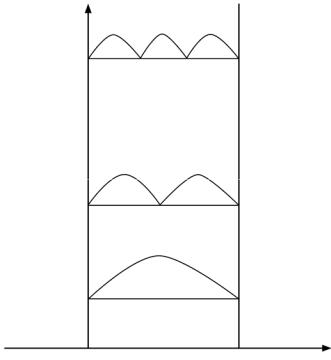
Так, решение уравнения Шредингера для микрочастицы массой m, находящейся в бесконечно глубокой одномерной потенциальной яме шириной l (рис. 2.5), на границах которой потенциальная энергия U = ∞, а внутри ямы U = 0, приводит к следующему результату.
Собственные волновые функции Ψ(x), определяющие вероятность нахождения микрочастицы в потенциальной яме, имеют вид
n (x) |
2 sin |
n x |
, |
|
2 |
||||
|
l |
|
где n – целое число, равное 1, 2, 3,…
Соответствующие волновым функциям Ψn собственные значения энергии En оказываются кратными целому числу n:
En 2h2 n2.
2ml2
На рис. 2.5 схематически изображены потенциальная яма, первые три энергетических уровня и плотность вероятности (x) 2 нахождения частицы
в разных точках ямы для n = 1, 2, 3.
Из рисунка видно, что, например, в состоянии с наименьшей энергией (n = 1) частицу с наибольшей вероятностью можно обнаружить в центре ямы, в состоянии с n = 2 – в середине первой и второй частей ямы.
Разность энергий между двумя ближайшими уровнями энергии в яме
En En 1 En 2h2 (2n 1). 2ml2
При больших значениях n (n>>1)
En 2h22 n. ml
62
E |Ψ (x)|2
E3 |
n = 3 |
E2 |
n = 2 |
|
E1 |
|
n = 1 |
U = |
U = 0 |
|
U = |
|
0 |
l |
x |
|
Рис. 2.5 |
|
|
Оценка этой разности для молекулы водорода H2 (m = 3,34·10–27 кг), находящейся в сосуде с диаметром l = 0,1 м, дает следующий результат:
E 3,142 (6,62 10 34 ) n 1,3 10 40 n Дж 8,1 10 20 n эВ. 3,34 10 27 0,12
Это значение столь мало, что квантование энергии практически не сказывается на характере движения молекулы в сосуде. Действительно, при комнатной температуре (T = 300 К) тепловая энергия молекулы равна примерно kT = 4·10–2 эВ (k – постоянная Больцмана), т. е. во много раз превосходит E, и поэтому учитывать квантовый характер поведения молекулы газа не
имеет практического смысла.
Однако для электрона (me = 9,1·10–31 кг) в атоме водорода (l = 10–10 м) E составляет приблизительно 102n эВ, т. е. становится значительной, и ее необходимо учитывать.
2.7. Принцип неопределенностей Гейзенберга
Экспериментальные исследования свойств микрочастиц показали, что точность определения их координат, энергии, импульсов и т. д. ограничена и регулируется сформулированным в 1927 г. В. Гейзенбергом принципом не-
63

определенности. Согласно этому принципу при одновременном определении (т. е. измерении в один и тот же момент времени) координат и импульса частицы неопределенности координат x, y, z и неопределенности проекций импульса на соответствующие оси координат (x, y и z) px, py, pz связаны неравенствами
x px 2 , y py 2 , z pz 2 ,
получившими название соотношений неопределенностей Гейзенберга.
Данные соотношения надлежит понимать следующим образом: микрочастицы, в принципе, не имеют одновременно точных значений координаты и соответствующей проекции импульса. Это связано не с ограниченной разрешающей способностью приборов и техники эксперимента, а отражает фундаментальный закон природы – двойственность корпускулярно-волновых свойств микрочастиц.
Так как проекция импульса частицы на ось x составляет px = m vx , со-
отношение неопределенностей Гейзенберга для координаты х и импульса можно переписать в виде
x vx 2m .
Следовательно, чем больше масса m частицы, тем меньше неопределенности ее координаты хиимпульса рх и темс большейточностью к этой частице применимо понятие траектории.
Аналогичные соотношения справедливы для энергии частицы и ее импульса:
E t 2h .
Здесь E – неопределенность энергии системы в данном состоянии; t – интервал времени (время жизни), в течение которого это состояние существует.
64