Материал: Бодунов Физика учебник
3. ЭЛЕМЕНТЫ АТОМНОЙ ФИЗИКИ
3.1. Строение атома
Ядерная модель атома Резерфорда. Э. Резерфорд с сотрудниками изу-
чал прохождение α-частиц через тонкие металлические фольги из золота и платины (рис. 3.1). Альфа-частицы – положительно заряженные частицы с зарядом 2е и массой, в 7300 раз превышающей массу электрона. Они возникают при радиоактивных превращениях.
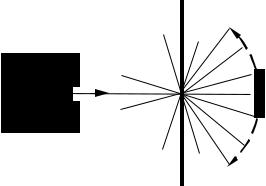
В опытах Э. Резерфорда источником α-частиц служили ядра урана (1), находившегося в свинцовом контейнере (2). Скорость вылетающих α-частиц
составляла 1,4 107 м/с. В виде узкого пучка эти частицы направлялись на тонкую фольгу (3) перпендикулярно ее поверхности. Рассеянные фольгой α-час- тицы регистрировалисьнаэкране(4), покрытомвеществом(сцинтиллятором), способным светиться при попадании на него частиц.
1
2 |
4 |
3
Рис. 3.1
Результаты опытов показали, что большинство α-частиц, прошедших через фольгу, почти не меняло направления своего движения. Однако некоторые α-частицы отклонялись на угол, достигавший 135–150°.
В 1911 г. Э. Резерфорд на основе результатов анализа своих исследований предложил ядерную (планетарную) модель атома. Согласно этой модели атом состоит из ядра и движущихся по замкнутым орбитам вокруг него электронов, образующих электронную оболочку атома. Размер атома порядка 10–10 м. Ядро имеет положительный заряд Zе (Z – порядковый номер элемента в Периодической системе элементов Менделеева, е – элементарный заряд). Размер ядра значительно меньше размера атома и составляет 10–15–10–14 м, его масса практически равна массе атома. Поскольку атомы нейтральны, заряд ядра равен суммарному заряду электронов, т. е. электронная оболочка ядра содержит Z электронов.
65

В рамках этой модели результаты опытов Резерфордаобъясняются следующим образом. Угол рассеяния α-частицы зависит от расстояния, на котором она пролетает вблизи ядра. Поскольку масса α-частицы почти в 2000 раз больше массы электрона, при прохождении через ее электронное облако эти частицы почти не отклоняются от первоначального направления, т. е. не рассеиваются. При пролете на малых расстояниях от ядра α-частица испытывает большую силу кулоновского отталкивания от массивного положительно заряженного ядра и поэтому рассеивается на больший угол. Так как размер ядра значительно меньше размера атома, число α-частиц, рассеянных на большой угол, значительно меньше числа α-частиц, прошедших фольгу без рассеяния.
Воспользовавшись законом Кулона, Э. Резерфорд получил формулу, связывающую число α-частиц, рассеянных на некоторый угол, со скоростью α-частиц и зарядом ядра. Результаты опытов полностью подтвердили ее справедливость, позволили оценить размер ядра и послужили важным доказательством правильности ядерной модели атома.
Однако некоторые экспериментальные факты и представления классической физики вошли в противоречие с предложенной моделью. Так, электрон, вращающийся вокруг ядра по круговой орбите радиусом r, движется с центростремительным ускорением v2/r, сообщаемым кулоновской силой. Согласно классической электродинамике ускоренно движущиеся заряженные частицыдолжныизлучатьэлектромагнитныеволны ивследствиеэтогонепрерывно терять энергию. В результате электроны должны приближаться к ядру и в конце концов упасть на него. Однако атом остается стабильным.
В соответствии со вторым законом Ньютона для электрона, движущегося в кулоновском поле ядра с зарядом Ze (Z – порядковый номер элемента в Периодической системе элементов Менделеева) по окружности радиусом r, справедливо равенство
Ze2 mev2 , 4 0r2 r
где тe – масса электрона; 0 – электрическая постоянная.
Согласно этому уравнению существует бесчисленное множество допустимых значений радиуса и соответствующих ему значений скорости (а значит, и энергии). Следовательно, при переходе электрона с орбиты на орбиту может испускаться в виде волны любая, а не вполне определенная порция энергии, т. е. спектры атомов должны быть сплошными. В действительности же атомы имеют линейчатый спектр.
Попытки построить модель атома в рамках классической физики не привели к успеху. Преодоление возникших трудностей потребовало создания квантовой теории атома.
66

Линейчатый спектр атома водорода. Спектры излучения разрежен-
ных газов(т. е. индивидуальных атомов) имеют линейчатую структуру, состоящую из отдельных спектральных линий. Самым простым и наиболее изученным является спектр атома водорода – самого простого атома, состоящего из ядра и одного электрона.
И. Бальмер подобрал эмпирическую формулу (обобщенная формула Бальмера), описывающую все известные в то время спектральные линии атома водорода в видимой области спектра:
R m12 n12 , n m,
где R = 3,29·1015 с–1 – постоянная Ридберга; n и m – целые числа. Разным m соответствуют разные спектральные серии: при m =1
|
1 |
|
|
1 |
|
|
||||||
R |
|
|
|
|
|
|
|
|
|
|
|
|
2 |
n |
2 |
||||||||||
|
|
|
|
|
||||||||
1 |
|
|
|
|
|
|
||||||
– ультрафиолетовая серия Лаймана, |
|
|
|
|
|
|
|
|
|
|
|
|
при m = 2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
1 |
|
|
||||||
R |
|
|
|
|
|
|
|
|
|
|
|
|
2 |
2 |
|
|
n |
2 |
|
||||||
|
|
|
|
|
|
|
|
|||||
– серия Бальмера (видимая область спектра), при m = 3
R 12 12
3 n
–инфракрасная серия Пашена и т. д.
Сувеличением n (номер линии в серии) расстояние (энергетический зазор) между линиями в каждой серии уменьшается.
Постулаты Бора. В 1913 г. Н. Бор построил первую качественно новую, квантовую, теорию атома. В основе теории Бора лежат два постулата.
Первый постулат Бора (постулат стационарных состояний). В атоме существуют стационарные (не изменяющиеся со временем) состояния – орбиты электронов, движение по которым не сопровождается излучением электромагнитных волн. Эти орбиты выделяются среди других тем, что на них электрон в атоме водорода имеет строго определенные дискретные (квантовые) значения момента импульса
L mvr n 2h n .
67
Здесь n = 1, 2, 3, … Соответственно энергия электрона на каждой из этих орбит имеет определенное значение Еn. Другие значения энергии невозможны.
Второй постулат Бора (правило частот). При переходе электрона с одной стационарной орбиты на другую атом излучает (или поглощает) один фотон с энергией
h En Em ,
где Еn и Em – энергии стационарных состояний атома.
Переход атома из состояния с большей энергией в состояние с меньшей энергией (Еm < Еn), т. е. переход электрона с более удаленной от ядра орбиты на более близкую, сопровождается излучением фотона. Переход атома в состояние с большей энергией (Еm > Еn), т. е. переход электрона на более удаленную от ядра орбиту, характеризуется поглощением фотона. Совокупность дискретных частот = (En – Em)/h квантовых переходов и определяет линейчатый спектр атома.
Боровская теория атома водорода. Сформулированные Бором посту-
латы позволили вычислить радиусы разрешенных орбит и энергию электрона на них для атома водорода (Z = 1). Решая систему из двух уравнений, первое из которых представляет собой уравнение движения электрона по круговой орбите радиусом r, записанное на основе второго закона Ньютона, а второе – первый постулат Бора,
|
v2 |
|
1 |
|
e2 |
|
|
m |
r |
|
|
|
r2 |
, |
|
4 0 |
|||||||
|
|
|
|
||||
|
|
n , |
|
|
|
||
mvr |
|
|
|
||||
получаем радиусы стационарных орбит электрона
r |
4 0 2 |
a |
n2 , |
а |
|
4 0 2 |
, n = 1, 2, 3,… |
|
|||||||
n |
e2m |
0 |
|
0 |
me2 |
|
|
|
|
|
|
|
|
||
Радиус первой орбиты атома водорода (r1 = a0 = 0,528·10–10 м) назы-
вается боровским радиусом.
Полная энергия электрона в атоме водорода есть сумма его кинетической и потенциальной энергии:
E mv2 |
|
e2 |
1 |
e2 |
|
me4 |
|
1 |
hR , |
|
|
|
|
|
|||||||
n |
2 |
|
4 0r |
2 4 0r |
|
8h2 02 n2 |
n2 |
|||
|
|
|
||||||||
68
где R |
me4 |
– постоянная Ридберга; hR = 13,6 эВ. Здесь введена принятая |
3 2 |
||
|
8h 0 |
|
в задачах атомной и ядерной физики единица измерения энергии электронвольт (эВ). 1 эВ – величина, численно равная работе по перемещению элементарного заряда е между точками с разностью потенциалов U = 1 В:
1 эВ = e∆U = 1,6·10–19 Кл·В = 1,6·10–19 Дж.
Из формулы энергии электрона в атоме следует, что энергия состояния атома зависит от значения n. Целое число n называется главным квантовым числом. Энергетическое состояние с n = 1 называется основным состоянием, состояния с n > 1 – возбужденными.
Изменяя значения n, получаем возможные уровни энергии атома водорода (Z = 1). С увеличением n энергия атома водорода возрастает, оставаясь отрицательной, и при n→ энергетические уровни приближаются к границе – значению E∞ = 0. Таким образом, атом водорода имеет минимальную энергию(E1 = –13,6 эВ) в основномсостоянии (n = 1) и максимальную(Е = 0) при n = . Значения Е ≥ 0 соответствуют ионизированному атому – отрыву от него электрона. При положительных значениях энергии электрон становится свободным (радиус орбиты бесконечен).
Согласно второму постулату Бора переход атома водорода (Z = 1) из возбужденного стационарного состояния n в стационарное (возбужденное или основное) состояние т с меньшей энергией сопровождается испусканием кванта с частотой
|
E E |
m |
|
1 |
|
1 |
|
|
n |
R |
|
|
|
. |
|
h |
|
|
m2 |
||||
|
|
n2 |
|
|
|||
Эта формула совпадает с обобщенной формулой Бальмера и описывает все известные спектральные линии атома водорода (рис. 3.2, сплошные стрелки, направленныевниз, соответствуютизлучению, штриховые– поглощению).
В основном состоянии (n = 1) электрон имеет наименьшее значение
полной энергии Е1 = –hR = –13,6 эВ и наименьшее значение радиуса орбиты a0 = 0,528·10–10 м.
К серьезным недостаткам теории Бора следует отнести невозможность объяснить интенсивность спектральных линий и описать спектры других атомов кроме атома водорода, в том числе и атома гелия (Z = 2) – атома, следующего в Периодической системе элементов Менделеева за атомом водорода и имеющего два электрона в электронной оболочке ядра.
69